Professional Documents
Culture Documents
Laboratorio Enlace Quimico
Uploaded by
Laurita Molina CabreraOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Laboratorio Enlace Quimico
Uploaded by
Laurita Molina CabreraCopyright:
Available Formats
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
INTRODUCCION En el desarrollo de esta actividad se va a tratar las propiedades de los enlaces qumicos, conceptos de conductividad elctrica de ellos que dieron a los qumicos los fundamento spara entender cmo se forman las molculas y los compuestos. La propuesta que dio Lewis de los elementos que se combinan para alcanzar la configuracin electrnica ms estable, cuando los tomos se interactan para formar un enlace qumico, slo entra en contacto sus regiones ms externas. Por eso cuando se estudian los enlaces qumicos se miran los electrones de valencia .El enlace qumico tiene dos formas como el enlace covalente y el inico. El enlace covalente polar y apolar es la combinacin de uno o ms pares de electrones entre dos tomos, este enlace no conduce la electricidad y tienen bajos puntos de fusin y el enlace inico es la transferencia de electrones de un tomo a otro, fundidos o en soluciones acuosas son buenos conductores de electricidad y presentan altos puntos de fusin.
LABORATORIO DE QUIMICA
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
I.OBJETIVO
Investigar el tipo de enlace qumico a travs de la conductividad elctrica. Con la propiedad de la solubilidad identificar el tipo de enlace de tipo inico, covalente polar, covalente apolar.
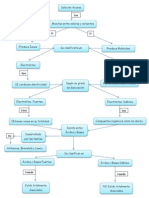
II.FUNDAMENTOS ENLACE QUIMICO
TIPOS ENLACES QUIMICOS: ENLACE IONICO
Resulta de la interaccin electrosttica entre iones, que suele ser el resultado de la transferencia neta de uno o ms electrones de un tomo o un grupo de tomos. Caracterstica de los compuestos inicos: Son slidos con altos puntos de fusin (tpicamente >400C). Muchos son solubles en disolventes polares como el agua. Casi todos son insolubles en disolventes polares, como hexano, C6H14 y tetracloruro de carbono, CCl4. Los compuestos fundidos son buenos conductores de la electricidad porque tiene cargada (iones) mviles Suelen formar entre dos elementos con electronegatividad muy diferente, de ordinario un metal y un no metal.
LABORATORIO DE QUIMICA
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
EJEMPLOS LiF LiCl LiBr NaF NaCl NaBr KF KCL ENLACE COVALENTE Resulta de la comparticin de uno o mas pares de electrones entre dos atomos ; estos dos tipos enlaces presentan los extremos. Todos los enlaces entre atomos distintos tienes al menos cierto grado de carcter ionico como covalentes. Caracterstica de los compuestos covalentes: Son gases lquidos o solidos de bajo punto de fusin (tpicamente <300C). Muchos son insolubles en disolventes polares. Casi todos son solubles en disolventes no polares, C6H14 y tetracloruro de carbono, CCl4. Los compuestos lquidos y fundidos no conducen la electricidad. Las disoluciones acuosas suelen ser malas conductoras de la electricidad, porque la mayor parte no posee partculas cargadas Suelen formarse entre dos elementos con electronegatividad semejante, de ordinario no metales.
LABORATORIO DE QUIMICA
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
Enlace covalente polar Enlace covalente polar Se origina cuando uno de los tomos dispone de mayor fuerza de atraccin de los electrones hacia su ncleo, como resultado se origina una molcula con parte negativa y otra parte positiva (dipolo). Los enlaces covalentes polares siempre se producen cuando el enlace se realiza entre 2 tomos diferentes. El grado de polaridad de la molcula resultante del enlace covalente, depende de la fuerza o atraccin que atrae los electrones hacia un tomo, este concepto es definido mediante la electronegatividad. Enlace covalente polar Enlace covalente polar Se origina cuando uno de los tomos dispone de mayor fuerza de atraccin de los electrones hacia su ncleo, como resultado se origina una molcula con parte negativa y otra parte positiva (dipolo). Los enlaces covalentes polares siempre se producen cuando el enlace se realiza entre 2 tomos diferentes. El grado de polaridad de la molcula resultante del enlace covalente, depende de la fuerza o atraccin que atrae los electrones hacia un tomo, este concepto es definido mediante la electronegatividad. Como ejemplos de enlaces covalentes polares podemos citar el agua, alcohol isoproplico.
LABORATORIO DE QUIMICA
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
Enlace covalente apolar Enlace covalente apolar - Se produce cuando ambos tomos disponen de la misma fuerza de atraccin de los electrones hacia su mismo ncleo. Los enlaces covalentes polares siempre se producen cuando el enlace se realiza entre 2 tomos iguales o con el mismo grado de electronegatividad. El concepto de molcula o material polar o apolar es de suma importancia para el estudio de los adhesivos, por lo general aquellas superficies que dispongan de molculas o materiales polares sern buenas para realizar un pegado o adhesivado. Un ejemplo claro es la molcula de Cloro, el cloro en estado natural se presenta como una molcula formada por 2 tomos de cloro, dichos tomos de cloro se encuentran unidos mediante un enlace covalente producido por la comparticin de 2 electrones
Durante este proceso 2 tomos se han unido para formar una molcula, obviando la teora de los orbitales moleculares enlazantes / antienlazantes y con objeto de explicarlo de una manera sencilla, podemos decir que 2 orbitales atmicos (Cl + Cl) se unen para formar un nuevo orbital molecular (Cl2).
LABORATORIO DE QUIMICA
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
ENLACE METALICO Para explicar las propiedades caractersticas de los metales (su alta conductividad elctrica y trmica, ductilidad y maleabilidad) se ha elaborado un modelo de enlace metlico conocido como modelo de la nube o del mar de electrones: Los tomos de los metales tienen pocos electrones en su ltima capa, por lo general 1, 2 3. stos tomos pierden fcilmente esos electrones (electrones de valencia) y se convierten en iones positivos, por ejemplo Na+, Cu2+, Mg2+. Los iones positivos resultantes se ordenan en el espacio formando la red metlica. Los electrones de valencia desprendidos de los tomos forman una nube de electrones que puede desplazarse a travs de toda la red. De este modo todo el conjunto de los iones positivos del metal queda unido mediante la nube de electrones con carga negativa que los envuelve.
LABORATORIO DE QUIMICA
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
III.EXPERIMENTAL
Materiales de equipo de conductividad elctrica Reactivos:
CuSO4 NaCl cido actico (CH3COOH) Tetracloruro de Carbono (CCl4) Tolueno(CH3-C6H5) Sacarosa (C12H22O11) H2O (Agua destilada) H2O(Agua Potable)
VI.PROCEDIMIENTO
1. Verificamos si cada una sustancias era buenos conductores de la electricidad NaCl
CuSO4
LABORATORIO DE QUIMICA
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
SACAROSA
AGUA PURA
AGUA POTABLE
LABORATORIO DE QUIMICA
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
ACIDO ACETICO (CH3COOH)
TETRACLORURO DE CARBONO CCl4
LABORATORIO DE QUIMICA
9
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
TOLUENO
BENCENO
LABORATORIO DE QUIMICA
10
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
MEZCLAS AGUA PURA + TOLUENO
AGUA PURA + NaCl
LABORATORIO DE QUIMICA
11
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
AGUA PURA + ACIDO ACETICO
AGUA PURA + BENCENO
AGUA PURA + SACAROSA
AGUA
LABORATORIO DE QUIMICA
PURA
12
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
+ CuSO4
BENCENO + CuSO4
LABORATORIO DE QUIMICA
13
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
VI. RESULTADO
CLORURO DE SODIO (NaCl): Puro no conduce electricidad porque es un compuesto inico, por lo tanto es un conductor de segundo orden, es decir, conduce electricidad en solucin acuosa o fundido. CuSO4 Conductividad: Puro no conduce electricidad por ser un compuesto inico, ya que a temperatura ambiente (25C) es un slido de aspecto cristalino. CuSO4 + Agua, conduce electricidad porque se ioniza en el agua. Solubilidad: Es soluble en el agua solubles en agua y metanol y ligeramente solubles en alcohol y glicerina. SACAROSA (C12H22O11) Conductividad: Por ser un compuesto covalente no conduce electricidad ya que no se ionizan en el agua. Solubilidad: Sacarosa + Agua, La sacarosa se disuelve con el agua porque es un compuesto covalente polar a igual que el agua. AGUA PURA Conductividad: No conduce porque para purificarla mediante la destilacin se ha eliminado iones e impurezas. AGUA POTABLE Conductividad: Est compuesto por sales y minerales por lo que el agua potable adquiere la propiedad de conductividad. ACIDO ACETICO (CH3COOH) Conductividad: ACIDO ACETICO (CH3COOH)
el cido actico o vinagre comn (CH3-COOH) al disolverse en agua produce iones los cuales pueden conducir la electricidad, pero solo levemente.
Solubilidad:
LABORATORIO DE QUIMICA
14
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
No conduce
TETRACLORURO DE CARBONO CCl4:no conduce Conductividad: Solubilidad:
TOLUENO: No conduce Conductividad: Solubilidad:
BENCENO: no conduce Conductividad: Solubilidad:
MEZCLAS AGUA PURA + TOLUENO: NO CONDUCE
LABORATORIO DE QUIMICA
15
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
AGUA PURA + ACIDO ACETICO: SI CONDUCE
AGUA PURA + BENCENO:NO CONDUCE
LABORATORIO DE QUIMICA
16
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
BENCENO + CuSO4:NO CONDUCE
VII.COMENTARIOS
En esta oportunidad hemos tenido la experiencia de trabajar con reacciones qumicas, para poder explicar la conductividad elctrica y solubilidad de algunos reactivos debido a su enlace qumico (covalente apolar, polar y inico), pues de acuerdo a eso hemos podido aprender las funciones de cada enlace y su debida importancia.
VIII.BIBLIOGRAFIA
-QUIMICA (8va edicion) ---Whitten,Davis,Peck,Stanley -Wikipedia-Edicin 2012
LABORATORIO DE QUIMICA
17
UNIVERISIDAD NACIONAL DEL CALLAO Escuela profesional de ingeniera pesquera
LABORATORIO DE QUIMICA
18
You might also like
- Propiedades de Los ColoidesDocument2 pagesPropiedades de Los ColoidesAmayraniElizabethCanNo ratings yet
- Espontaneidad de Las Reacciones QuimicasDocument14 pagesEspontaneidad de Las Reacciones Quimicasjjlevano100% (4)
- Stequiometria de Formacion Del Oxalato de CalcioDocument8 pagesStequiometria de Formacion Del Oxalato de CalcioCesar Augusto LosadaNo ratings yet
- Reporte 2 Tabla Periodica Operaciones SimplesDocument11 pagesReporte 2 Tabla Periodica Operaciones SimplesDaniel Juarez Serrano100% (1)
- 3) Leyes de Los GasesDocument52 pages3) Leyes de Los GasesCarolina Estephanie Flores GuerraNo ratings yet
- Enlace Quimico UnmsmDocument42 pagesEnlace Quimico UnmsmWilber Milla TrujilloNo ratings yet
- Informe RedoxDocument11 pagesInforme RedoxIzander GGNo ratings yet
- INFORME-Solucion de Tiosulfato de SodioDocument8 pagesINFORME-Solucion de Tiosulfato de SodioJosé MolinaNo ratings yet
- Representación estereoquímica moléculasDocument5 pagesRepresentación estereoquímica moléculasMaria Jose RamirezNo ratings yet
- PracticaDocument16 pagesPracticaJeff VillaplanaNo ratings yet
- Practica 11Document2 pagesPractica 11Norman ZarateNo ratings yet
- InformeDocument19 pagesInformecristina rodriguezNo ratings yet
- Trancision ElectronicaDocument14 pagesTrancision ElectronicaLeonardoNo ratings yet
- Máquina de Movimiento PerpetuoDocument8 pagesMáquina de Movimiento PerpetuoMimi MuñozNo ratings yet
- Informe Final de Obtencion y Reconocimiento de Alcanos, Alquenos y AlquinosDocument7 pagesInforme Final de Obtencion y Reconocimiento de Alcanos, Alquenos y AlquinosMaría Paula SarastyNo ratings yet
- 2 Lab. Análisis Químico deDocument13 pages2 Lab. Análisis Químico dewillyballNo ratings yet
- Problemas de Trabajo y Potencia Electrica.Document3 pagesProblemas de Trabajo y Potencia Electrica.Hairo Euan MooNo ratings yet
- Informe de Laboratorio de QuímicaDocument9 pagesInforme de Laboratorio de QuímicaFranco AlexanderNo ratings yet
- AminasDocument58 pagesAminasIsrael R. TercerosNo ratings yet
- Laboratorio Conductividad EléctricaDocument9 pagesLaboratorio Conductividad Eléctricavalentina tafurNo ratings yet
- Informe N°5Document19 pagesInforme N°5SERGIO HUGO BROSSARD OBANDONo ratings yet
- 1introyanál elemtalQO23Document57 pages1introyanál elemtalQO23Frida SaldañaNo ratings yet
- Informe 6Document6 pagesInforme 6Rosalinda Quispe LuyoNo ratings yet
- Cuestionario - Grupo 14Document10 pagesCuestionario - Grupo 14Ariana NoeliaNo ratings yet
- Calibracion Multi Variable Modelo Directo Imprtante-1Document8 pagesCalibracion Multi Variable Modelo Directo Imprtante-1Emily Coromoto Gonzalez MarcanoNo ratings yet
- LUZ POLARIZADA AhuuunkesaDocument29 pagesLUZ POLARIZADA AhuuunkesaDavid GarciaNo ratings yet
- Mapa Conceptual Equilibrio Quimico AlexaDocument1 pageMapa Conceptual Equilibrio Quimico AlexaAlexis Jose Guarecuco0% (1)
- QUIMICA GENERAL REACCION NO2Document1 pageQUIMICA GENERAL REACCION NO2Junior FigueroaNo ratings yet
- Isomeria 2Document24 pagesIsomeria 2Joseph EstradaNo ratings yet
- Tema 7 - KpsDocument45 pagesTema 7 - Kpsjose contreras100% (2)
- Teoria Del Campo CristalinoDocument14 pagesTeoria Del Campo CristalinoKpnuvoNo ratings yet
- INFORME SUSTANCIAS POLARES Y NO POLARES (Listo)Document6 pagesINFORME SUSTANCIAS POLARES Y NO POLARES (Listo)9615120No ratings yet
- Informe 5Document5 pagesInforme 5TATIANA ROJAS CARONo ratings yet
- Analisis Estructural ProyectoDocument11 pagesAnalisis Estructural ProyectoFrancisco Ruiz0% (1)
- Ensayo Sobre La Composición y Clasificación de Los SuelosDocument4 pagesEnsayo Sobre La Composición y Clasificación de Los Sueloskathy100% (1)
- Numero de ReynoldsDocument17 pagesNumero de ReynoldsSusan MarquezNo ratings yet
- Importancia de los no metales en la industria y economíaDocument3 pagesImportancia de los no metales en la industria y economíaJjmvm VieyraNo ratings yet
- Citofisica Soluciones PDFDocument9 pagesCitofisica Soluciones PDFNehemias CruzNo ratings yet
- Examen Diagnostico Diagrama de Fases.Document10 pagesExamen Diagnostico Diagrama de Fases.Angel DoroteoNo ratings yet
- Informe de Plasmolisis y Turgencia 2Document39 pagesInforme de Plasmolisis y Turgencia 2Eduardo Everdeen100% (1)
- Enlaces QuimicosDocument35 pagesEnlaces QuimicosHenry Carrión Vivar100% (1)
- Problemas de RedoxDocument28 pagesProblemas de RedoxGerson Sanchez GonzalesNo ratings yet
- Sustitucion y Eliminacion E2-E1Document17 pagesSustitucion y Eliminacion E2-E1JesusNo ratings yet
- Tarea de Estereoquímica y Visualización Molecular AlumnosDocument10 pagesTarea de Estereoquímica y Visualización Molecular AlumnosYanet Gloria Condori IngaNo ratings yet
- Informe #6-Química General A1Document19 pagesInforme #6-Química General A1Jose Carlos Salgado Arimana83% (12)
- Grupos metales alcalinos reaccionesDocument11 pagesGrupos metales alcalinos reaccionesEric Enrique Pariona ChuquilinNo ratings yet
- Informe de LaboratorioDocument6 pagesInforme de LaboratoriolizpedraosNo ratings yet
- UntitledDocument7 pagesUntitledLuis Alejandro CoavasNo ratings yet
- Trabajo de Investigación Celdas Galvánicas o VoltaicasDocument9 pagesTrabajo de Investigación Celdas Galvánicas o Voltaicasjuan andres olmedo guerraNo ratings yet
- Práctica 3 - ConductimetríaDocument3 pagesPráctica 3 - ConductimetríaEsteban CortesNo ratings yet
- Factores Que Influyen en La Disolución. Propiedades Coligativas. Soluciones de Electrolitos PDFDocument1 pageFactores Que Influyen en La Disolución. Propiedades Coligativas. Soluciones de Electrolitos PDFCRISTIAN LOPEZ GUALTEROSNo ratings yet
- Practica 22Document10 pagesPractica 22Lucía Molina RamírezNo ratings yet
- ElodeaDocument6 pagesElodeaChristopher Guevara CheNo ratings yet
- Espectroscopia de Emisión de LlamaDocument5 pagesEspectroscopia de Emisión de LlamaANA CRISTINA TAMAYO PARRANo ratings yet
- Practica 7 CromatografiaDocument7 pagesPractica 7 CromatografiamaryNo ratings yet
- Proceso para la hidrogenación selectiva de acetileno a etilenoDocument13 pagesProceso para la hidrogenación selectiva de acetileno a etilenoAnonymous 1y4CXqX0% (1)
- Practica 6Document7 pagesPractica 6gil vasquez laskmi danaeNo ratings yet
- Practica 1 de QuimicaDocument8 pagesPractica 1 de QuimicaNorberto Ruiz PerezNo ratings yet
- Experiencia de Laboratorio N°14 Enlace QuimicoDocument6 pagesExperiencia de Laboratorio N°14 Enlace Quimicovanessasol2007No ratings yet
- Enlaces QuimicosDocument7 pagesEnlaces QuimicosLiliana MenaNo ratings yet
- Pasos de La Monografia de Quimica Del AguaDocument2 pagesPasos de La Monografia de Quimica Del AguaLaurita Molina CabreraNo ratings yet
- Important 1Document1 pageImportant 1Laurita Molina CabreraNo ratings yet
- Tecno 1Document9 pagesTecno 1Laurita Molina CabreraNo ratings yet
- Primera ActividaD.0Document4 pagesPrimera ActividaD.0Laurita Molina CabreraNo ratings yet
- Integrales DoblesDocument17 pagesIntegrales DoblesLaurita Molina CabreraNo ratings yet
- La Politica Que Viene. Una Lectura de GiDocument18 pagesLa Politica Que Viene. Una Lectura de GivdbvdbNo ratings yet
- Análisis de los elementos abióticos de LachayDocument10 pagesAnálisis de los elementos abióticos de LachayValeria RondónNo ratings yet
- Sales de Schüssler: Calcio, Hierro y Fósforo para tejidos y sangreDocument14 pagesSales de Schüssler: Calcio, Hierro y Fósforo para tejidos y sangreJosé de ZorNo ratings yet
- Análisis de La Película de Lutero PDFDocument3 pagesAnálisis de La Película de Lutero PDFRonyHuamaniTincoNo ratings yet
- Visita A Una BibliotecaDocument4 pagesVisita A Una BibliotecaCarolina Flores CornejoNo ratings yet
- Juegos para pasar el verano en familiaDocument61 pagesJuegos para pasar el verano en familiaUniformes AdrianaNo ratings yet
- Estudio de Un Caso de Fijación de Objetivos Anuales en Una Empresa TrasnacionalDocument15 pagesEstudio de Un Caso de Fijación de Objetivos Anuales en Una Empresa TrasnacionalUnMandoMedioNo ratings yet
- Unidad 1 - Primeros Modelos AtómicosDocument33 pagesUnidad 1 - Primeros Modelos AtómicosTotto Valdés PodestáNo ratings yet
- Sociedad TainaDocument32 pagesSociedad Tainaluz melaniaNo ratings yet
- Uso de Animales en La ExperimentaciónDocument3 pagesUso de Animales en La ExperimentaciónMelissa RomeroNo ratings yet
- Texturas y Secretos de La Imagen en Movimiento: Trabajo de Grado Dirigido PorDocument95 pagesTexturas y Secretos de La Imagen en Movimiento: Trabajo de Grado Dirigido PorSol Arias LandaNo ratings yet
- Celis - Activacion Presencia y Honestidad RadicalDocument12 pagesCelis - Activacion Presencia y Honestidad RadicalRodrigo VegaNo ratings yet
- SALARIO Emocional TrabajoDocument5 pagesSALARIO Emocional TrabajoAlejandro SuarezNo ratings yet
- Crisis de Los Estados ModernosDocument7 pagesCrisis de Los Estados ModernosAlejandro BejaranoNo ratings yet
- Evolución Del Derecho Positivo Peruano Código Civil 1852 y Tratado de Lima 1877Document5 pagesEvolución Del Derecho Positivo Peruano Código Civil 1852 y Tratado de Lima 1877raul rodolfo oregon palominoNo ratings yet
- Sistema de Informacion Web para La Gestion de Procesos Administrativos yDocument25 pagesSistema de Informacion Web para La Gestion de Procesos Administrativos yNatalie Noemi GarciaNo ratings yet
- EnsayoDocument4 pagesEnsayoSofía Edith González MontezumaNo ratings yet
- Dividendos y Reembolso de CapitalDocument78 pagesDividendos y Reembolso de CapitalLaloGarcíaNo ratings yet
- Resumen Protocolo de KiotoDocument1 pageResumen Protocolo de KiotoDenisseRamosHernndezNo ratings yet
- TIPOS DE LINEAS Dibujo Asistido Por Computadora.Document8 pagesTIPOS DE LINEAS Dibujo Asistido Por Computadora.Francisco Tonatiuh Ortiz ArroyoNo ratings yet
- Resumen Del Prólogo de El Capital de Karl MarxDocument3 pagesResumen Del Prólogo de El Capital de Karl Marxgabriel2663No ratings yet
- Los Acueductos Precolombinos de NascaDocument4 pagesLos Acueductos Precolombinos de NascaJean SantistebanNo ratings yet
- Manual Curso RedesDocument215 pagesManual Curso RedesOtro CorreoNo ratings yet
- Componentes GUI Parte IVDocument16 pagesComponentes GUI Parte IVJean Paul PereaNo ratings yet
- Guia de Pensamiento y LenguajeDocument21 pagesGuia de Pensamiento y LenguajeEmmanuel HernándezNo ratings yet
- Ensayo Conceptos Basicos de La Legislacion DocumentalDocument2 pagesEnsayo Conceptos Basicos de La Legislacion DocumentalLUCY CONSTAIN100% (1)
- Ticket Sarajevo Koper 3029428960Document1 pageTicket Sarajevo Koper 3029428960Tai Shan elva Alatrista TrampusNo ratings yet
- Balotario de Derecho Privado y Derecho Procesal Civil UNMSM-Examen Escrito de Fin de Carrera DerechoDocument33 pagesBalotario de Derecho Privado y Derecho Procesal Civil UNMSM-Examen Escrito de Fin de Carrera DerechoPamela Fiorella Bautista EncisoNo ratings yet
- Check List RodilloDocument2 pagesCheck List RodilloAngelo PuescasNo ratings yet
- Reporte: Practica 5 "Equilibrio Químico y Principio de Le-Châtelier"Document9 pagesReporte: Practica 5 "Equilibrio Químico y Principio de Le-Châtelier"RIVERA QUINTERO Victor AlejandroNo ratings yet