Professional Documents
Culture Documents
07 - Titrage PH Vinaigre
Uploaded by
Chartier JulienOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
07 - Titrage PH Vinaigre
Uploaded by
Chartier JulienCopyright:
Available Formats
TS – TP Chimie n°7 Eric DAINI – Lycée Paul Cézanne – Aix en Provence - http://labotp.
org
TITRAGE D'UN VINAIGRE
Objectifs: réaliser le titrage pH-métrique d'un vinaigre.
I TITRAGE pH-METRIQUE D'UN VINAIGRE
1) Degré d'un vinaigre
• Le vinaigre est essentiellement une solution aqueuse diluée d'acide
éthanoïque: CH3COOH.
Les concentrations commerciales de vinaigre sont exprimées en degrés.
• Le degré d'un vinaigre est égal à la masse, en gramme, d'acide
éthanoïque contenue dans 100 g de solution de vinaigre.
Par exemple un vinaigre à 6° d'acidité contient 6 g d'acide éthanoïque
Hydroxyde de sodium
pour 100 g de solution de vinaigre. CB = 0,10 mol.L-1
VBE
2) Dilution de la solution de vinaigre
• La solution de vinaigre, notée S0, étant trop concentrée, il faut la diluer 10 fois
pour obtenir une solution diluée notée S. On veut préparer 100,0 mL de Solution S
solution S. VA = 10,0 mL
CA = ??? mol.L-1
a) Quel matériel faut-il utiliser pour réaliser cette dilution ? +
phénolphtaléïne
b) Écrire le protocole expérimental.. Après accord du professeur, réaliser la dilution.
3) Titrage colorimétrique rapide de la solution diluée S
• Rincer la burette graduée avec la solution d'hydroxyde de sodium de
concentration CB = 0,10 mol.L-l . La remplir à nouveau et ajuster le zéro.
• Prélever 10,0 mL de S avec une pipette jaugée et les verser dans un bécher. Titrage Colorimétrique
• Ajouter quelques gouttes de phénolphtaléine: zone de virage [8 –10].
• Réaliser le titrage et déterminer un ordre de grandeur du volume Hydroxyde de sodium
d'hydroxyde de sodium versé à l'équivalence, noté VBE. Faire deux dosages CB = 0,10 mol.L-1
VBE
concordants.
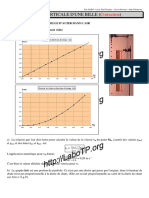
4) Titrage pH-métrique et tracé du graphe pH = f(VB)
Solution S
VA = 10,0 mL
• Etalonner le pH-mètre et rincer la sonde pH-métrique avec de l'eau distillée. CA = ?
• Remplir la burette graduée avec la solution d'hydroxyde de sodium .
• Prélever 10,0 mL de S avec une pipette jaugée et les verser dans un bécher.
• Ajouter juste assez d'eau pour que la sonde soit correctement immergée.
• Faire vérifier votre montage avant de commencer le titrage.
pH=
• Préparer une feuille de papier millimétré format A4 paysage et tracer les
axes pH et VB avec les échelles suivantes:
sur pH: 1 cm ⇔ 1 unité de pH Titrage pH-métrique
sur VB: 1 cm ⇔ 1 mL.
TS – TP Chimie n°7 Eric DAINI – Lycée Paul Cézanne – Aix en Provence - http://labotp.org
• Réaliser le titrage par suivie pH-métrique de la solution S, en ajoutant la solution d'hydroxyde de sodium
d'abord mL par mL, puis en rapprochant les volumes VB versés par pas de 0,5 mL puis de 0,2 mL lorsque VB
est compris approximativement dans l'intervalle [VBE – 3; VBE + 3].
Après chaque ajout, positionner directement le point sur le graphe sans faire de tableau.
• Continuer les ajouts jusqu'à VB = 20,0 mL.
II EXPLOITATION DES RESULTATS
1) Déterminer les coordonnées (VBE, pHE) du point équivalent du titrage en utilisant la méthode des tangentes.
Faire apparaître les tracés.
2) Ecrire les couples acide / base mis en jeu dans le titrage et en déduire l'équation de la réaction de titrage.
3) Exprimer puis calculer la constante d'équilibre K de la réaction de titrage. La réaction est-elle totale ?
Justifier.
Données: à 25°C pKE = 14 - pKA associée au couple de l'acide éthanoïque : pKA = 4,8
4) Définir l'équivalence du titrage et en déduire une relation entre les quantités des réactifs mises en jeu.
5) Calculer la concentration molaire CS de la solution S.
6) En déduire la concentration C0 de la solution S0 du vinaigre.
7) La masse volumique du vinaigre est: µ vinaigre = 1,0 × 103 g.L-1 . Calculer le volume Vvin occupé par 100 g de
vinaigre. En déduire la quantité n0 d'acide éthanoïque contenue dans 100 g de la solution S0 de vinaigre.
8) Calculer la masse m0 d'acide éthanoïque contenue dans 100 g de la solution S0 de vinaigre.
9) En déduire le degré d'acidité du vinaigre et comparer avec la valeur indiquée par le fabricant. Écart relatif.
10) L'ajout d'eau distillée modifie-t-il le volume VBE de base versée à l'équivalence ? Pourquoi ?
11) La phénolphtaléïne (zone de virage [8 –10]) était-il un indicateur coloré adapté au titrage colorimétrique ?
Pourquoi ?
Données: M(C) = 12 g.mol-1 - M(O) = 16 g.mol-1 - M(H) = 1,0 g.mol-1.
TS – TP Chimie n°7 Eric DAINI – Lycée Paul Cézanne – Aix en Provence - http://labotp.org
TITRAGE D'UN VINAIGRE
• paillasse élève:
2 burettes graduées 25 mL
2 pipettes jaugées de 10,0 mL + propipette
1 fiole jaugée de 100,0 mL
2 petits béchers 50 mL
1 agitateur magnétique avec aimant
2 pots en verre pour les solutions
1 verre à pied poubelle
pH-mètre + solution d'étalonnage
Solution d'hydroxyde de sodium à 0,10 mol.L-1
Pissette d'eau distillée
Phénolphtaléine
• paillasse prof
Solution de vinaigre à 6° et 8°.
Réserves solutions et matériels
You might also like
- Chromatographie: Les Grands Articles d'UniversalisFrom EverandChromatographie: Les Grands Articles d'UniversalisNo ratings yet
- 07 - Titrage Colorimetrique DeboucheurDocument2 pages07 - Titrage Colorimetrique DeboucheurChartier JulienNo ratings yet
- 07 - Titrage Colorimetrique Deboucheur CorDocument2 pages07 - Titrage Colorimetrique Deboucheur CorChartier JulienNo ratings yet
- Gee L1gi Zenasni TPDocument65 pagesGee L1gi Zenasni TPSoumia SalhiNo ratings yet
- 04 Charge Condensateur CorrectionDocument4 pages04 Charge Condensateur CorrectionChartier Julien100% (1)
- 07 Titrage PH Vinaigre CorrectionDocument4 pages07 Titrage PH Vinaigre CorrectionChartier Julien86% (7)
- Titrage Du Vinaigre CorrectionDocument4 pagesTitrage Du Vinaigre CorrectionOstensible50% (2)
- 08 Loi Newton CorrectionDocument4 pages08 Loi Newton CorrectionChartier JulienNo ratings yet
- TP4 Analytique 3émé AnnéeDocument14 pagesTP4 Analytique 3émé AnnéeLïnâ ExØtîc DõlĽNo ratings yet
- Qualité de L'eauDocument59 pagesQualité de L'eauabderrahimn100% (2)
- Chimie TP9 Titrage Conduc VinaigreDocument2 pagesChimie TP9 Titrage Conduc VinaigreMarius MissiNo ratings yet
- 07 Titrage PH VinaigreDocument3 pages07 Titrage PH Vinaigrenabil douadiNo ratings yet
- 11 Pendule Simple CorrectionDocument2 pages11 Pendule Simple CorrectionChartier Julien87% (23)
- BPT Sciences-Industrielles-B 2008 TSIDocument23 pagesBPT Sciences-Industrielles-B 2008 TSISouhaib LoudaNo ratings yet
- 12 Pendule Elastique CorrectionDocument2 pages12 Pendule Elastique CorrectionChartier Julien90% (10)
- 11 Ester CorrectionDocument7 pages11 Ester CorrectionChartier Julien100% (2)
- TP Chimie N°7 Dosage OxydoreductionDocument1 pageTP Chimie N°7 Dosage OxydoreductionSerge.Omisos367767% (3)
- 07 RLC CorrectionDocument5 pages07 RLC CorrectionChartier JulienNo ratings yet
- TP2 de ChimieDocument2 pagesTP2 de Chimiemohammed el amineNo ratings yet
- C71 - TP 2 Chimie Minerale Reactions de Complexation: RougeDocument7 pagesC71 - TP 2 Chimie Minerale Reactions de Complexation: RougeMarck CadiilNo ratings yet
- 09 Chute CorrectionDocument3 pages09 Chute CorrectionChartier Julien100% (3)
- Chimie-TP6 Dosage D'un Produit CommercialDocument3 pagesChimie-TP6 Dosage D'un Produit CommercialChartier JulienNo ratings yet
- TP Dosage PhmetriqueDocument1 pageTP Dosage PhmetriqueNesrine BouzidNo ratings yet
- 04 PH Tau CorrectionDocument4 pages04 PH Tau CorrectionChartier JulienNo ratings yet
- Dosage de L'acide Citrique Dans Un Détartrant Commercial (Corrigé)Document4 pagesDosage de L'acide Citrique Dans Un Détartrant Commercial (Corrigé)theobromine100% (5)
- 06 BBT CorrectionDocument4 pages06 BBT CorrectionChartier JulienNo ratings yet
- 03 Suivi Spectro CorDocument5 pages03 Suivi Spectro CorChartier JulienNo ratings yet
- 01 Transf Dos CorDocument5 pages01 Transf Dos CorChartier JulienNo ratings yet
- TP ch4 Titrage PhmetriqueDocument2 pagesTP ch4 Titrage PhmetriquebounegabNo ratings yet
- Titrage VinaigreDocument2 pagesTitrage VinaigreDjahid Jo100% (2)
- Chimie-TP4 Determination de Qr-CorrDocument3 pagesChimie-TP4 Determination de Qr-CorrChartier Julien100% (1)
- Rapport Acide BaseDocument10 pagesRapport Acide BaseBouafia AbdelrahmaneNo ratings yet
- TP ConductimetrieDocument5 pagesTP ConductimetriePedro Assassi100% (1)
- Chimie TP2 Dosage CorrDocument3 pagesChimie TP2 Dosage CorrChartier JulienNo ratings yet
- C03 Cinetique ReactionDocument2 pagesC03 Cinetique ReactionmohNo ratings yet
- Chimie B Chap8 Titrage AcidobasiqueDocument6 pagesChimie B Chap8 Titrage AcidobasiqueSamantha Farah100% (1)
- P2016 CM11 TP FasciculeDocument44 pagesP2016 CM11 TP FasciculeRochdi BAATINo ratings yet
- PS CMM b3 TP Dosage Du Diiode Dans La BetadineDocument7 pagesPS CMM b3 TP Dosage Du Diiode Dans La BetadinemranonimosNo ratings yet
- TP ÉlectroDocument18 pagesTP ÉlectroBichou HomNo ratings yet
- TitrageDocument3 pagesTitrageelhijaziyoussefNo ratings yet
- TP SM24 2011-2012Document35 pagesTP SM24 2011-2012HichamLahbilNo ratings yet
- Spe - Methode de MohrDocument4 pagesSpe - Methode de MohrAbdou aziz fallNo ratings yet
- TS Spe Chimie TP 8 Dosage Ions Chlorures Par La Methode de Mohr EleveDocument2 pagesTS Spe Chimie TP 8 Dosage Ions Chlorures Par La Methode de Mohr Elevechabi khaoulaNo ratings yet
- TP N°2 ChimieDocument5 pagesTP N°2 ChimieDenilson Josemir100% (1)
- Mode Opératoire SpectroDocument2 pagesMode Opératoire SpectroMushy Sõft Thiñg100% (2)
- Cinetique ConductimetrieDocument10 pagesCinetique ConductimetrieMouad Arrad100% (1)
- Rhaoui AbdoDocument9 pagesRhaoui AbdoAli BoutaharNo ratings yet
- TP Chimie Eau PDFDocument15 pagesTP Chimie Eau PDFAysan OgluNo ratings yet
- S - Rie TD Chimie1Document12 pagesS - Rie TD Chimie1Aristide MfifenNo ratings yet
- tp05 Maiver 2Document14 pagestp05 Maiver 2kmeriemNo ratings yet
- 10 6 TP Dosage de La BétadineDocument3 pages10 6 TP Dosage de La BétadinemranonimosNo ratings yet
- Compte Rendu 1Document11 pagesCompte Rendu 1hadil100% (1)
- TP Dosage PH MétriqueDocument2 pagesTP Dosage PH MétriqueAbidine CHAHIR100% (2)
- Compte Rendu AspirineDocument5 pagesCompte Rendu AspirineMer IemNo ratings yet
- AspirineDocument3 pagesAspirinemariem outahmiditNo ratings yet
- Manipulation 355Document7 pagesManipulation 355oulahnoud boubakerNo ratings yet
- Préparation de SolutionsDocument8 pagesPréparation de Solutionsbessama84No ratings yet
- TS TPC13Document3 pagesTS TPC13Prince AbdooNo ratings yet
- TP PH Metre ATHIR - New1Document8 pagesTP PH Metre ATHIR - New1samibenhabileNo ratings yet
- TP 5 STDocument2 pagesTP 5 STABDelpari SeraicheNo ratings yet
- TP Chimie n1Document2 pagesTP Chimie n1Oussoufi Mze Kaanbi100% (2)
- CocaDocument5 pagesCocatheobromine100% (4)
- Applications de la spectrophotomérie en phytochimie: sciencesFrom EverandApplications de la spectrophotomérie en phytochimie: sciencesNo ratings yet
- Null 231221 095942Document2 pagesNull 231221 095942zeinabhatemtarchichiNo ratings yet
- TD Acide Fort Base Forte Dosage TS2Document10 pagesTD Acide Fort Base Forte Dosage TS2pathediakhate4No ratings yet
- Rapport Degre D'aciditeDocument5 pagesRapport Degre D'aciditezeinabhatemtarchichiNo ratings yet
- tp8 Dosage Phmetrique PDFDocument2 pagestp8 Dosage Phmetrique PDFMokhtarBensaidNo ratings yet
- Chimie-TP4 Determination de Qr-CorrDocument3 pagesChimie-TP4 Determination de Qr-CorrChartier Julien100% (1)
- Chimie-TP5 Suivi Phmetrique de L'acide Ethanoique Par La SoudeDocument2 pagesChimie-TP5 Suivi Phmetrique de L'acide Ethanoique Par La SoudeChartier Julien100% (1)
- Chimie-TP4 Determination de QRDocument2 pagesChimie-TP4 Determination de QRChartier JulienNo ratings yet
- Chimie-TP3 Mesure Du PH de SolutionsDocument2 pagesChimie-TP3 Mesure Du PH de SolutionsChartier JulienNo ratings yet
- 13 Etude Dynamique Energetique Ressort CorDocument7 pages13 Etude Dynamique Energetique Ressort CorChartier JulienNo ratings yet
- Chimie TP1 Facteurs Cinetiques CorrDocument1 pageChimie TP1 Facteurs Cinetiques CorrChartier Julien100% (1)
- Chimie TP2 Dosage CorrDocument3 pagesChimie TP2 Dosage CorrChartier JulienNo ratings yet
- Chimie-TP3 Mesure Du PH de Solutions-CorrDocument2 pagesChimie-TP3 Mesure Du PH de Solutions-CorrChartier JulienNo ratings yet
- 14 RadioactivitéDocument2 pages14 RadioactivitéChartier Julien100% (1)
- Chimie-TP1 Facteurs CinetiquesDocument1 pageChimie-TP1 Facteurs CinetiquesChartier JulienNo ratings yet
- 12 Pendule ElastiqueDocument2 pages12 Pendule ElastiqueChartier JulienNo ratings yet
- 10 EulerDocument3 pages10 EulerChartier JulienNo ratings yet
- 11 Pendule SimpleDocument2 pages11 Pendule SimpleChartier Julien100% (5)
- 10 Euler CorrectionDocument5 pages10 Euler CorrectionChartier JulienNo ratings yet
- 05 RC CorrectionDocument5 pages05 RC CorrectionChartier JulienNo ratings yet
- 08 Loi NewtonDocument4 pages08 Loi NewtonChartier JulienNo ratings yet
- 09 ChuteDocument4 pages09 ChuteChartier Julien100% (2)
- 06 RLDocument4 pages06 RLChartier JulienNo ratings yet
- 04 Charge CondensateurDocument4 pages04 Charge CondensateurChartier JulienNo ratings yet
- 06 RL CorrectionDocument6 pages06 RL CorrectionChartier JulienNo ratings yet
- 07 RLCDocument5 pages07 RLCChartier JulienNo ratings yet
- 03 Ondes Lunmineuses CorrectionDocument2 pages03 Ondes Lunmineuses CorrectionChartier JulienNo ratings yet
- 04 Charge CondensateurDocument4 pages04 Charge CondensateurChartier JulienNo ratings yet
- Extrait 42337210Document135 pagesExtrait 42337210Souley Hega Harouna DialloNo ratings yet
- TP Benamara WDocument3 pagesTP Benamara Wabir ben100% (1)
- Compte Rendu SDMDocument5 pagesCompte Rendu SDMMustapha MoussaouiNo ratings yet
- Aromatique S 1Document20 pagesAromatique S 1Faculté De Médecine BécharNo ratings yet
- Bts Chimiste GC 2015Document11 pagesBts Chimiste GC 2015ben yahya ezzeddineNo ratings yet
- Corrosion PpsDocument18 pagesCorrosion Ppsayoub garnateNo ratings yet
- Physique Chimie Tsi Exemple 2017Document9 pagesPhysique Chimie Tsi Exemple 2017ZH hasnaeNo ratings yet
- L'Alchimie SimplifiéeDocument15 pagesL'Alchimie Simplifiéeyves.mpNo ratings yet
- L'élimination de Méthyle Orange Par Adsorption Sur L'argile NaturalDocument65 pagesL'élimination de Méthyle Orange Par Adsorption Sur L'argile NaturalMeriem RosigeNo ratings yet
- TPE Sur Le Blanchiments Des Fibres Cellulosique Nkomo Et PELAGODocument9 pagesTPE Sur Le Blanchiments Des Fibres Cellulosique Nkomo Et PELAGOleprinceeustacheadaNo ratings yet
- Atg 1 Introduction ..... Appareillage Atg Courbe Simple 2018 2019Document33 pagesAtg 1 Introduction ..... Appareillage Atg Courbe Simple 2018 2019fouad alimdar100% (1)
- 1re S Chimie - TP 10 - Caractristaion Des Groupements FonctionnelsDocument1 page1re S Chimie - TP 10 - Caractristaion Des Groupements Fonctionnelsla physique selon le programme Français100% (1)
- Corrige Exercices 14 21 Chimie OrganiqueDocument33 pagesCorrige Exercices 14 21 Chimie OrganiqueFofo BokovouNo ratings yet
- 665 5-065 PDFDocument85 pages665 5-065 PDFSamir MazafranNo ratings yet
- Epreuve Bac 2022 Chimie Série C D e Cameroun PDFDocument2 pagesEpreuve Bac 2022 Chimie Série C D e Cameroun PDFAmza Farel100% (2)
- Liaison CovalenteDocument17 pagesLiaison CovalenteHaytem bossNo ratings yet
- Ds06 Acide Base Stereochimie CorrigeDocument2 pagesDs06 Acide Base Stereochimie CorrigeAya BenhadiyaNo ratings yet
- Solutes Hydrophobes Cabane01Document11 pagesSolutes Hydrophobes Cabane01taoufik akabliNo ratings yet
- Cours Premiere ADocument27 pagesCours Premiere Atoto TOTOROTONo ratings yet
- Les Sols de Moyenne Sénégal: La DuDocument12 pagesLes Sols de Moyenne Sénégal: La DuPape SeckNo ratings yet
- Cours 3 Les SteroidesDocument23 pagesCours 3 Les SteroidesSARAHNo ratings yet
- Cours Géotech CNAS ParisDocument362 pagesCours Géotech CNAS ParisObaidaAiche0% (1)
- Resumé VerreDocument1 pageResumé VerreBoudali AbdelkaderNo ratings yet
- Exercices Alcools-ThiolsDocument10 pagesExercices Alcools-ThiolsJean-François Abena100% (2)
- Qualite Eau Du Robinet Def Cle444f4cDocument14 pagesQualite Eau Du Robinet Def Cle444f4cMamadou fayeNo ratings yet
- Iec61198 (Ed1 0) B ImgDocument33 pagesIec61198 (Ed1 0) B Imganjes1No ratings yet
- 2015 Chimie RABATDocument1 page2015 Chimie RABATKarimBenANo ratings yet
- A Quoi Sert Le Phosphore Pour Les PlantesDocument2 pagesA Quoi Sert Le Phosphore Pour Les Planteslatifa hajjoubiNo ratings yet
- 4.chapitre 3 - ATDDocument21 pages4.chapitre 3 - ATDachouak hettalNo ratings yet