Professional Documents
Culture Documents
Química lista exercícios fixação AV02
Uploaded by
Natalia AmaralOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Química lista exercícios fixação AV02
Uploaded by
Natalia AmaralCopyright:
Available Formats
Srie / turma:
_2____
Aluno(a): Professor: Arnoldo Silva Disciplina: Qumica Data: _____/ _____/ 2013 Ensino Mdio
Lista de Exerccio de Fixao para AV02 3 Bim.
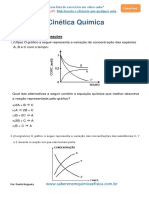
1. Sobre catalisadores, so feitas as quatro afirmaes seguintes. I - So substncias que aumentam a velocidade de uma reao. II - Reduzem a energia de ativao da reao. III - As reaes nas quais atuam no ocorreriam nas suas ausncias. IV - Enzimas so catalisadores biolgicos. Dentre estas afirmaes, esto corretas, apenas: a) I e II. d) I, II e IV. b) II e III. e) II, III e IV. c) I, II e III. 2. A elevao de temperatura aumenta a velocidade das reaes qumicas porque aumenta os fatores apresentados nas alternativas, EXCETO: a) A energia cintica mdia das molculas. b) A energia de ativao. c) A frequncia das colises efetivas. d) O nmero de colises por segundo entre as molculas. e) A velocidade mdia das molculas. 3. Responder questo com base no esquema a seguir, que representa situaes em comprimidos anticidos efervescentes de mesma constituio reagem em presena de gua. durante 30 segundos, as bolhas de gs formadas imediatamente aps os reagentes serem misturados. Em cada experimento, usou-se o mesmo volume de uma mesma soluo de HCl e a mesma massa de ferro, variando-se a forma de apresentao da amostra de ferro e a temperatura. O quadro indica as condies em que cada experimento foi realizado: experimento ferro temperatura I prego 40 C II prego 20 C III palhinha de ao 40 C Assinale a alternativa que apresenta os experimentos na ordem crescente do nmero de bolhas observado: a) II, I, III. d) II, III, I. b) III, II, I. e) I, III, II. c) I, II, III. 5. Analise as afirmativas abaixo. I. A energia de ativao de uma reao qumica aumenta com o aumento da temperatura do sistema reacional. II. A velocidade de uma reao qumica determinada pela etapa mais lenta. III. A variao de entalpia de uma reao independe do uso de catalisadores. IV. Todas as colises entre as molculas de um reagente so efetivas, excetuando-se quando os reagentes so lquidos e em temperaturas baixas. Assinale a alternativa que contempla as afirmativas corretas. a) I, II e IV, apenas. d) II e III, apenas. b) II, III e IV, apenas. e) I e III, apenas. c) I, III e IV, apenas. 6. O esquema mostra observaes feitas por um aluno, quando uma chapa de alumnio foi colocada em um tubo de ensaio, contendo soluo aquosa de HCl.
Pelo exame do esquema, pode-se afirmar que as reaes que ocorrem em menor tempo do que a do frasco I, so as dos frascos: a) II e III. d) III e IV. b) II e IV. e) III e V. c) II e V. 4. Trs experimentos foram realizados para investigar a velocidade da reao entre HCl aquoso diludo e ferro metlico. Para isso, foram contadas,
CO(g) + O2(g) CO2(g) Esses catalisadores atuam no sentido de: a) aumentar a energia de ativao da reao. b) reduzir a velocidade da reao. c) inibir a reao do CO com o oxignio do ar. d) reduzir a energia de ativao da reao. e) alterar a espontaneidade da reao. 10. Se a velocidade de uma reao a 20 C x mol/min, o valor da nova velocidade (mol/min) se aumentarmos a temperatura de 30 C, (regra de Van't Hoff), ser de: a) 2x d) 16x b) 4x e) 32x c) 8x 11. Considere as duas fogueiras representadas a seguir, feitas, lado a lado, com o mesmo tipo e quantidade de lenha.
Nessa experincia, ocorre o desprendimento de um gs e a formao de um sal. A respeito dela correto afirmar que: a) a frio, a reao forte e processa-se instantaneamente. b) o sal formado insolvel. c) o gs formado o oxignio. d) a reao acelerada quando o sistema aquecido. e) a velocidade da reao no se altera com o aumento de temperatura. 7. Uma reao qumica processa-se conforme o grfico abaixo.
incorreto afirmar que: a) a passagem I endotrmica. b) a passagem II envolve a menor energia de ativao. c) a passagem III a mais lenta. d) III libera mais calor do que II. e) a reao se processa em etapas. 8. Pesquisadores do Instituto Max Planck, na Alemanha conseguiram ativar o CO2 para uso em uma reao qumica. Este procedimento um primeiro passo para um sonho antigo do homem: realizar a fotossntese artificial. Para isto, os pesquisadores se utilizaram de um catalisador sem metal. Neste sentido, qual o papel de um catalisador em uma reao qumica? a) Diminuir as energias de reagentes e produtos. b) Encontrar um novo caminho reacional com uma menor energia de ativao. c) Ser consumido durante a reao, propiciando uma maior quantidade de reagente. d) Eliminar completamente a energia de ativao. e) Inibir os choques efetivos de reagentes e produtos. 9. Para reduzir o efeito do CO emitido atravs do escapamento dos carros, usam-se catalisadores adequados, que transformam o CO em CO2, reduzindo o efeito de poluio, de acordo com a equao:
A rapidez da combusto da lenha ser a) maior na fogueira 1, pois a superfcie de contato com o ar maior. b) maior na fogueira 1, pois a lenha est mais compactada, o que evita a vaporizao de componentes volteis. c) igual nas duas fogueiras, uma vez que a quantidade de lenha a mesma e esto no mesmo ambiente. d) maior na fogueira 2, pois a lenha est menos compactada, o que permite maior reteno de calor pela madeira. e) maior na fogueira 2, pois a superfcie de contato com o ar maior. 12. Voc est cozinhando batata e fazendo carne grelhada, tudo em fogo baixo, num fogo a gs. Se voc passar as duas bocas do fogo para fogo alto, o que acontecer com o tempo de preparo? a) Diminuir para os dois alimentos. b) Diminuir para a carne e aumentar para as batatas. c) No ser afetado. d) Diminuir para as batatas e no ser alterado para a carne. e) Diminuir para a carne e permanecer o mesmo para as batatas.
13. No estudo da cintica da reao 2NO + 2H2 N2 + 2H2O, temperatura de 700C, foram obtidos os seguintes dados, de acordo com a tabela abaixo: [H2] 1x103 2x103 2x103 [NO] 1x103 1x103 2x103 Velocidade inicial 3x105 6x105 24x105
16. Um dos objetivos do catalisador no sistema de descarga de um automvel o de converter os xidos de nitrognio em molculas menos danosas ao ambiente. 2NO(g) N2(g) + O2 (g) A funo do catalisador na reao a de: a) fortalecer as ligaes no reagente. b) impedir a formao do produto. c) diminuir a velocidade de decomposio do NO(g). d) diminuir a energia cintica da reao. e) diminuir a energia de ativao da reao. 17. A figura mostra o perfil reacional da decomposio de um composto X por dois caminhos reacionais diferentes, I e II. Baseado nas informaes apresentadas nessa figura, assinale a opo ERRADA.
catalisador
Analisando os resultados, correto afirmar que a lei da velocidade para essa reao : a) v = k[H2][NO]2. d) v = k[H2]2[NO]2. b) v = k[H2][NO]. e) v = k[NO]2. c) v = k[H2]2. 14. Uma reao que pode ocorrer no ar poludo : NO2(g) + O3(g) NO3(g) + O2(g), trs experimentos foram realizados a 25C, para estudar a cintica dessa reao: [NO2] inicial 5,0x105 5,0x105 2,5x105 [O3] inicial 1,0x105 2,0x105 2,0x105 Velocida de inicial (mol/L.s) 2,2x105 4,4x105 2,2x105
Experimento 1 2 3
Utilizando os dados experimentais da tabela acima, determine a expresso da lei da velocidade, a ordem da reao e o valor da constante de velocidade, respectivamente. a) v = k [O3]; ordem = 1 e k = 2,2 x107 s1. b) v = k [NO2]; ordem = 1 e k = 4,4 x107 s1. c) v = k [NO2]; ordem = 2 e k = 2,2 x 10107 s1. d) v = k [NO2][O3]; ordem = 2 e k = 4,4 x107 s1. e) v = k [NO2] + [O3]; ordem = 2 e k = 4,4x107 s1. 15. Considere o seguinte mecanismo de reao genrica: A4+ + B2+ A4+ + B3+ C+ + B4+ A3+ + B3+ (etapa lenta) A3+ + B4+ (etapa rpida) C3+ + B2+ (etapa rpida)
a) O caminho reacional II envolve duas etapas. b) A quantidade de energia liberada pelo caminho reacional I igual do caminho reacional II. c) O composto K um intermedirio no processo reacional pelo caminho II. d) O caminho reacional I mostra que a decomposio de X de primeira ordem. e) O caminho reacional II refere-se reao catalisada. 18. A sntese de HI um processo exotrmico que, no equilbrio, pode ser representado pela equao: H2(g) + I2(g) 2HI(g) Com relao a esse processo, CORRETO afirmar que: a) quando abaixarmos a temperatura, o equilbrio deslocado para a direita. b) quando adicionarmos uma pequena quantidade de hidrognio, o equilbrio deslocado para a esquerda. c) quando retirarmos uma parte do iodo, o equilbrio deslocado para a direita. d) quando adicionarmos um catalisador, o equilbrio deslocado para a direita.
Com relao a este mecanismo, assinale a opo ERRADA. a) A reao global representada pela equao: C+ + 2 A4+ C3+ + 2 A 3+. 2+ b) B catalisador. c) B3+ e B4+ so intermedirios da reao. d) A lei de velocidade descrita pela equao v = k[C+][A4+]. e) A reao de segunda ordem.
19. O monxido de carbono um gs incolor, sem cheiro e muito reativo. Ele reage, por exemplo, com o gs oxignio formando o dixido de carbono, de acordo com a equao qumica a seguir. 2CO(g) + O2(g) 2CO2(g) Experimentalmente observam-se as informaes que esto no quadro a seguir. [CO] [O2] (mol.L1) (mol.L1) 0,04 0,04 0,08 0,04 0,04 0,08 Velocidade inicial (mol.L1.min1) 7,36 x 105 2,94 x 104 1,47 x 104
22. Um comprimido efervescente de vitamina C intacto, pesando 5 g, quando colocado em um copo contendo gua a 25 C, ser dissolvido em dois minutos. Considerando essa informao, assinale verdadeira (V) ou falsa (F) em cada uma das proposies. ( ) Se o comprimido efervescente estiver em pequenos pedaos, o tempo de dissoluo tambm ser de dois minutos, pois a massa continua sendo 5 g. ( ) O tempo de dissoluo do comprimido efervescente intacto mantm-se quando o comprimido for dissolvido em gua a 40 C, pois a rea de contato a mesma. ( ) Quanto maior a superfcie de contato do comprimido efervescente com a gua, maior o nmero de colises favorveis, portanto maior a velocidade de dissoluo. ( ) O aumento da temperatura diminui a energia de ativao, diminuindo, portanto, o tempo de dissoluo. A sequncia correta a) V - F - V - V. d) F - F - V - F. b) F - V - F - V. e) V - V - F - F. c) V - V - F - V. 23. Uma reao qumica atinge o equilbrio qumico quando: a) ocorre simultaneamente nos sentidos direto e inverso. b) as velocidades das reaes direta e inversa so iguais. c) os reagentes so totalmente consumidos. d) a temperatura do sistema igual do ambiente. e) a razo entre as concentraes de reagentes e produtos unitria. 24. A aplicao do princpio de Le Chatelier possibilita o controle da direo e da extenso de uma determinada reao qumica. Um exemplo tpico o equilbrio entre as formas cor de rosa e azul dos ons cobalto.
[Co(H2O)]2+(aq) + 4Cl(aq)
Considerando a equao qumica e os dados do quadro, assinale a alternativa correta. a) Para a lei de velocidade, a expresso para esta reao v = k[CO2]2. b) Conforme aumenta a concentrao do produto, aumenta a velocidade da reao. c) Esta uma reao de ordem zero com relao ao CO2 e de segunda ordem quanto reao global. d) A velocidade de formao do CO2 nesta reao independente da concentrao de O2. e) O valor da constante de velocidade para esta reao 1,15 L2.mol2.min1. 20. Do equilbrio C(s) + CO2(g) 2CO(g), H=174kJ/mol de carbono, INCORRETO afirmar que: a) kp = (pCO)2 / (pCO2) b) a velocidade da reao direta (V1) igual velocidade da reao inversa (V2). c) a adio de catalisador no altera o equilbrio. d) um aumento da presso total favorece a formao do monxido de carbono. e) a diminuio da temperatura desfavorece a formao do monxido de carbono. 21. Um dos objetivos do catalisador no sistema de descarga de um automvel o de converter os xidos de nitrognio em molculas menos danosas ao ambiente. 2NO(g) N2(g) + O2 (g) A funo do catalisador na reao a de: a) fortalecer as ligaes no reagente. b) impedir a formao do produto. c) diminuir a velocidade de decomposio do NO(g). d) diminuir a energia cintica da reao. e) diminuir a energia de ativao da reao.
catalisador
cor de rosa
[CoCl4]2+(aq) + 6H2O(l); azul H= +120cal/mol
Assinale a alternativa que apresenta uma ao sobre o sistema, que favorece a formao da soluo de cor azul. a) Diminuio da concentrao de Cl. b) Diminuio da temperatura. c) Diluio da soluo. d) Aumento da concentrao de gua. e) Adio de cloreto de sdio aquoso.
25. Considere o diagrama de energia para uma dada reao qumica.
28. O grfico a seguir representa a evoluo de um sistema em que uma reao reversvel ocorre at atingir o equilbrio.
Leia com ateno as seguintes armativas: I. A reao endotrmica. II. O H da reao dado por X. III. A energia de ativao sem catalisador dada por Y. IV. O abaixamento da energia de ativao, vericado pela adio de um catalisador, dado por Z. So corretas somente as armativas: a) I, III e IV. d) I e II. b) I, II e III. e) II e IV. c) II, III e IV. 26. Na reao de dissociao trmica do HI(g), a velocidade de reao proporcional ao quadrado da concentrao molar do HI. Se triplicarmos a concentrao do HI, a velocidade da reao: a) aumentar 6 vezes. b) aumentar 9 vezes. c) diminuir 6 vezes. d) diminuir 9 vezes. e) diminuir 3 vezes 27. Os seguintes grficos representam variveis de uma reao qumica:
Sobre o ponto t1, neste grfico, pode-se afirmar que indica: a) uma situao anterior ao equilbrio, pois as velocidades das reaes direta e inversa so iguais. b) um instante no qual o sistema j alcanou equilbrio. c) uma situao na qual as concentraes de reagentes e produtos so necessariamente iguais. d) uma situao anterior ao equilbrio, pois a velocidade da reao direta est diminuindo e a velocidade da reao inversa est aumentando. e) um instante no qual o produto das concentraes dos reagentes igual ao produto das concentraes dos produtos. 29. Caso, ao equilbrio abaixo, seja adicionado uma soluo de NaOH, NH4+(aq.) + OH1(aq.) NH3(g) + H2O(lq.)
a) a quantidade de amnia liberada aumenta. b) a concentrao do on amnio aumenta. c) o pH da soluo em equilbrio diminui. d) no h qualquer alterao. e) a quantidade de amnia liberada diminui. 30. Considere a seguinte reao: 2 SO2(g) + O2(g) 2 SO3(g) + 23,5 kcal
Os grficos indicam: a) No instante t1, a velocidade da reao direta igual da inversa. b) Aps t2, no ocorre reao. c) No instante t1, a reao atingiu o equilbrio. d) A curva 4 corresponde velocidade da reao inversa. e) No ponto de interseco das curvas 3 e 4, a concentrao de produtos igual de reagentes.
Para que o equilbrio possa ser deslocado para a direita poderemos: I. Aumentar a presso II. Aumentar a temperatura III. Aumentar a concentrao de SO2(g) IV. Diminuir a presso V. Diminuir a temperatura Esto corretas as afirmaes: a) I, III e V. d) III, IV e V. b) I, II e III. e) I, IV e V. c) II, III e IV.
31. Estudou-se a cintica da reao: S(s) + O2(g) SO2(g), realizada a partir de enxofre e oxignio em um sistema fechado. Assim, as curvas I, II e III do grfico abaixo representam as variaes das concentraes dos componentes com o tempo, desde o momento da mistura at o sistema atingir o equilbrio.
33. Em um recipiente de volume V ocorre a seguinte reao de equilbrio em fase gasosa: 1A + 1B 2C. No incio, so colocados 6,5 mols de cada reagente e aps atingido o equilbrio, restaram 1,5 mols de cada reagente. A constante de equilbrio (Kc) igual a: a) 45 V d) 44,4 b) 22,2 V e) 22,2 V 2 c) 44,4 V 34. Num copo, estabelece-se o seguinte equilbrio heterogneo: Ag+(aq) + Cl(aq) AgCl(s) Com relao possibilidade de se deslocar este equilbrio para a direita, mantendo-se a temperatura constante, so feitas as seguintes sugestes: I. acrescentar AgCl(s); II. retirar uma parte do AgCl(s); III. acrescentar um pouco de NaCl(s); IV. acrescentar gua; V. evaporar parte da gua; Das sugestes acima, ir (iro) deslocar, efetivamente, o equilbrio no sentido desejado apenas: a) III. d) III e V. b) I e IV. e) II, III e V. c) II e III. 35. Atingido o equilbrio qumico na reao: H2(g) + I2(g) 2 HI(g) medimos os valores das constantes de equilbrio, em funo das concentraes molares (Kc) e em funo das presses parciais (Kp). Em conseqncia, teremos: a) sempre Kc = Kp; b) sempre Kc > Kp; c) sempre Kc < Kp; d) Kc Kp, dependendo da temperatura; e) Kc Kp, dependendo da temperatura.
As variaes das concentraes de S, de O2 e de SO2 so representadas, respectivamente, pelas curvas: a) I, II e III d) I, III e II b) II, III e I e) III, II e I c) III, I e II 32. A transformao de um composto A em um composto B, at se atingir o equilbrio (A S B), foi estudada em trs experimentos. De um experimento para o outro, variou-se a concentrao inicial do reagente A ou a temperatura ou ambas. Registraram-se as concentraes de reagente e produto em funo do tempo.
Com esses dados, afirma-se: I. Os experimentos 1 e 2 foram realizados mesma temperatura, pois as constantes de equilbrio correspondentes so iguais. II. O experimento 3 foi realizado numa temperatura mais elevada que o experimento 1, pois no experimento 3 o equilbrio foi atingido em um tempo menor. III. A reao endotrmica no sentido da formao do produto B. Dessas afirmaes: a) todas so corretas. b) apenas I e III so corretas. c) apenas II e III so corretas. d) apenas I correta. e) apenas II correta.
O estudo transforma as boas intenes em bons resultados Bom Estudo!
You might also like
- Ficha Individual de Acompanhamento Periódico Do AlunoDocument1 pageFicha Individual de Acompanhamento Periódico Do AlunoETI LUIZ RODRIGUES ETI100% (6)
- ANEXO III - Procedimento Solda CVSDocument8 pagesANEXO III - Procedimento Solda CVSEduardo OliveiraNo ratings yet
- Cinetica Quimica UniDocument6 pagesCinetica Quimica UnicarlostucupiNo ratings yet
- Quím CinéticaDocument8 pagesQuím CinéticaJoão Ribeiro Franco NetoNo ratings yet
- Cinética QuímicaDocument6 pagesCinética QuímicaSirlei Gonçalves PoffoNo ratings yet
- Cinética Química: Velocidade de ReaçõesDocument166 pagesCinética Química: Velocidade de Reaçõesandrevini890% (1)
- Manual 0349Document57 pagesManual 0349Rita CatitaNo ratings yet
- Balancim e AndaimesDocument52 pagesBalancim e AndaimesbacogoNo ratings yet
- Figuras de EstiloDocument3 pagesFiguras de EstiloLuís 060No ratings yet
- Lista de Exercicios Cinetica Quimica EQM061Document13 pagesLista de Exercicios Cinetica Quimica EQM061Mariana DomicianoNo ratings yet
- Lista de exercícios de cinética e equilíbrio químicoDocument7 pagesLista de exercícios de cinética e equilíbrio químicoLeonardo Alves de OliveiraNo ratings yet
- Dissertação Marcelo Mayora - Versão FinalDocument293 pagesDissertação Marcelo Mayora - Versão FinalmarianadutragarciaNo ratings yet
- Fatores que alteram a velocidade de reações químicasDocument27 pagesFatores que alteram a velocidade de reações químicasLuiza FreitasNo ratings yet
- Alfa - Módulo 40Document28 pagesAlfa - Módulo 40Luiza FreitasNo ratings yet
- Lista de Exercícios I (2º Bimestre) - 3º AnoDocument3 pagesLista de Exercícios I (2º Bimestre) - 3º AnoMikeas LimaNo ratings yet
- CURSO QUÍMICA REAÇÕESDocument11 pagesCURSO QUÍMICA REAÇÕESMauro RomeroNo ratings yet
- Cinética QuímicaDocument5 pagesCinética QuímicaJames OliverNo ratings yet
- Cinética Química: exercícios sobre energia de ativação e velocidade de reaçõesDocument14 pagesCinética Química: exercícios sobre energia de ativação e velocidade de reaçõesFrancis Francisco Johane SemanaNo ratings yet
- 2012 cm0690 Cinetica Quimica 02Document22 pages2012 cm0690 Cinetica Quimica 02R4d1c4lDr34m3rNo ratings yet
- Cinética químicaDocument6 pagesCinética químicaRanked PlayerNo ratings yet
- Lista de Exercícios Cinética QuímicaDocument6 pagesLista de Exercícios Cinética QuímicagabezmirandaNo ratings yet
- Cinetica CompletaDocument5 pagesCinetica CompletaConta ReservaNo ratings yet
- Ficha 12Document9 pagesFicha 12Gustavo FernandoNo ratings yet
- CINÉTICADocument7 pagesCINÉTICAVaneilton ReynaudNo ratings yet
- Cinética Blog PDFDocument6 pagesCinética Blog PDFWelff JuniorNo ratings yet
- Cinetica Quimica If ExercDocument5 pagesCinetica Quimica If ExercRaquel Andreola ValenteNo ratings yet
- Reação química: cinética e fatores que influenciam a velocidadeDocument10 pagesReação química: cinética e fatores que influenciam a velocidadeErick Teckio100% (1)
- Química 12a provaDocument2 pagesQuímica 12a provaDinis JustinoNo ratings yet
- DF Quimica Welson 5e790a5ce82acDocument28 pagesDF Quimica Welson 5e790a5ce82acPedro HenriqueNo ratings yet
- Velocidade Das Reações - ÍtaloDocument8 pagesVelocidade Das Reações - ÍtaloItalo PiresNo ratings yet
- Matéria e Suas PropriedadesDocument28 pagesMatéria e Suas PropriedadesGleisonNo ratings yet
- Exercicios de Cinetica QuimicaDocument3 pagesExercicios de Cinetica QuimicaOrnilia MatiasNo ratings yet
- Cinetica QuimicaDocument2 pagesCinetica QuimicaCMJ O caderno mágico do JamesNo ratings yet
- Cinetica - Fatores Que Alteram A Velocidade - 20220215124854 - U2FsdDocument7 pagesCinetica - Fatores Que Alteram A Velocidade - 20220215124854 - U2FsdJoao MaiaNo ratings yet
- Exercícios de Cinética QuímicaDocument8 pagesExercícios de Cinética QuímicaLuana CuccaroloNo ratings yet
- Exercício de CinéticaDocument7 pagesExercício de CinéticaIsaque MouraNo ratings yet
- Lista Exercicio Cinetica QuimicaDocument4 pagesLista Exercicio Cinetica QuimicaKely GontijoNo ratings yet
- Lista Da Aula 3 - Cinética QuímicaDocument5 pagesLista Da Aula 3 - Cinética QuímicaE P Som RJNo ratings yet
- Cinética Química - Objetivas - BásicoDocument4 pagesCinética Química - Objetivas - BásicoLeonardo JacquesNo ratings yet
- Cinetica Quimica 21 Questoes Com GabaritoDocument6 pagesCinetica Quimica 21 Questoes Com GabaritoCíntia GhettiNo ratings yet
- Resumo Quimica Terceiro Ano Ensino MédioDocument32 pagesResumo Quimica Terceiro Ano Ensino MédioLuariel BrochiNo ratings yet
- Formação de estalactites em cavernasDocument9 pagesFormação de estalactites em cavernasfernandaveredianoNo ratings yet
- Cinética química: decomposição de N2O5Document3 pagesCinética química: decomposição de N2O5RiaNo ratings yet
- 156Document4 pages156Danielle GianniniNo ratings yet
- EXERCICIOS CINÉTICA EQUIL Isct 12 CLASSE PDFDocument5 pagesEXERCICIOS CINÉTICA EQUIL Isct 12 CLASSE PDFKeila Jessica SamsonNo ratings yet
- Cinetica ExerciciosDocument2 pagesCinetica ExercicioscarlostucupiNo ratings yet
- Velocidade Média das Reações: Fatores que Afetam e Exercícios ResolvidosDocument28 pagesVelocidade Média das Reações: Fatores que Afetam e Exercícios ResolvidosIque Castro MarianoNo ratings yet
- Atividade Cinética II SGDocument7 pagesAtividade Cinética II SGademairmoreiraNo ratings yet
- Lista Cinética 2023 - 2TDocument2 pagesLista Cinética 2023 - 2TRafael playeraleNo ratings yet
- Fase_3_Lista_1_cinética_com_gabaritoDocument4 pagesFase_3_Lista_1_cinética_com_gabaritoventiladoramoebaNo ratings yet
- Ficha de QuimicaDocument4 pagesFicha de QuimicavivaldoNo ratings yet
- Cinética Química: Velocidade de ReaçõesDocument4 pagesCinética Química: Velocidade de ReaçõesOFito FernandesNo ratings yet
- Equilíbrio e CinéticaDocument7 pagesEquilíbrio e CinéticaHidro Solo - Departamento TécnicoNo ratings yet
- DF Quimica Welson 5e790946badf2 PDFDocument27 pagesDF Quimica Welson 5e790946badf2 PDFKeverto. SoaresNo ratings yet
- Exercícios Revisão CinéticaDocument20 pagesExercícios Revisão CinéticaIara DaherNo ratings yet
- Lista Cinética QuímicaDocument6 pagesLista Cinética QuímicavfmgarciaNo ratings yet
- Revisà o 2 S㩠Rie Termoquà - Mica - SagradoDocument6 pagesRevisà o 2 S㩠Rie Termoquà - Mica - SagradoNoemia CarolinaNo ratings yet
- Quimica ADocument10 pagesQuimica Ahelenaquevedo64No ratings yet
- Cinética QuímicaDocument9 pagesCinética QuímicaPauloMesquitaNo ratings yet
- Exercícios de Cinética Química Prof. Flokinho: 2 3 2 (G) 3 (G) 3 (G) 2 (G)Document2 pagesExercícios de Cinética Química Prof. Flokinho: 2 3 2 (G) 3 (G) 3 (G) 2 (G)Sara LunaNo ratings yet
- FQ Cap3Document6 pagesFQ Cap3filipelima.graveNo ratings yet
- Ficha de Exercicios de Preparacao-1Document27 pagesFicha de Exercicios de Preparacao-1Damião JeremiasNo ratings yet
- Cinetica Quimica Enunciados 20190625-080524Document52 pagesCinetica Quimica Enunciados 20190625-080524Júlia DemunerNo ratings yet
- LISTA9Document12 pagesLISTA9Amanda Tenório BatistaNo ratings yet
- Cinética química exercíciosDocument6 pagesCinética química exercíciosNazareno BragaNo ratings yet
- Cálculo II 1 Lista - FÇ 2 Variáveis - 2004Document6 pagesCálculo II 1 Lista - FÇ 2 Variáveis - 2004Alan FrancoNo ratings yet
- Complexo Eletrônico BrasileiroDocument28 pagesComplexo Eletrônico BrasileiroNatalia AmaralNo ratings yet
- PDF Licitação e Contrato Administrativo PDFDocument25 pagesPDF Licitação e Contrato Administrativo PDFNatalia AmaralNo ratings yet
- Livre Comércio Versus Protecionismo - Uma Analise Das Principais Teorias de Comércio Internacional PDFDocument18 pagesLivre Comércio Versus Protecionismo - Uma Analise Das Principais Teorias de Comércio Internacional PDFNatalia AmaralNo ratings yet
- A Evolucao Do Setor Industrial Madeireiro em Rondonia e A Exploracao Dos Recursos FlorestaisDocument12 pagesA Evolucao Do Setor Industrial Madeireiro em Rondonia e A Exploracao Dos Recursos FlorestaisNatalia AmaralNo ratings yet
- Geoprocessaento Na Organização e Análise de Dados Sócio-Econômicos Municipais para MGDocument27 pagesGeoprocessaento Na Organização e Análise de Dados Sócio-Econômicos Municipais para MGNatalia AmaralNo ratings yet
- Crocco Et Al-2006-Nova Economia PDFDocument31 pagesCrocco Et Al-2006-Nova Economia PDFNatalia AmaralNo ratings yet
- Bases Do Nacionalismo Econômico em Friedrich ListDocument23 pagesBases Do Nacionalismo Econômico em Friedrich ListNatalia AmaralNo ratings yet
- Polinômios e Equações PolinomiaisDocument45 pagesPolinômios e Equações PolinomiaisNatalia AmaralNo ratings yet
- MiniCurso - Introd Econometria Espacial PDFDocument77 pagesMiniCurso - Introd Econometria Espacial PDFMarcoJulioKolinskyNo ratings yet
- Cysne - Curso de Matemática para Economistas - Cap. 1 e 2 PDFDocument75 pagesCysne - Curso de Matemática para Economistas - Cap. 1 e 2 PDFIago Henrique Rodrigues MonteiroNo ratings yet
- A política econômica do governo Dilma: um período de experimentalismoDocument116 pagesA política econômica do governo Dilma: um período de experimentalismoMontesein RafaelNo ratings yet
- Força Elétrica - IiDocument2 pagesForça Elétrica - IiNatalia AmaralNo ratings yet
- Como Fazer A TeseDocument2 pagesComo Fazer A TeseNatalia AmaralNo ratings yet
- Geometria Espacial BlogDocument34 pagesGeometria Espacial BlogNatalia AmaralNo ratings yet
- Cardápio Atkins 7 DiasDocument8 pagesCardápio Atkins 7 DiasBruna JesusNo ratings yet
- Lista de Exercícios - Sistemas LinearesDocument4 pagesLista de Exercícios - Sistemas LinearesJulieneGarciaNo ratings yet
- Binômio de Newton e exercíciosDocument1 pageBinômio de Newton e exercíciosNatalia AmaralNo ratings yet
- Sistema Endócrino e DiabetesDocument17 pagesSistema Endócrino e DiabetesNatalia AmaralNo ratings yet
- The Sims 3 SitesDocument2 pagesThe Sims 3 SitesNatalia AmaralNo ratings yet
- 50 Perguntas Mais Frequentes em Entrevistas de EmpregoDocument7 pages50 Perguntas Mais Frequentes em Entrevistas de Emprego石原 フラビオNo ratings yet
- Orocongo Saber e o Coletivo Laava - Uma Plataforma deDocument13 pagesOrocongo Saber e o Coletivo Laava - Uma Plataforma deLeonardo LimaNo ratings yet
- Lewis CarolDocument1 pageLewis CarolLuana M.No ratings yet
- Acolhida - QCP - CmneDocument16 pagesAcolhida - QCP - Cmnejorge.a.oliveiraNo ratings yet
- UNLista 30426 LI5EVPv7Document13 pagesUNLista 30426 LI5EVPv7Rebecca VenturaNo ratings yet
- Cópia de Controle de Assistecia Tecnica PROTECSEGDocument65 pagesCópia de Controle de Assistecia Tecnica PROTECSEGMarcio SouzaNo ratings yet
- Análise da gestão de resíduos sólidos em empresasDocument2 pagesAnálise da gestão de resíduos sólidos em empresasTEN TTusNo ratings yet
- RefrerencialDocument20 pagesRefrerencialPedro Nuno SantosNo ratings yet
- Pronomes de tratamento oficiaisDocument12 pagesPronomes de tratamento oficiaisAmanda Santos100% (1)
- Relatório Estagio Torno ConvencionalDocument49 pagesRelatório Estagio Torno ConvencionalMarcelo FeniliNo ratings yet
- Ficha Tobias v0.55Document4 pagesFicha Tobias v0.55VanilaNo ratings yet
- Primeira meditação cartesiana de HusserlDocument16 pagesPrimeira meditação cartesiana de HusserltomascbNo ratings yet
- AcasDocument123 pagesAcassandeep5100% (1)
- TCC 19-11 - Revisado e FormatadoDocument66 pagesTCC 19-11 - Revisado e FormatadooliveiracaduNo ratings yet
- Jornal de Aprendizagem - OPORTUNIDADEDocument7 pagesJornal de Aprendizagem - OPORTUNIDADEchico1977No ratings yet
- Um Encontro Intermulticultural de Aguas BrasivianasDocument19 pagesUm Encontro Intermulticultural de Aguas BrasivianasLuciano LealNo ratings yet
- 2 Visita Técnica À Fábrica de Lubrificantes OILTECBRASDocument8 pages2 Visita Técnica À Fábrica de Lubrificantes OILTECBRASNick EduNo ratings yet
- Funções de Manipulação de ArquivoDocument4 pagesFunções de Manipulação de Arquivocock4546No ratings yet
- Capitulo Sobre A Poti PiauiDocument84 pagesCapitulo Sobre A Poti PiauiJaqueMorais29No ratings yet
- Comunicação HumanaDocument7 pagesComunicação HumanaLaura AzevedoNo ratings yet
- Contos de FadasDocument4 pagesContos de Fadasemérico arnaldoNo ratings yet
- Joy Mills - Uma Jornada EvolutivaDocument15 pagesJoy Mills - Uma Jornada EvolutivaPaulo BaptistaNo ratings yet
- 2.1 Estratégias e Atitudes Na ComunicaçãoDocument3 pages2.1 Estratégias e Atitudes Na ComunicaçãoCarmindo LuzNo ratings yet
- Acesso ao site Poder Público RGEDocument44 pagesAcesso ao site Poder Público RGEKiko LikoNo ratings yet
- Tabela Periódica Exercícios ConfiguraçõesDocument3 pagesTabela Periódica Exercícios ConfiguraçõesAíla LimaNo ratings yet