Professional Documents
Culture Documents
Regla de La Palanca
Uploaded by
Ashinko KunCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Regla de La Palanca
Uploaded by
Ashinko KunCopyright:
Available Formats
REGLA DE LA PALANCA Estas cantidades normalmente se expresan como porcentaje del peso (% peso), es una regla matemtica valida
para cualquier diagrama binario. En regiones de una sola fase, la cantidad de la fase simple es 100%. En regiones bifsicas, sin embargo, se deber calcular la cantidad de cada fase. na t!cnica es "acer un balance de materiales. #ara calcular las cantidades de l$quido % de s&lido, se constru%e una palanca sobre la isoterma con su punto de apo%o en la composici&n original de la aleaci&n (punto dado). El bra'o de la palanca, opuesto a la composici&n de la fase cu%a cantidad se calcula se divide por la longitud total de la palanca, para obtener la cantidad de dic"a fase. En general la regla de la palanca se puede escribir de la siguiente forma( #)*+E,-./E 0E 1.2E 3 bra'o opuesto de palanca x 100 4ongitud local de la isoterma 2e puede utili'ar la regla de la palanca en cualquier regi&n bifsica de un diagrama de fases binario. En regiones de una fase no se usa el clculo de la regla de la palanca puesto que la respuesta es obvia (existe un 100% de dic"a fase presente). #asos para calcular las composiciones( 1.0ibujar la isoterma.
5.Encontrar el largo del lado opuesto a la composici&n deseada.
6.0ividir el largo del opuesto por la isoterma(
7.El resultado se multiplica por 100. Ejercicio #ara dejar esto ms claro, se pondr un ejemplo( na aleaci&n de cobre 8 n$quel contiene 79% en peso de +u % :6% de ,i % est a 1.600 ;+. (a)<+ul es el porcentaje en peso de cobre en las fases s&lida % l$quida a esta temperatura= (b)<>u! porcentaje en peso de la aleaci&n es l$quida, % qu! porcentaje es s&lida=
Solucin(
a) % +u en fase l$quida( ::% +u % +u en fase s&lida( 75% +u ?s3 (@0 A@l) B (@28@l) b) #ara el ,$quel( Co 3 :6%, Cl 3 7:%, Cs 3 :D%. @s3 (:687:) B (:D87:) 3 0,E5 @l 3 (@s8@0) B (@s8@l)3 (:D8:6)B(:D87:)3 0,6D
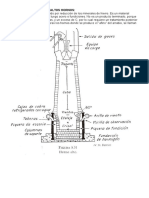
Diagrama Fe-C. Fases en el sistema Fe-Fe3C. En la figura 7.1 se representa el
diagrama de fases del sistema binario 1e8 1e 6+ para contenidos altos de "ierro. El "ierro sufre cambios estructurales con la temperatura antes de fundir. . temperatura ambiente la forma estable es la ferrita o 1e8 (estructura ++F). . G15 ;+ la ferrita sufre
una transformaci&n polim&rfica a austenita o 1e8 (+++). 4a austenita se transforma a otra fase ++F a 16G7 ;+ que se conoce como ferrita8 , la cual funde a1:6D ;+. -odos estos cambios se pueden observar en el eje vertical del diagrama de fases para el "ierro puro. El otro eje de la figura 7.1 s&lo llega al E.90 % en peso de +, concentraci&n que coincide con el 100 % molar del compuesto intermedio 1e6+ conocido como carburo de "ierro o cementita. 4a parte entre el E.90 % de + % el 100 % de + (grafito puro) no es importante desde el punto de vista tecnol&gico % no se va a estudiar. El carbono en un soluto intersticial en el "ierro % forma disoluciones s&lidas con la ferrita ( % ) % con la austenita (). 4a ferrita tiene una estructura ++F % en los intersticios se puede situar mu% poco carbono, el mximo es un 0.055 % a 959 ;+. .unque en proporci&n mu% baja, el carbono afecta muc"o a las propiedades mecnicas de la ferrita. Esta fase es relativamente blanda, ferromagn!tica por debajo de 9ED ;+, % de densidad 9.DD gBcc. 4a austenita (1e8) de estructura +++ tiene una solubilidad mxima de carbono del 5.11 % a 117D ;+. 2olubilidad aproximadamente 100 veces superior a la de la ferrita. 4as transformaciones de fase de la austenita son mu% importante en los tratamientos t!rmicos de los aceros como se ver ms adelante. 4a ferrita8 solo se diferencia de la en el tramo de temperatura donde existe. .l ser s&lo estable a altas temperaturas no tiene inter!s t!cnico.4a cementita desde el punto de vista mecnico es dura % frgil, % su presencia aumenta la resistencia de muc"os aceros.
ALEACIONES HIERRO-CARBONO
El "ierro puro apenas tiene aplicaciones industriales, pero formando aleaciones con el carbono (adems de otros elementos), es el metal ms utili'ado en la industria moderna. . la temperatura ambiente, salvo una pequeHa parte disuelta en la ferrita, todo el carbono que contienen las aleaciones 1e8+ est en forma de carburo de "ierro( +1e6 ). #or eso, las aleaciones 1e8+ se denominan tambi!n aleaciones "ierro8carburo de "ierro. 4as aleaciones con contenido de + comprendido entre 0.06% % 1.9E% tienen caracter$sticas mu% bien definidas % se denominan aceros. 4os aceros de cualquier proporci&n de carbono dentro de los l$mites citados pueden alearse con otros elementos, formando los denominados aceros aleados o aceros especiales. .lgunos aceros aleados pueden contener excepcionalmente "asta el 5.:% de +. 4os aceros generalmente son forjables, % es !sta una cualidad mu% importante que los distingue. 2i la proporci&n de + es superior a 1.9E% las aleaciones de 1e8+ se denominan fundiciones, siendo la mxima proporci&n de + aleado del E.E9%, que corresponde a la cementita pura. 4as fundiciones, en general, no son forjables. Tipos de aceros: En las aleaciones 1e8+ pueden encontrarse "asta once constitu%entes diferentes, que se denominan( ferrita, cementita, perlita, austenita, martensita, troostita sorbita, bainita, ledeburita, steadita % grafito.
FERRITA
.unque la ferrita es en realidad una soluci&n s&lida de carbono en "ierro alfa, su solubilidad a la temperatura ambiente es tan pequeHa que no llega a disolver ni un 0.00D% de +. Es por esto que prcticamente se considera la ferrita como "ierro alfa puro. 4a ferrita es el ms blando % dIctil constitu%ente de los aceros. +ristali'a en una estructura J++. -iene una dure'a de G: KicLers, % una resistencia a la rotura de 5D MgBmm5, llegando a un alargamiento del 6: al 70%. .dems de todas estas caracter$sticas, presenta propiedades magn!ticas. En los aceros aleados, la ferrita suele contener ,i, Nn, +u, 2i, .l en disoluci&n s&lida sustitucional. .l microscopio aparece como granos monofsicos, con l$mites de grano ms irregulares que la austenita. El motivo de esto es que la ferrita se "a formado en una transformaci&n en estado s&lido, mientras que la austenita, procede de la solidificaci&n. 4a ferrita en la naturale'a aparece como elemento proeutectoide que acompaHa a la perlita en( 8 8 8 +ristales me'clados con los de perlita (0.::% +) 1ormando una red o malla que limita los granos de perlita (0.::% a 0.D:% de +) 1ormando agujas en direcci&n de los planos cristalogrficos de la austenita.
CE EN!I!A
Es carburo de "ierro % por tanto su composici&n es de E.E9% de + % G6.66% de 1e en peso. Es el constitu%ente ms duro % frgil de los aceros, alcan'ando una dure'a de GE0 KicLers. +ristali'a formando un paralelep$pedo ortorr&mbico de gran tamaHo. Es magn!tica "asta los 510O+, temperatura a partir de la cual pierde sus propiedades magn!ticas. .parece como( 8 8 8 8 +ementita proeutectoide, en aceros "ipereutectoides, formando un red que envuelve a los granos perl$ticos. +omponente de la perlita laminar. +omponente de los gl&bulos en perlita laminar. +ementita alargada (terciaria) en las uniones de los granos (0.5:% de +)
PERLITA
Es un constitu%ente compuesto por el DE.:% de ferrita % el 16.:% de cementita, es decir, "a% E.7 partes de ferrita % 1 de cementita. 4a perlita tiene una dure'a de aproximadamente 500 KicLers, con una resistencia a la rotura de D0 MgBmm5 % un alargamiento del 1:%. +ada grano de perlita est formado por lminas o placas alternadas de cementita % ferrita. Esta estructura laminar se observa en la perlita formada por enfriamiento mu% lento. 2i el enfriamiento es mu% brusco, la estructura es ms borrosa % se denomina perlita sorb$tica. 2i la perlita laminar se
calienta durante algIn tiempo a una temperatura inferior a la cr$tica (956 O+), la cementita adopta la forma de gl&bulos incrustados en la masa de ferrita, recibiendo entonces la denominaci&n de perlita globular.
AUSTENITA
Este es el constitu%ente ms denso de los aceros, % est formado por la soluci&n s&lida, por inserci&n, de carbono en "ierro gamma. 4a proporci&n de + disuelto var$a desde el 0 al 1.9E%, correspondiendo este Iltimo porcentaje de mxima solubilidad a la temperatura de 1160 O+.4a austenita en los aceros al carbono, es decir, si ningIn otro elemento aleado, empie'a a formarse a la temperatura de 956O+. -ambi!n puede obtenerse una estructura austen$tica en los aceros a temperatura ambiente, enfriando mu% rpidamente una probeta de acero de alto contenido de + a partir de una temperatura por encima de la cr$tica, pero este tipo de austenita no es estable, % con el tiempo se transforma en ferrita % perlita o bien cementita % perlita. Excepcionalmente, "a% algunos aceros al cromo8niquel denominados austen$ticos, cu%a estructura es austen$tica a la temperatura ambiente. 4a austenita est formada por cristales cIbicos de "ierro gamma con los tomos de carbono intercalados en las aristas % en el centro. 4a austenita tiene una dure'a de 60: KicLers, una resistencia de 100 MgBmm5 % un alargamiento de un 60 %. ,o presenta propiedades magn!ticas.
MARTENSITA
Jajo velocidades de enfriamiento bajas o moderadas, los tomos de + pueden difundirse "ac$a afuera de la estructura austen$tica. 0e este modo, los tomos de 1e se mueven ligeramente para convertir su estructura en una tipo J++. Esta transformaci&n gamma8alfa tiene lugar mediante un proceso de nucleaci&n % crecimiento dependiente del tiempo (si aumentamos la velocidad de enfriamiento no "abr tiempo suficiente para que el carbono se difunda en la soluci&n %, aunque tiene lugar algIn movimiento local de los tomos de 1e, la estructura resultante no podr llagar a ser J++, %a que el carbono est PatrapadoQ en la soluci&n). 4a estructura resultante denominada martensita, es una soluci&n s&lida sobresaturada de carbono atrapado en una estructura tetragonal centrada en el cuerpo. Esta estructura reticular altamente distorsionada es la principal ra'&n para la alta dure'a de la martensita, %a que como los tomos en la martensita estn empaquetados con una densidad menor que en la austenita, entonces durante la transformaci&n (que nos lleva a la martensita) ocurre una expansi&n que produce altos esfuer'os locali'ados que dan como resultado la deformaci&n plstica de la matri'. 0espu!s de la cementita es el constitu%ente ms duro de los aceros. 4a martensita se presenta en forma de agujas % cristali'a en la red tetragonal. 4a proporci&n de carbono en la martensita no es constante, sino que var$a "asta un mximo de 0.DG% aumentando su dure'a, resistencia mecnica % fragilidad con el contenido de carbono. 2u dure'a est en torno a :70 KicLers, % su resistencia mecnica var$a de 19: a 5:0 MgBmm5 % su alargamiento es del orden del 5.: al 0.:%. .dems es magn!tica.
BAINITA
2e forma la bainita en la transformaci&n isoterma de la austenita, en un rango de temperaturas de 5:0 a ::0O+. El proceso consiste en enfriar rpidamente la austenita "asta una temperatura constante, manteni!ndose dic"a temperatura "asta la transformaci&n total de la austenita en bainita.
LEDEBURITA
4a ledeburita no es un constitu%ente de los aceros, sino de las fundiciones. 2e encuentra en las aleaciones 1e8+ cuando el porcentaje de carbono en "ierro aleado es superior al 5:%, es decir, un contenido total de 1.9E% de carbono. 4a ledeburita se forma al enfriar una fundici&n l$quida de carbono (de composici&n alrededor del 7.6% de +) desde 1160O+, siendo estable "asta 956O+, decomponi!ndose a partir de esta temperatura en ferrita % cementita
You might also like
- Astm E3-95Document12 pagesAstm E3-95Diego R. AllaucaNo ratings yet
- Clase 9. Aplicación Regla de La PalancaDocument16 pagesClase 9. Aplicación Regla de La PalancaJairo Silva CoreaNo ratings yet
- Regla de La PalancaDocument8 pagesRegla de La PalancaFrancisco Javier CanoNo ratings yet
- Potencial Zeta en 5 MinDocument14 pagesPotencial Zeta en 5 MinCarlos GamarraNo ratings yet
- EyutDocument15 pagesEyutLuis FernandezNo ratings yet
- Procesos de Obtencion Del Hierro AceroDocument103 pagesProcesos de Obtencion Del Hierro AceroivanNo ratings yet
- Flujo Del FluidoDocument2 pagesFlujo Del FluidojonathanNo ratings yet
- CalcinaciónDocument2 pagesCalcinaciónSofía De AndaNo ratings yet
- Aleacion Zinc y MagnesioDocument10 pagesAleacion Zinc y MagnesioMaria HerasNo ratings yet
- Reologia y PropiedadesDocument33 pagesReologia y PropiedadesJorge D. VarelaNo ratings yet
- QCASDocument51 pagesQCASIkkI-N-mIzUkINo ratings yet
- Manual de Prácticas de Química Orgánica IIIDocument60 pagesManual de Prácticas de Química Orgánica IIIAthenas A.PNo ratings yet
- Solidificación UnidireccionalDocument16 pagesSolidificación UnidireccionalKarina FloresNo ratings yet
- Designacion Magnesio 2014Document9 pagesDesignacion Magnesio 2014MiguelMTNo ratings yet
- Curva de solubilidad HCCl3-CH3COOH-H2ODocument14 pagesCurva de solubilidad HCCl3-CH3COOH-H2OSteevenRafaelPinargoteNo ratings yet
- Difusión de Carbono en El Acero Aisi 8620Document28 pagesDifusión de Carbono en El Acero Aisi 8620alexisNo ratings yet
- Calci NaciónDocument8 pagesCalci NaciónguiovanaNo ratings yet
- Eliminación cianuro aguas residuales mineríaDocument19 pagesEliminación cianuro aguas residuales mineríaAbraham ParedesNo ratings yet
- Rol Del Ingeniero Químico en El Desarrollo Del PaísDocument4 pagesRol Del Ingeniero Químico en El Desarrollo Del PaísMayra YaniraNo ratings yet
- Determinación de plomo con EDTADocument10 pagesDeterminación de plomo con EDTACristiano Ronaldo wasfNo ratings yet
- Intercaras en Cristales y MicroestructurasDocument26 pagesIntercaras en Cristales y MicroestructurasjorgeNo ratings yet
- Boletín Informativo # 1 - METTLER TOLEDODocument2 pagesBoletín Informativo # 1 - METTLER TOLEDOMauricio Cruz100% (1)
- Zaida Proceso de Produccion de NiquelDocument23 pagesZaida Proceso de Produccion de NiquelMairet Chacon100% (1)
- Clase 1 de PolimerosDocument8 pagesClase 1 de PolimerosDanielys AlvarezNo ratings yet
- Síntesis de Una PerovskitaDocument6 pagesSíntesis de Una PerovskitaDiana LopezNo ratings yet
- Transferencia de Masa Por DifusionDocument58 pagesTransferencia de Masa Por DifusionCristhianPLNo ratings yet
- Preparación de probetas metalográficasDocument17 pagesPreparación de probetas metalográficasGian Juarez RondoNo ratings yet
- Diagrama Ternario de Una Mezcla de Compuestos Parcialmente MisciblesDocument7 pagesDiagrama Ternario de Una Mezcla de Compuestos Parcialmente MisciblesSolo alguienNo ratings yet
- La PerovskitaDocument15 pagesLa PerovskitaDayana CanoNo ratings yet
- Uso Diagramas TernariosDocument35 pagesUso Diagramas TernariosCarl's Adirolf ParadiseNo ratings yet
- Sistemas TernariosDocument57 pagesSistemas TernariosNaTalia Becerra100% (1)
- Adsorción en fase líquida: Isotermas y aplicacionesDocument43 pagesAdsorción en fase líquida: Isotermas y aplicacionesLourdes Lizbeth GonzalesNo ratings yet
- Preparación de Muestra IDocument77 pagesPreparación de Muestra IMaela C O'SheaNo ratings yet
- Introducción A La Química Física de SuperficiesDocument4 pagesIntroducción A La Química Física de SuperficiesGeorge ValvuenaNo ratings yet
- Explicacion Celda MercurioDocument1 pageExplicacion Celda MercurioLucas SarnariNo ratings yet
- Cálculo Propiedades TermodinámicasDocument11 pagesCálculo Propiedades TermodinámicasMijhael Anatholi Romero MamaniNo ratings yet
- Transiciones de Fases Unidad II Cinètica de Las Transformaciones de FaseDocument85 pagesTransiciones de Fases Unidad II Cinètica de Las Transformaciones de Fasecoreano63No ratings yet
- Catalogo de Implantes - Introduccion A Los Biomateriales.Document27 pagesCatalogo de Implantes - Introduccion A Los Biomateriales.Everardo IdkNo ratings yet
- Fenómenos de TransporteDocument12 pagesFenómenos de TransporteMaribel OtoyaNo ratings yet
- Nano Material EsDocument16 pagesNano Material EscesitarcalcinaNo ratings yet
- Mineralogía y Obtención de Materiales 2Document128 pagesMineralogía y Obtención de Materiales 2Ailine AmarantaNo ratings yet
- Sistemas ColoidalesDocument16 pagesSistemas ColoidalesmaelraNo ratings yet
- Regla de La PalancaDocument7 pagesRegla de La PalancaJuan Carlos Lema ChulliNo ratings yet
- Regla de La PalancaDocument6 pagesRegla de La Palancabrandontw9No ratings yet
- Sistema Hierro - Carbono Pero SanzDocument74 pagesSistema Hierro - Carbono Pero SanzFranco GutierrezNo ratings yet
- Metalurgia Grupo 4Document24 pagesMetalurgia Grupo 4ALEXANDERCRUSHNo ratings yet
- Ciencia de Los MaterialesDocument4 pagesCiencia de Los MaterialesLuisDavidRosasStarkNo ratings yet
- Diagrama IsomorfoDocument5 pagesDiagrama IsomorfoJordan Muñoz Garcia50% (2)
- Aleaciones HipereutectoidesDocument3 pagesAleaciones HipereutectoidesGianni R. ZorziniNo ratings yet
- Diagrama Hierro-Carbono: Transformaciones y MicroestructurasDocument28 pagesDiagrama Hierro-Carbono: Transformaciones y MicroestructurasEDISON IDROVONo ratings yet
- Diagrama de MariaDocument18 pagesDiagrama de MariaRicardo ArellanoNo ratings yet
- Clasificación de los aceros: tipos y propiedadesDocument3 pagesClasificación de los aceros: tipos y propiedadesCarolinaRodriguezSotoNo ratings yet
- Aleaciones Hierro CarbonoDocument7 pagesAleaciones Hierro Carbonoheyler camposNo ratings yet
- 6.1 Diagrama Fe-Fe3CDocument53 pages6.1 Diagrama Fe-Fe3CFrida MartinezNo ratings yet
- Aceros - Diagrama Fe-C - Microconstituyentes - TratamientosDocument44 pagesAceros - Diagrama Fe-C - Microconstituyentes - Tratamientoswjosel100% (1)
- Ferrita y constituyentes del aceroDocument35 pagesFerrita y constituyentes del aceroRuben Paguay100% (2)
- FerritaDocument2 pagesFerritaDavid CVNo ratings yet
- Certamen 4 PautaDocument5 pagesCertamen 4 PautaMichel MancillaNo ratings yet
- CONSTRUCCION DEL DIAGRAMA Fe-C PDFDocument9 pagesCONSTRUCCION DEL DIAGRAMA Fe-C PDFmauricio100% (1)
- Practica 6Document10 pagesPractica 6Daniel TorresNo ratings yet
- ANUALIDADESDIFERIDASDocument15 pagesANUALIDADESDIFERIDASYasary AlbornozNo ratings yet
- Numeros ... IMODocument15 pagesNumeros ... IMOAshinko KunNo ratings yet
- AmortizacionesDocument31 pagesAmortizacionesAshinko KunNo ratings yet
- Mapa de Ley Gral. de Indijenas...Document1 pageMapa de Ley Gral. de Indijenas...Ashinko KunNo ratings yet
- Regla de La PalancaDocument7 pagesRegla de La PalancaAshinko KunNo ratings yet
- Mapa de Acuerdo 200Document1 pageMapa de Acuerdo 200Ashinko KunNo ratings yet
- Enfoque Formativo de La EvaluacionDocument67 pagesEnfoque Formativo de La Evaluacionرافائيل سانشيزNo ratings yet
- Clase CubiertasDocument79 pagesClase CubiertasEduardoNo ratings yet
- Cimentaciones Pilotaje 120307Document69 pagesCimentaciones Pilotaje 120307quipelo50% (2)
- Arquitectura y La HigieneDocument24 pagesArquitectura y La HigieneAshinko KunNo ratings yet
- Clase CubiertasDocument79 pagesClase CubiertasEduardoNo ratings yet
- G8B3C5Document8 pagesG8B3C5Anahí OsunaNo ratings yet
- Obtención Del ArrabioDocument30 pagesObtención Del ArrabiokaesarNo ratings yet
- 11 Aleaciones No Férreas Al - SNDocument58 pages11 Aleaciones No Férreas Al - SNLuis ApoyalaNo ratings yet
- Unidad III - 1 Tratamientos TérmicosDocument56 pagesUnidad III - 1 Tratamientos TérmicosLuz claritaNo ratings yet
- Material PeltonDocument4 pagesMaterial PeltonWilliam ThompsonNo ratings yet
- 2.4 - Soldaduras 2020 ActDocument21 pages2.4 - Soldaduras 2020 ActMariano IsaacNo ratings yet
- Curvas TTT Isotermicas Acero Especializacion SoldaduraDocument4 pagesCurvas TTT Isotermicas Acero Especializacion SoldaduraJoseNo ratings yet
- 3 Lab Metal - Fisica Ii-Revenido Aceros D3Document19 pages3 Lab Metal - Fisica Ii-Revenido Aceros D3Antony ChuicaNo ratings yet
- Estudio comparativo de la conformabilidad de aceros AHSS y de embutición mediante curvas FLC y LDRDocument99 pagesEstudio comparativo de la conformabilidad de aceros AHSS y de embutición mediante curvas FLC y LDRCamilo BayonaNo ratings yet
- Estructuras de Los Metales Ferrosos y No Ferrosos.Document2 pagesEstructuras de Los Metales Ferrosos y No Ferrosos.Angel Burciaga100% (2)
- Tratamientos Termicos SemestreDocument101 pagesTratamientos Termicos SemestreHeber ArcanaNo ratings yet
- Tabla Microestructa AcerosDocument5 pagesTabla Microestructa AcerosMariangeles Carolina Fonseca YanezNo ratings yet
- Hierro y Sus AleacionesDocument56 pagesHierro y Sus AleacionesJulio Cesar CutipaNo ratings yet
- Ensayo Jominny2023Document10 pagesEnsayo Jominny2023Santiago OrbeaNo ratings yet
- Proceso Productivo Del AceroDocument27 pagesProceso Productivo Del AceroMaría Del A. VargasNo ratings yet
- EL DIAGRAMA Fe CarbonoDocument33 pagesEL DIAGRAMA Fe CarbonodretorNo ratings yet
- Ejercicios TTT y CCTDocument15 pagesEjercicios TTT y CCTElián OviedoNo ratings yet
- Tratamientos TermicosDocument12 pagesTratamientos TermicosAnderson Castro SalazarNo ratings yet
- Curvas CCTDocument22 pagesCurvas CCTyomer20004100% (1)
- Instituto Tecnológico de MoreliaDocument28 pagesInstituto Tecnológico de MoreliamarianaNo ratings yet
- Parcial 2 SoldaduraDocument6 pagesParcial 2 SoldaduraVíctor LópezNo ratings yet
- Informe TemplabilidadDocument7 pagesInforme TemplabilidadBrallan MorenoNo ratings yet
- Tratamientos Termicos de Los AcerosDocument8 pagesTratamientos Termicos de Los AcerosGustavo Alsó100% (1)
- Fundamentos Del Acero de Alta ResistenciaDocument109 pagesFundamentos Del Acero de Alta ResistenciaJulio Rodriguez100% (1)
- Ensayo de Metalografía y Tratamientos Térmicos PDFDocument31 pagesEnsayo de Metalografía y Tratamientos Térmicos PDFdiego andres oviedo tapiasNo ratings yet
- Martensita RevenidaDocument3 pagesMartensita RevenidaIsmael MelendezNo ratings yet
- Aceros MartensíticosDocument3 pagesAceros MartensíticosEduardo SNNo ratings yet
- CAP11 Aceros para HerramientasDocument24 pagesCAP11 Aceros para HerramientasOtoniel Olán JiménezNo ratings yet
- Informe 3 de Estructura y Propiedades de Los MaterialesDocument23 pagesInforme 3 de Estructura y Propiedades de Los MaterialesEd LCNo ratings yet
- Ejercicios Resueltos de Metalurgia Física Ii AaaaaaaaDocument17 pagesEjercicios Resueltos de Metalurgia Física Ii AaaaaaaaXiomara Llanos CordovaNo ratings yet
- Curvas TTTDocument5 pagesCurvas TTTFranco Salinas VargasNo ratings yet