Professional Documents
Culture Documents
Metabolizm To Całokształt Reakcji Biochemicznych Zachodzących W Komórkach Organizmu
Uploaded by
Bartosz0 ratings0% found this document useful (0 votes)
143 views8 pagesOriginal Title
Metabolizm to Całokształt Reakcji Biochemicznych Zachodzących w Komórkach Organizmu
Copyright
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
143 views8 pagesMetabolizm To Całokształt Reakcji Biochemicznych Zachodzących W Komórkach Organizmu
Uploaded by
BartoszCopyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
You are on page 1of 8
1
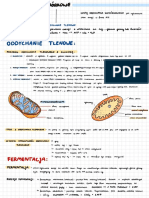
Metabolizm to caoksztat reakcji biochemicznych zachodzcych w komrkach organizmu, zwizany
z przepywem materii, energii i informacji, zapewniajcy m. in. organizmowi wzrost, ruch i
rozmnaanie. Istniej 2 kierunki przemian metabolicznych: anaboliczny i kataboliczny.
Anabolizm obejmuje reakcje syntezy zoonych zwizkw organicznych ze zwizkw prostych.
Reakcje te wymagaj dostarczenia energii, w wyniku czego w produktach syntezy nagromadzona jest
wiksza ilo energii ni w substratach. Do reakcji anabolicznych zaliczamy np. biosyntez biaek,
lipidw czy wglowodanw. Przykadem jest take proces asymilacji CO
2
. w przebiegu fotosyntezy lub
chemosyntezy.
Katabolizm natomiast obejmuje reakcje rozkadu zoonych zwizkw organicznych na produkty
proste, zawierajce mniejszy zapas energii ni substraty. Wyzwolona w tych substratach energia jest
gromadzona w uniwersalnym przenoniku energii adenozyno-5trifosforanie (ATP). ATP jest
nukleozydotrifosforanem zawierajcym adenin, ryboz i trzy grupy fosforanowe Przykadem
katabolitycznego procesu jest oddychanie wewntrzkomrkowe polegajce na rozkadzie zwizkw
zoonych, np. glukozy, na substancje proste, np. H
2
O i CO
2
. W wyniku tego procesu powstaje energia
(magazynowana w ATP), ktra jest wykorzystywana nastpnie do przebiegu wielu funkcji yciowych
organizmu. Zasadniczym rdem ATP s trzy procesy:
1. Glikoliza
2. Cykl kwasu cytrynowego
3. Fosforylacja oksydacyjna, ktra jest najwikszym ilociowo rdem ATP w organizmach tlenowych.
Fosforylacja oksydacyjna wymaga acucha transportu elektronw i wytwarzanie ATP jest zwizane z
utlenianiem NADH i FADH
2
do NAD
+
i FAD oraz z generowaniem gradientu protonowego w poprzek
wewntrznej bony mitochondrialnej :
ADP + P
i
+ NADH + H
+
+ 1/2 O
2
ATP + NAD
+
+H
2
O.
Moe jeszcze istnie inny typ fosforylacji, tzw. fosforylacja substratowa, gdzie synteza ATP z
ADP i P
i
odbywa si na skutek bezporedniego rozkadu (utleniania) substratu, np. kwasu 3-
fosfoglicerynowego do pirogronianu (w czasie glikolizy):
wysokoenergetyczny substrat + P
i
+ ADP niskoenergetyczny produkt + ATP.
Natomiast w komrkach rolinnych zachodzi fosforylacja fotosyntetyczna, gdzie synteza ATP
odbywa si kosztem energii dostarczanej przez kwanty wiata:
ADP + P
i
+ energia wietlna ATP.
Glikoliza
Metabolizm wglowodanw dotyczy przede wszystkim glukozy, ktra we wszystkich komrkach
ssakw jest metabolizowana w procesie glikolizy do pirogronianu. Glikoliza jest to wyjtkowy szlak,
poniewa moe on przebiega zarwno w warunkach tlenowych (aerobowych) i beztlenowych
(anaerobowych) oraz moe dostarcza stosunkowo maych iloci ATP. Jednake w procesie
cakowitego utleniania glukozy w warunkach tlenowych, a wic utleniania take kocowego produktu
glikolizy pirogronianu, konieczny jest udzia nie tylko tlenu, ale rwnie niektrych zespow
enzymw mitochondrialnych, takich jak kompleks dehydrogenazy pirogronianowej, cykl kwasu
cytrynowego oraz acuch oddechowy. W warunkach beztlenowych drode przeksztacaj
pirogronian w etanol. Tworzenie etanolu lub mleczanu z glukozy jest przykadem fermentacji. Glikoliza
zachodzi w cytosolu komrki, gdzie znajduje si wiksza cz enzymw szlaku glikolitycznego.
Glikoliza jest nie tylko podstawow drog metabolizmu glukozy prowadzc do wytwarzania
acetylo-CoA i utleniania w cyklu kwasu cytrynowego, lecz take stanowi gwny szlak metabolizmu
fruktozy i galaktozy pochodzenia pokarmowego. Zasadnicze znaczenie to, e glikoliza moe
dostarcza ATP w nieobecnoci tlenu, co pozwala miniom szkieletowym funkcjonowa sprawnie
przy niedostatecznych procesach aerobowych. Miesie sercowy, przystosowany do warunkw
tlenowych, charakteryzuje si ma aktywnoci glikolityczn.
2
Etapy glikolizy s nastpujce:
1. Glukoza przez fosforylacj z udziaem heksokinazy w obecnoci ATP jest przeksztacana w
glukozo-6-fosforan.
2. Glukozo-6-fosforan (aldoza) ulega izomeryzacji katalizowanej przez izomeraz glukozofosforanow
w fruktozo-6-fosforan (ketoza).
3. Fruktozo-6-fosforan jest fosforylowany z udziaem fosfofruktokinazy w obecnoci ATP w fruktozo-
1,6-bisfosforan.
4. Fruktozo-1,6-bisfosforan (6 atomw wgla) jest rozszczepiany przez aldolaz na dwie czstki:
aldehyd 3-fosfoglicerynowy (3 atomy wgla) i fosfodihydroksyaceton (3 atomy wgla).
5. Aldehyd 3-fosfoglicerynowy jest dalej wykorzystywany w procesie glikolizy i jest on przeksztacany
do 1,3-bisfosfoglicerynianu. Reakcj katalizuje dehydrogenaza aldehydu 3-fosfoglicerynowego z
uyciem nieorganicznego fosforanu i NAD H
+
.
6. 1,3-bisfosfoglicerynian jest przeksztacany do 3-fosfoglicerynianu. Reakcj katalizuje kinaza
fosfoglicerynianowa tworzca te ATP.
7. 3-fosfoglicerynian jest przeksztacany w 2-fosfoglicerynian przez fosfogliceromutaz.
8. Enolaza katalizuje odwodnienie 2-fosfoglicerynianu i powstanie fosfoenolopirogronianu.
9. Kinaza pirogronianowa katalizuje utworzenie pirogronianu i ATP.
Znaczenie glikolizy
1. Wytwarzanie ATP; w reakcjach szlaku glikolitycznego bezporednio powstaj tylko dwie czsteczki
ATP na jedn czsteczk glukozy. Sumaryczna reakcja przeksztacenia glukozy w pirogronian jest
nastpujca:
glukoza + 2P
i
+ 2ADP + 2NAD
+
2 czsteczki pirogronianu + 2ATP + 2NADH + 2H
+
+ + 2H
2
O.
2. Wytwarzanie intermediatw, np. acetylo-CoA - prokursora w syntezie kwasw tuszczowych i
cholesterolu.
2. Glikoliza dostarcza take substratw do cyklu kwasu cytrynowego i fosforylacji oksydacyjnej.
Losy pirogrionianu powstaego w procesie glikolizy
W warunkach tlenowych pirogronian zostaje przeksztacony w acetylo-CoA (CH
3
-CO-S-CoA,
aktywny octan) , ktry wchodzi w cykl kwasu cytrynowego:
pirogronian + NAD
+
+ CoA acetylo-CoA + CO
2
+ NADH.
Reakcj t katalizuje dehydrogenaza pirogronianowa.
W warunkach ograniczonego dostpu tlenu, panujcych podczas intensywnego wysiku
fizycznego, ilo NADH wytwarzanego podczas glikolizy przekracza moliwoci acucha
oddechowego pod wzgldem utleniania NADH z powrotem do NAD
+
. W tym wypadku pirogronian
syntetyzowany w miniu szkieletowym podczas glikolizy zostaje przeksztacony w mleczan przez
dehydrogenaz mleczanow w reakcji generujcej NAD
+
, dziki czemu glikoliza w dalszym cigu
wytwarza ATP. Jednake mleczan jest metabolitem uwizionym w lepej uliczce, poniewa
metabolizowany moe by dalej tylko z powrotem w pirogronian. Mleczan dyfunduje wic z mini do
krwi, skd przechodzi do wtroby. Tutaj w wtrobie, przedostaje si do komrek, gdzie z udziaem
dehydrogenazy mleczanowej zostaje przeksztacony z powrotem w pirogronian. Nastpnie pirogronian
w procesie glukoneogenezy ulega przeksztaceniu w glukoz; ta zostaje uwolniona znw do
krwiobiegu, skd moe by pobierana przez misie szkieletowy (i mzg). Cykl tych reakcji nazywa si
cyklem Corich.
U drody i innych mikroorganizmw, NAD
+
niezbdny do podtrzymywania cigoci glikolizy w
warunkach beztlenowych jest regenerowany w procesie nazywanym fermentacj alkoholow.
Pirogronian zostaje przeksztacony w aldehyd octowy (przez dekarboksylaz pirogronianow), a
nastpnie w etanol (przez dehydrogenaz alkoholow), przy czym w tej drugiej reakcji zachodzi
reoksydacja NADH do NAD
+
:
pirogronian + H
+
aldehyd octowy + CO
2
aldehyd octowy + NADH + H
+
etanol + NAD
+
.
3
Cykl kwasu cytrynowego
Kolejnym etapem tworzenia energii z glukozy w warunkach tlenowych jest oksydacyjna
dekarboksylacja pirogronianu do acetylo-CoA, ktry nastpnie zostaje utleniony do CO
2
w szeregu
reakcji cyklu kwasu cytrynowego, nazywanego rwnie cyklem kwasw trikarboksylowych lub cyklem
Krebsa (od nazwiska odkrywcy, w 1937 r.). Cykl ten stanowi gwne rdo energii wykorzystywanej do
syntezy ATP, a take powstaj w nim prekursory dla wielu rnych szlakw biosyntez. Matriks
mitochondrium jest miejscem, w ktrym przebiega cykl kwasu cytrynowego.
Pomostem czcym glikoliz z cyklem kwasu cytrynowgo jest zachodzca take w matriks
mitochondrium oksydacyjna dekarboksylacja pirogronianu :
pirogronian + CoA + NAD
+
acetylo-CoA + CO
2
+ NADH.
Reakcja ta katalizowana jest przez kompleks dehydrogenazy pirogronianowej.
Dalsze etapy cyklu kwasu cytrynowego s nastpujce:
1. Wytwarzanie cytrynianu z 4-wglowego dwukarboksylowego szczawiooctanu i acetylo-CoA.
Reakcja ta katalizowana jest przez syntaz cytrynianow.
2. Cytrynian jest izomeryzowany do izocytrynianu przez akonitaz (hydrataza akonitowa).
3. Utlenianie izocytrynianu do -ketoglutaranu katalizowane przez dehydrogenaz izocytrynianow.
Reakcja ta wymaga NAD
+
.
4. Oksydacyjna dekarboksylacja -ketoglutaranu do bursztynylo-CoA katalizowana przez kompleks
dehydrogenazy -ketoglutaranowej. Reakcja ta wymaga NAD
+
, jako kofaktora. 5. Przeksztacenie
bursztynylo-CoA w bursztynian katalizowane przez syntetaz bursztynylo-CoA. Reakcja ta wymaga
fosforanu nieorganicznego i GDP lub ATP. 6. Utlenianie bursztynianu do fumaranu katalizowane przez
dehydrogenaz bursztynianow. W reakcji tej uczestniczy FAD.
7. Uwodnienie fumaranu do jabczanu katalizowane przez fumaraz.
8. Utlenienie jabczanu do szczawiooctanu katalizowane przez dehydrogenaz jabczanow. Reakcja
ta wymaga NAD
+
, jako kofaktora.
Sumaryczne rwnanie cyklu kwasu cytrynowego jest nastpujce:
acetylo-CoA + 3NAD
+
+ FAD + GDP + P
i
+ 2H
2
O 2CO
2
+ 3NADH + FADH
2
+ GTP + 2H
+
+ CoA.
Regulacja cyklu kwasu cytrynowego
Na regulacj cyklu ma wpyw kilka parametrw: dostpno substratw, hamujce dziaanie
nagromadzonych produktw i oparte na mechanizmach sprzenia zwrotnego allosteryczne
hamowanie przez nastpne intermediaty cyklu. Najbardziej prawdopodobnymi miejscami regulacji s
reakcje nieodwracalne katalizowane przez nastpujce enzymy:
- syntaz cytrynianow (hamowana przez cytrynian, a take przez ATP)
- dehydrogenaz izocytrynianow (hamowana przez NADH i ATP, a aktywowana przez ADP)
- dehydrogenaz -ketoglutaranow (hamowana przez NADH i bursztynylo-CoA)
- dehydrogenaz pirogronianow (hamowana przez NADH i acetylo-CoA).
Cykl Krebsa przebiega szybciej, gdy poziom energii w komrce jest niski (due stenie ADP, a mae
stenie ATP i NADH), a zwalnia swj przebieg, gdy dochodzi do akumulacji ATP (jak i rwnie
NADH, byrsztynylo-CoA oraz cytrynianu).
Znaczenie cyklu kwasu cytrynowego
- Utlenianie pirogronianu do CO
2
i H
2
O z jednoczesnym uzyskiwaniem energii. Podczas kadego cyklu
powstaje 12 czstek ATP; jedna bezporednio w cyklu, a 11 dziki reoksydacji przez fosforylacj
oksydacyjn trzech czsteczek NADH i jednej czsteczki FADH
2
wytwarzanych w cyklu. Na kad z 3
czstek NADH wytwarzanych podczas cyklu kwasu cytrynowego powstaj w procesie fosforylacji
oksydacyjnej 2,5 czstki ATP, a na 1 czstk FADH
2
powstaje 1,5 czstki ATP. Jedna czsteczka
GTP (lub ATP) jest syntetyzowana bezporednio w reakcji przeksztacajcej bursztynylo-CoA w
bursztynian. Tak wic utlenianie jednej czsteczki glukozy w cyklu kwasu cytrynowego daje 2 ? 12
czsteczek ATP.
- Cykl kwasu cytrynowego poza utlenianiem spenia take inne role metaboliczne. Uczestniczy w
4
glukoneogenezie, transaminacjach, deaminacjach i syntezie kwasw tuszczowych. Intermediaty cyklu
kwasu cytrynowego dostarczaj prekursorw do wielu szlakw biosyntez:
1. synteza aminokwasw nastpuje po transaminacji -ketoglutaranu
2. synteza nukleotydw purynowych i pirymidynowych z -ketoglutaranu i szczawiooctanu
3. szczawiooctan moe by przeksztacany w glukoz w procesie glukoneogenezy
4. bursztynylo-CoA jest najwaniejszym intermediatem w syntezie piercienia porfirynowego grup
hemowych
5. cytrynian przenosi grupy acylowe, potrzebne do syntezy kwasw tuszczowych, z mitochondriw do
cytosolu.
acuch oddechowy
Utworzone m.in. podczas glikolizy czy cyklu kwasu cytrynowego NADH i FADH
2
s bogate
energetycznie, poniewa zawieraj pary elektronw o wysokim potencjale przenoszenia. Energia
swobodna uwalniana w znacznej iloci podczas przenoszenia tych elektronw na tlen czsteczkowy
jest wykorzystywana do syntezy ATP. Elektrony s przenoszone z NADH do O
2
z udziaem trzech
wielkich kompleksw biakowych:
- reduktazy NADH-Q (ubichinon)
- reduktazy cytochromowej
- oksydazy cytochromowej.
Grupami przenoszcymi elektrony s: flawiny, centra elazo-siarkowe, hemy i jony miedzi. Elektrony
czy wodory przepywaj przez acuch oddechowy od skadnikw bardziej elektroujemnych do bardziej
elektrododatniego tlenu. Elektrony przenoszone s z reduktazy NADH-Q do drugiego kompleksu
acucha reduktazy cytochromowej, przez zredukowan form ubichinonu (Q), ktry szybko
dyfunduje w bonie mitochondrialnej. Ubichinon take przenosi elektrony z FADH
2
(wytworzonego w
cyklu kwasu cytrynowego) do reduktazy cytochromowej. Cytochrom c natomiast przerzuca elektrony z
reduktazy cytochromowej na oksydaz cytochromow, bdc kocowym elementem acucha
oddechowego. Zasadnicze skadniki acucha oddechowego oraz transport elektronw.
Wydajno ATP przy utlenianiu glukozy
Podczas cakowitego utleniania glukozy do CO
2
w procesie glikolizy, cyklu kwasu cytrynowego i
acucha oddechowego w warunkach tlenowych tworzy si ok. 30 czsteczek ATP, jak obliczono w
Tabeli 1. W warunkach beztlenowych kocowy produkt glikolizy pirogronian nie wchodzi jednak w
cykl kwasu cytrynowego, ale ulega dekarboksylacji (odczenie CO
2
) i redukcji do etanolu, a ilo
uwolnionej energii jest bardzo maa. Zysk energetyczny z 1 czsteczki glukozy wynosi 2 ATP .
Proces glukoneogenezy
Glukoneogeneza jest procesem obejmujcym wszystkie mechanizmy metaboliczne
odpowiedzialne za przeksztacenie zwizkw niecukrowych, takich jak mleczan i pirogronian,
intermediaty cyklu kwasu cytrynowego, szkielety wglowe wielu aminokwasw oraz glicerol w glukoz
lub glikogen. Proces ten jest ogromnie wany, poniewa mzg i erytrocyty w normalnych warunkach
jako rdo energii wykorzystuj prawie wycznie glukoz. Zapas glikogenu w wtrobie jest
wystarczajcy, aby zaopatrywa mzg w glukoz przez okoo p dnia godowania. Dlatego
glukoneogeneza ma szczeglnie wane znaczenie w okresie godu albo intensywnego wysiku. Do
wytwarzania glukozy w procesie glukoneogenezy podczas godowania zostaj wykorzystane przede
wszystkim aminokwasy pochodzce z rozoonych biaek oraz glicerol otrzymany po rozoeniu
tuszczw. Podczas wysiku poziom glukozy we krwi, konieczny do funkcjonowania mzgu i mini
szkieletowych jest podtrzymywany dziki procesowi glukoneogenezy przebiegajcej w wtrobie.
Glukoneogeneza jest umiejscowiona gwnie w wtrobie oraz nerkach, gdzie znajduje si peen
zestaw niezbdnych enzymw dla tego procesu. Bardzo maa aktywno glukoneogenezy pojawia si
w mzgu oraz w miniach.
Szczawiooctan produkt pierwszej reakcji glukoneogenezy, musi opuci mitochondrium i przej do
cytosolu, w ktrym s zlokalizowane nastpne reakcje enzymatyczne. Dlatego te wytwarzany przez
karboksylaz pirogronianow szczawiooctan musi wyj z mitochondrium. Jednake wewntrzna
bona mitochondrialna komrek zwierzcych jest nieprzepuszczalna dla tego zwizku. Tak wic
5
szczawiooctan wewntrz mitochondrium ulega przeksztaceniu w jabczan z udziaem mitochondrialnej
dehydrogenazy jabczanowej. Jabczan nastpnie przedostaje si przez bon mitochondrialn dziki
specjalnemu biaku transportujcemu, a w cytoplazmie zostaje z powrotem przeksztacony w
szczawiooctan przez dehydrogenaz jabczanow. Szczawioctan spenia dwie wane funkcje. Jest on
nie tylko intermediatem zuywanym w procesie glukoneogenezy, ale take jest kluczowym
intermediatem cyklu kwasu cytrynowego, gdzie czy si z acetylo-CoA tworzc cytrynian i ostatecznie
zostaje zregenerowany w tym cyklu. W glikolizie, glukoza ulega metabolizmowi do pirogronianu.
W glukoneogenezie pirogronian jest przeksztacany do glukozy. Zatem glukoneogeneza wydaje si
by odwrceniem glikolizy. Niemniej glukoneogeneza nie jest odwrceniem glikolizy. Poniewa trzy
reakcje glikolizy s zasadniczo nieodwracalne; katalizuj je nastpujce enzymy: heksokinaza,
fosfofruktokinaza i kinaza pirogronianowa. Dlatego te w procesie glukoneogenezy te trzy reakcje
musz by odwrcone, a wic glukoneogeneza nie jest prostym odwrceniem glikolizy.
Reakcje glukoneogenezy:
1. Karboksylaza pirogronianowa w obecnoci ATP, jednej z witamin B biotyny i CO
2
przeksztaca
pirogronian w szczawiooctan
2. Szczawiooctan zostaje poddany dziaaniu karboksykinazy fosfoenolopirogronianowej, ktra
rwnoczenie dekarboksyluje i fosforyluje go tworzc fosfoenolopirogronian (PEP) i zostaje uwolniony
CO
2
. W reakcji tej jest niezbdny bogatoenergetyczny fosforan w postaci GTP
3. PEP jest przeksztacany w fruktozo-1-6-bisfosforan z udziaem enolazy, fosfogliceromutazy,
fosfoglicerokinazy, dehydrogenazy aldehydu 3-fosfoglicerynowego, izomerazy trifosforanowej i
aldolazy
4. Fruktozo-1-6-bisfosforan jest defosforylowany przez enzym fruktozo-1-6-bisfosfataz i powstaje
fruktozo-6-fosforan
5. Fruktozo-6-fosforan jest przeksztacany w glukozo-6-fosforan z udziaem izomerazy
glukozofosforanowej
6. Glukozo-6-fosforan zostaje przeksztacony w glukoz przez glukozo-6-fosfataz.
Podczas procesu glukoneogenezy zostaj zuyte cztery czsteczki ATP i dwie czsteczki GTP
na jedn czsteczk glukozy, natomiast w czasie glikolizy powstaj dwie czsteczki ATP. Gdyby wic
reakcje glikolizy i glukoneogenezy miay moliwoci rwnoczesnego dziaania, to wynikiem netto
przeksztacenia glukozy w pirogronian i odwrotnie byoby zuycie dwch czsteczek ATP i dwch
czsteczek GTP w tak zwanym cyklu daremnym. Jednak zapobiega temu cile skoordynowana
regulacja glikolizy i glukoneogenezy. Przebieg obu tych szlakw jest koordynowany w ten sposb, e
jeli jeden szlak jest relatywnie nieaktywny, drugi w tym czasie jest bardzo aktywny.
Szlak pentozofosforanowy
rdem siy redukcyjnej w komrce jest zarwno NADH, jak i NADPH, ale czsteczki te peni
cakowicie odmienne funkcje w wikszoci reakcji biochemicznych. NADH jest utleniany w acuchu
oddechowym w celu wytwarzania energii gromadzonej w ATP w drodze fosforylacji oksydacyjnej.
Natomiast NADPH spenia rol donora protonw i elektronw w redukcyjnych procesach biosyntezy.
NADH i NADPH pomimo ich podobnej struktury chemicznej (NADPH rni si tylko od NADH grup
fosforanow przy atomie wgla w pozycji 2 jednej z ryboz) nie mog si zastpowa wzajemnie w
procesach metabolicznych, dlatego te komrka musi przeprowadza wiele reakcji specyficznie
tworzcych NADPH. Reakcje te zgrupowane s w szlaku pentozofosforanowym (szlak pentozowy,
szlak heksozomonofosforanowy lub fosfoglukonianowy), ktry zachodzi w cytosolu i ma istotne
znaczenie w tych tkankach (tkanka tuszczowa, gruczoy mleczne i kora nadnerczy), w ktrych
syntetyzowane s kwasy tuszczowe i steroidy z acetylo-CoA. Aktywno tego szlaku jest niewielka w
tkankach, ktre nie syntetyzuj ani kwasw tuszczowych, ani steroidw, np. w miniach
szkieletowych. Podstawowym zadaniem reakcji szlaku jest utlenianie glukozo-6-fosforanu do rybozo-5-
fosforanu i wytwarzanie NADPH:
glukozo-6-fosforan + 2NADP
+
+ H
2
O rybozo-5-fosforan + 2NADPH + 2H
+
+ CO
2
.
Szlak pentozofosforanowy ma trzy etapy:
1. Reakcje utleniania przeksztacajce glukozo-6-fosforan w rybulozo-5-fosforan z wytworzeniem
dwch czsteczek NADPH. Glukozo-6-fosforan jest utleniany przez dehydrogenaz glukozo-6-
6
fosforanow do 6-fosfoglukono--laktonu (ester wewntrzny midzy grup karboksylow przy atomie
wgla w pozycji 1, a grup hydroksylow przy atomie wgla w pozycji 5). Podczas tej reakcji dochodzi
do wytworzenia NADPH. Nastpnie 6-fosfoglukono--lakton jest hydrolizowany przez laktonaz do 6-
fosfoglukonianu, ktry dalej w obecnoci dehydrogenazy 6-fosfoglukonianowej jest przeksztacany w
rybulozo-5-fosforan. Reakcja katalizowana przez dehydrogenaz 6-fosfoglukonianow jest
dekarboksylacj oksydacyjn. Ponadto reakcja katalizowana przez dehydrogenaz glukozo-6-
fosforanow jest nieodwracalna, a enzym ten jest regulowany przez NADP
+
. Kiedy komrka zuywa
NADPH, to zwikszajce si stenie NADP
+
stymuluje dehydrogenaz glukozo-6-fosforanow,
wskutek czego dziaanie szlaku i regeneracja NADPH przebiegaj szybciej.
2. Izomeryzacja rybulozo-5-fosforanu do rybozo-5-fosforanu z udziaem izomerazy
pentozofosforanowej (rybozofosforanowej).
3. Powizanie szlaku pentozofosforanowego z glikoliz dziaaniem transketolazy i transaldolazy.
Enzymy te katalizuj trzy reakcje odwracalne. W rezultacie w przebiegu tych reakcji z trzech pentoz
powstaj dwie heksozy i jedna trioza. Transketolazy przenosz jednostki dwuwglowe, a transaldolazy
trjwglowe. Cukrem dostarczajcym fragmentw dwu- lub trjwglowych jest zawsze ketoza,
natomiast akceptorem zawsze aldoza. Pierwsz z trzech reakcji czcych szlak pentozofosforanowy z
glikoliz jest powstawanie z dwch pentoz aldehydu 3-fosfoglicerynowego i sedoheptulozo-7-
fosforanu. Donorem fragmentu dwuwglowego w tej reakcji jest ksylulozo-5-fosforan (powstay po
przeksztaceniu rybulozo-5-fosforanu z udziaem epimerazy pentozofosforanowej). Nastpnie aldehyd
3-fosfoglicerynowy i sedoheptulozo-7-fosforan reaguj, tworzc fruktozo-6-fosforan i erytrozo-4-
fosforan. Reakcj t katalizuje transaldolaza. W trzeciej reakcji odbywa si synteza fruktozo-6-
fosforanu i aldehydu 3-fosfoglicerynowego z erytrozo-4-fosforanu i ksylulozo-5-fosforanu z udziaem
transaldolazy. Po zsumowaniu wszystkich trzech reakcji otrzymujemy:
2 ksylulozo-5-fosforan + rybozo-5-fosforan 2 fruktozo-6-fosforan +
+ aldehyd 3-fosfoglicerynowy.
Reakcje katalizowane przez transketolaz i transaldolaz s odwracalne, dlatego kocowe
produkty szlaku pentozofosforanowego mog si zmienia w zalenoci od metabolicznych potrzeb
komrki. Zatem, gdy komrka potrzebuje NADPH, a nie ma zapotrzebowania na rybozo-5-fosforan,
ten ostatni ulega przeksztaceniu w glikolityczny intermediat i jest wczony do glikolizy. W odwrotnej
sytuacji, gdy zapotrzebowanie na rybozo-5-fosforan znacznie przekracza zapotrzebowanie na
NADPH, transketolaza i transaldolaza dziaaj w odwrotnym kierunku, przeksztacaj fruktozo-6-
fosforan i aldehyd 3-fosfoglicerynowy, pobrane z glikolizy, w rybozo-5-fosforan.
Znaczenie szlaku pentozofosforanowego:
- tworzenie NADPH dla redukujcych syntez takich jak synteza kwasw tuszczowych i steroidw
- przeksztacanie heksoz w pentozy, a w szczeglnoci w rybozo-5-fosforan. Rybozo-5-fosforan lub
jego pochodne s potrzebne do syntezy RNA, DNA, NAD
+
, FAD, ATP, koenzymu A i innych wanych
czsteczek
- dostarczenie CO
2
, ktry jest charakterystycznym produktem tego szlaku.
Rozkad i synteza glikogenu
Glikogen jest polisacharydem zapasowym zwierzt, odkadanym gwnie w wtrobie i miniach
szkieletowych, gdzie jest przechowywany w postaci ziaren glikogenu umiejscowionych w cytosolu.
Ponadto glikogen jest atwo uruchamian zapasow form glukozy. Ziarna oprcz glikogenu zawieraj
rwnie enzymy i biaka regulatorowe konieczne dla degradacji i syntezy glikogenu. Jego struktura
przypomina amylopektyn. Glikogen jest duym polimerem zbudowanym z reszt glukozy poczonych
wizaniem 1,4-glikozydowym, od ktrego odchodz odgazienia w miejscach, gdzie wystpuj
wizania 1,6-glikozydowe, pojawiajce si co 6-12 reszt glukozy. Masa czsteczkowa glikogenu
siga ponad 100 milionw, co odpowiada liczbie 6 x 10
+
reszt glukozy.
Metabolizm glikogenu ma due znaczenie, poniewa umoliwia utrzymywanie midzy posikami
odpowiedniego poziomu glukozy we krwi (z glikogenu magazynowanego w wtrobie), a take suy
jako zapas energii dla pracujcych mini. Utrzymywanie odpowiedniego stenia glukozy we krwi jest
wane dla tkanek ze wzgldu na to, e jest ona atwo metabolizowanym rdem energii, szczeglnie
dla mzgu, ktry zuywa wycznie glukoz, z wyjtkiem sytuacji po dugotrwaym godzeniu.
7
Rozkad glikogenu (glikogenoliz) katalizuj dwa enzymy: fosforylaza glikogenowa i enzym
usuwajcy rozgazienia, czyli rozbijajcy wizania 1,6-glikozydowe.
Fosforylaza glikogenowa katalizuje usuwanie reszt glukozy z nieredukujcego koca czsteczki
glikogenu (koniec z wolna grup 4-OH) w formie glukozo-1-fosforanu w ten sposb, e rozbija
wizania 1,4-glikozydowe. Fosforylaza glikogenowa moe usuwa tylko te reszty glukozy, ktre s
oddalone od miejsca rozgazienia o wicej ni pi reszt. Drugim substratem potrzebnym w procesie
rozkadu glikogenu jest ortofosforan (P
i
).
glikogen (n reszt) + P
i
glikogen (n-1 reszt) + glukozo-1-fosforan
Reakcja ta jest przykadem fosforolizy, gdzie wizanie kowalencyjne ulega rozbiciu na skutek dodania
grupy fosforanowej. Jest to reakcja odwracalna.
Do rozkadu glikogenu konieczny jest rwnie enzym usuwajcy rozgazienia, ktry usuwa wizania
1,6-glikozydowe.
Utworzony w reakcji glukozo-1-fosforan zostaje nastpnie przeksztacony w glukozo-6-fosforan przez
fosfoglukomutaz:
glukozo-1-fosforan glukozo-6-fosforan.
Dalszy los glukozo-6-fosforanu zaley od tkanki. W wtrobie znajduje si glukozo-6-fosfataza,
przeksztacajca glukozo-6-fosforan w glukoz, ktra nastpnie dyfunduje do krwi i pozostaje w niej w
moliwie staym steniu:
glukozo-6-fosforan + H
2
O glukoza + P
i
.
W miniach (nie ma glukozo-6-fosfatazy) proces rozkadu glikogenu suy gwnie szybkiemu
uzyskaniu energii, dlatego te glukozo-6-fosforan jest natychmiast metabolizowany w szlaku glikolizy.
Synteza glikogenu (glikogenogeneza) nie jest odwrceniem jego rozkadu, lecz jest odrbnym
szlakiem reakcji. Syntez glikogenu przeprowadzaj trzy enzymy:
1. Pirofosforylaza urydynodifosfo-glukozy (UDP-glukozy) katalizuje syntez UDP-glukozy
(zaktywowana forma glukozy) z urydynotrifosforanu (UTP) i glukozo-1-fosforanu:
UTP + glukozo-1-fosforan UDP-glukoza + PP
i
.
Powstajcy w tej reakcji pirofosforan (PP
i
) szybko ulega hydrolizie dziaaniem pirofosfatazy, wskutek
czego uwalnia si energia. UDP-glukoza powstaje natomiast dziki utworzeniu wizania estrowego
pomidzy grup hydroksylow przy atomie wgla w pozycji 1, a reszt difosforanow czsteczki UDP.
2. Syntaza glikogenowa katalizuje przeniesienie glukozy z UDP-glukozy do rosncego acucha
polisacharydowego. Reszty glukozy z UDP-glukozy doczone s do grup -OH przy atomie wgla w
pozycji 4 przy kocu nieredukujcym czsteczki glikogenu, tworzc wizania -1,4-glikozydowe.
Syntaza glikogenowa moe wydua jedynie ju istniejcy acuch. Dlatego te potrzebny jest
inicjator. Rol t spenia biako o nazwie glikogenina (m. cz. 37 kDa), ktra zawiera osiem poczonych
wizaniem -1,4-glikozydowym, reszt glikozylowych. Do tego biaka syntaza glikogenowa docza
dalsze reszty glikozylowe i tak wydua acuch. Kade ziarno glikogenu w swoim rdzeniu zawiera
jedn czsteczk glikogeniny.
3. Wizanie -1,6-glikozydowe w czsteczce glikogenu powstaje z udziaem enzymu rozgaziajcego
[amylo- (1,4 1,6) transglikozylaza]. Odbywa si to w ten sposb, e gdy pewna liczba czsteczek
glukozy zostanie ju poczona w prosty acuch cukrowy o wizaniach -1,4-glikozydowych, enzym
rozgaziajcy rozcina jedno wizanie -1,4-glikozydowe i przenosi odcinek (zazwyczaj zawierajcy
okoo 7 reszt glukozy) do bardziej wewntrznego miejsca czsteczki. Nastpnie odcinek ten jest
doczony przez wizanie -1,6-glikozydowe. Rozgazienia s wane, poniewa enzymy, ktre
rozkadaj i syntetyzuj glikogen, pracuj tylko przy kocu czsteczki glikogenu. W efekcie dziki
rozgazieniom wzrasta szybko syntezy i rozkadu glikogenu.
Regulacja metabolizmu glikogenu
Metabolizm glikogenu jest kontrolowany zarwno przez regulacj allosteryczn, jak i
hormonaln. Gdyby synteza i rozkad glikogenu miay moliwo rwnoczesnego dziaania, to efektem
8
netto byaby hydroliza UTP, w tak zwanym cyklu daremnym. Aby nie doszo do takiej sytuacji, oba
procesy musz podlega cisej kontroli. Regulacja metabolizmu glikogenu jest efektywna dziki
rwnowadze midzy aktywnociami syntazy glikogenowej i fosforylazy. Natomiast enzymy
rozgaziajcy i odgaziajcy czsteczk glikogenu nie s regulowane.
Streszczenie
W niniejszej pracy omwiono waniejsze szlaki metabolizmu wglowodanw:
- szlak glikolizy
- szlak glukoneogenezy
- tor pentozofosforanowy
- szlak rozkadu i syntezy glikogenu.
Opisano rwnie cykl kwasu cytrynowego, transport elektronw i fosforylacj oksydacyjn.
Wykaz stosowanych skrtw
acetylo-CoA acetylokoenzym-A
ADP adenozynodifosforan
ATP adenozynotrifosforan
CoA koenzym A
FAD dinukleotyd flawinoadeninowy - utleniony
FADH
2
dinunkleotyd falwinoadeninowy zredukowany
GDP guanozynodifosforan
GTP gaunozynotrifosforan
NAD
+
- dinukleotyd nikotynamidoadeninowy utleniony
NADH dinukleotyd nikotynamidoadeninowy zredukowany
P
i
fosforan nieorganiczny (ortofosforan)
PP
i
nieorganiczny pirofosforan
UDP- difosforan urydyny
UTP urydynotrifosforan
Pimiennictwo
1. Krtkie wykady biochemia B.D. Hames, N.H. Hooper, J.D. Houghton, PWN 2000
2. Biochemia L. Stryer, PWN 1997
3. Biochemia Harpera R.K. Murray, D.K. Granner, P.A. Mayes, V.W. Rodwell, Wyd. Lek. 1996
4. wiczenia z biochemii pod red. L. Kyszejko-Stefanowicz, PWN 2003
5. Biochemie und pathobiochemie G. Loffler, P. Petrides, Springer 1998
You might also like
- Bliskie Spotkania Z Biologią METABOLIZM Czesc2 PDFDocument36 pagesBliskie Spotkania Z Biologią METABOLIZM Czesc2 PDFLeneator AniśkiewiczNo ratings yet
- Metabolizm 2013Document39 pagesMetabolizm 2013Phortis44No ratings yet
- FotosyntezaDocument3 pagesFotosyntezaTomasz GrochowskiNo ratings yet
- MetabolizmDocument4 pagesMetabolizmNina WąsikNo ratings yet
- CW RozszDocument22 pagesCW RozszKarolina MarczykNo ratings yet
- Hormony Część 2Document6 pagesHormony Część 2Katarzyna NierwinskaNo ratings yet
- Przemiany Promieniotworcze Zapis RownanDocument20 pagesPrzemiany Promieniotworcze Zapis Rownanalicja szumskaNo ratings yet
- Materiał ALL NewDocument261 pagesMateriał ALL NewENo ratings yet
- 11.39 Reakcje Jadrowe Test Z Widoczna PunktacjaDocument2 pages11.39 Reakcje Jadrowe Test Z Widoczna PunktacjaEdytaNo ratings yet
- (Zadania) Reakcje RedoksDocument4 pages(Zadania) Reakcje RedoksPatrycja ŚwiniarskaNo ratings yet
- Kwasy KarboksyloweDocument42 pagesKwasy KarboksyloweAndrew LondonNo ratings yet
- 7) Rośliny NagozalążkoweDocument6 pages7) Rośliny NagozalążkoweAgnieszka KarwackaNo ratings yet
- Ważne PDFDocument38 pagesWażne PDFAnonymous 7vjENho3kNo ratings yet
- Biotechnologia I Inżynieria GenetycznaDocument6 pagesBiotechnologia I Inżynieria GenetycznaxuexueNo ratings yet
- Test BiotechnologiaDocument5 pagesTest BiotechnologiaiuwbfjcNo ratings yet
- SPRAWDZIAN - FIZYKA JĄDROWA - PytaniaDocument10 pagesSPRAWDZIAN - FIZYKA JĄDROWA - PytaniaZielonkaNo ratings yet
- Zasady MetabolizmuDocument4 pagesZasady MetabolizmuKasia SzewcNo ratings yet
- Nieorganiczna - Zestaw MaturalnyDocument8 pagesNieorganiczna - Zestaw MaturalnyKeewxNo ratings yet
- 5 NagozalążkoweDocument36 pages5 NagozalążkoweLena TyburaNo ratings yet
- Cykl MiesiączkowyDocument16 pagesCykl MiesiączkowyNatalia FlisNo ratings yet
- Cytologia - Powtórzenie 2023 W1Document2 pagesCytologia - Powtórzenie 2023 W1Polomaniac ŻubrNo ratings yet
- ElektrochemiaDocument26 pagesElektrochemiaremigiusz_kowalikNo ratings yet
- METABOLIZM cz.1 (Tematy Od 1 Do 5)Document16 pagesMETABOLIZM cz.1 (Tematy Od 1 Do 5)Katarzyna StrugałaNo ratings yet
- METABOLIZMDocument51 pagesMETABOLIZMWielokropekNo ratings yet
- Oddychanie KomórkoweDocument2 pagesOddychanie KomórkoweOlaf GrycNo ratings yet
- Metabolizm - PrzemianyDocument3 pagesMetabolizm - PrzemianyJagodaNo ratings yet
- Genetyka PCR, SangerDocument3 pagesGenetyka PCR, SangerKoperekNo ratings yet
- FotosyntezaDocument1 pageFotosyntezaEryk MalinowskiNo ratings yet
- 6 OkrytozalążkoweDocument66 pages6 OkrytozalążkoweLena TyburaNo ratings yet
- Grupa Klasa .................... Imię .................................................................................. Liczba Punktów ...... / 15 PDocument4 pagesGrupa Klasa .................... Imię .................................................................................. Liczba Punktów ...... / 15 PDarek EmekNo ratings yet
- Tkanki Roslinne-2Document72 pagesTkanki Roslinne-2WielokropekNo ratings yet
- Biochemia MMDocument10 pagesBiochemia MMMatylda MazurNo ratings yet
- Zadania Maturalne Z Biologii 3 - BiologHelpDocument13 pagesZadania Maturalne Z Biologii 3 - BiologHelpMajaNo ratings yet
- Zadania Z Genetyki Dla Liceum Zakres PodstawowyDocument1 pageZadania Z Genetyki Dla Liceum Zakres PodstawowyPiotr ŚwitalNo ratings yet
- Testy-Tom2 Odp PRDocument7 pagesTesty-Tom2 Odp PRchemik100% (1)
- Układ KrążeniaDocument2 pagesUkład KrążeniaAlicja szeligaNo ratings yet
- Egzamin AnatomiaDocument2 pagesEgzamin AnatomiaemiliaNo ratings yet
- Tkanki Roślinne I ZwierzęceDocument3 pagesTkanki Roślinne I ZwierzęceRafał100% (2)
- Odpowiedzi Do Zadan Powtorzeniowych Do Podrecznika Biologia Na Czasie 3 Zakres RozszerzonyDocument11 pagesOdpowiedzi Do Zadan Powtorzeniowych Do Podrecznika Biologia Na Czasie 3 Zakres RozszerzonyMadzia TNo ratings yet
- Ukad Krenia - PowtrzenieDocument1 pageUkad Krenia - PowtrzenieAnna KasprowiczNo ratings yet
- c73dbcd9d6facd8ed5332d91a99f904bDocument6 pagesc73dbcd9d6facd8ed5332d91a99f904bNicole HupaNo ratings yet
- Powtórzenie-Prąd Elektryczny. Test - EkowydrukDocument4 pagesPowtórzenie-Prąd Elektryczny. Test - EkowydrukMiły MiłoszNo ratings yet
- Fizyka Atomowa I Jadrowa - Elementarna Rzecz o Elementarnych Skladnikach Materii PrezentacjaDocument27 pagesFizyka Atomowa I Jadrowa - Elementarna Rzecz o Elementarnych Skladnikach Materii PrezentacjaMałgorzata Kubusiak 3gNo ratings yet
- Geny Sprzężone Z PłciąDocument3 pagesGeny Sprzężone Z PłciąJoanna CzaplińskaNo ratings yet
- Krzyzowki KrewDocument1 pageKrzyzowki KrewAdam SkwNo ratings yet
- Uk - Nerwowy - FunkcjeDocument74 pagesUk - Nerwowy - FunkcjeRobert WadlewskiNo ratings yet
- Fizjologia RoslinDocument4 pagesFizjologia RoslinAgnieszka Karwacka100% (2)
- BIOLOGIA Zbior Zadan Matura 2018 Tom 1 DEMO PDFDocument44 pagesBIOLOGIA Zbior Zadan Matura 2018 Tom 1 DEMO PDFMarkoweprodukty. SaTMNo ratings yet
- Zadania Maturalne - Mszaki, Paprotiniki, Tkanki RoślinneDocument35 pagesZadania Maturalne - Mszaki, Paprotiniki, Tkanki RoślinneJulia KuszewskaNo ratings yet
- Chemia Organiczna IIDocument13 pagesChemia Organiczna IIPaulinka3624532No ratings yet
- 02-03. Człowiek Przedsiębiorczy - Osobowość Człowieka, Postawa PrzedsiębiorczaDocument6 pages02-03. Człowiek Przedsiębiorczy - Osobowość Człowieka, Postawa Przedsiębiorczamortal3550% (2)
- Protisty - Zadania MaturalneDocument7 pagesProtisty - Zadania MaturalneMatylda KowalczukNo ratings yet
- Zadania Maturalne Z Biologii - BiologHelpDocument34 pagesZadania Maturalne Z Biologii - BiologHelpJoanna WawrzyniecNo ratings yet
- 4.Test-Oddychanie Komórkowe. Oddychanie TlenoweDocument4 pages4.Test-Oddychanie Komórkowe. Oddychanie TlenoweLeon Kubiak100% (1)
- Geny I GenomyDocument17 pagesGeny I GenomyAnna Brzuziewska100% (1)
- Metabolizm I EnzymyDocument9 pagesMetabolizm I EnzymyOla KowalskaNo ratings yet
- Bilans Energetyczny Katabolizmu Tlenowego I Beztlenowego GlukozyDocument19 pagesBilans Energetyczny Katabolizmu Tlenowego I Beztlenowego GlukozyOliwia BłaszkiewiczNo ratings yet
- Biochemia ZadaniaDocument13 pagesBiochemia Zadaniawrobelnatalia781No ratings yet
- Glikoliza - Wspolny Etap KatabolDocument16 pagesGlikoliza - Wspolny Etap KatabolWaifuNoLaifuNo ratings yet
- BIOCHEMIADocument4 pagesBIOCHEMIANatalia BoguszNo ratings yet
- SelenDocument3 pagesSelenBartoszNo ratings yet
- Aktywność Przeciwutleniająca Wybranych Owoców JagodowychDocument8 pagesAktywność Przeciwutleniająca Wybranych Owoców JagodowychBartoszNo ratings yet
- Właściwości Zdrowotne Oliwy Z OliwekDocument4 pagesWłaściwości Zdrowotne Oliwy Z OliwekBartoszNo ratings yet
- Energetyka OrganizmuDocument27 pagesEnergetyka OrganizmuBartoszNo ratings yet
- N 313 06 KroliczakDocument34 pagesN 313 06 KroliczakBartoszNo ratings yet
- AspektyDocument5 pagesAspektyBartoszNo ratings yet
- s54 Wietrzyk 1 00Document6 pagess54 Wietrzyk 1 00BartoszNo ratings yet
- 1 PBDocument6 pages1 PBBartoszNo ratings yet
- 02-09 Artykul4pDocument5 pages02-09 Artykul4pBartoszNo ratings yet
- ZW 2013 07 03Document5 pagesZW 2013 07 03BartoszNo ratings yet
- Endokrynologia Polska - 2004Document71 pagesEndokrynologia Polska - 2004Bartosz100% (1)
- Filozofia SłownikDocument28 pagesFilozofia SłownikBartosz100% (2)
- Cykl Koniunkturalny A Zmiany RKWDocument12 pagesCykl Koniunkturalny A Zmiany RKWBartoszNo ratings yet
- ZW 2013 07 03Document5 pagesZW 2013 07 03BartoszNo ratings yet
- Chirurgia Trzustki 2005Document14 pagesChirurgia Trzustki 2005BartoszNo ratings yet
- Rehabilitacja Po Rekonstrukcji W.krzyzowego PrzedniegoDocument15 pagesRehabilitacja Po Rekonstrukcji W.krzyzowego PrzedniegozwijkaNo ratings yet
- Morfologia Więzadeł Krzyżowych Stawu KolanowegoDocument6 pagesMorfologia Więzadeł Krzyżowych Stawu KolanowegoBartoszNo ratings yet
- Historia Myśli Ekonomicznej - Karol MarksDocument12 pagesHistoria Myśli Ekonomicznej - Karol MarksBartosz100% (1)
- Manual - Honda Accord 1993-'98Document1,248 pagesManual - Honda Accord 1993-'98Bartosz70% (10)
- Jak Budować Nowe Źródła Ciepła I Energii ElektrycznejDocument10 pagesJak Budować Nowe Źródła Ciepła I Energii ElektrycznejBartoszNo ratings yet
- Ebook - PL. LAO TSY - Tao Te King Czyli Księga Drogi I Cnoty. - Tao Filozofia Taoizm Chiny Historia Sztuka - Książka.KsiazkiDocument41 pagesEbook - PL. LAO TSY - Tao Te King Czyli Księga Drogi I Cnoty. - Tao Filozofia Taoizm Chiny Historia Sztuka - Książka.KsiazkiBartosz100% (5)
- Filozofia Kant - Uzasadnienie Metafizyki MoralnościDocument60 pagesFilozofia Kant - Uzasadnienie Metafizyki MoralnościBartoszNo ratings yet
- Filozofia Leibniz - MonadologiaDocument8 pagesFilozofia Leibniz - MonadologiaBartoszNo ratings yet
- Staw KolanowyDocument6 pagesStaw KolanowyBartoszNo ratings yet
- Etyka Jako FilozofiaDocument7 pagesEtyka Jako FilozofiaBartosz0% (1)
- Balcerowicz - Socjalizm Kapitalizm TransformacjaDocument223 pagesBalcerowicz - Socjalizm Kapitalizm TransformacjaBartoszNo ratings yet
- Odpowiedzi KomorkaDocument22 pagesOdpowiedzi KomorkaMarta ŁajewskaNo ratings yet
- Metabolizm - Zadania (PR)Document16 pagesMetabolizm - Zadania (PR)majaA98No ratings yet
- Klucz MetabolizmDocument16 pagesKlucz MetabolizmahaNo ratings yet
- Seminarium 2Document37 pagesSeminarium 2Ja SkNo ratings yet
- Biologia KomórkaDocument12 pagesBiologia KomórkadorNo ratings yet
- MetabolizmDocument20 pagesMetabolizmtrash11111No ratings yet
- 4.1 Podstawowe Zasady MetabolizmuDocument5 pages4.1 Podstawowe Zasady MetabolizmuDominik BudniakNo ratings yet
- Histologia Dla KosmetologówDocument166 pagesHistologia Dla KosmetologówKamilaNo ratings yet
- Glukoneogeneza I GlikogenolizaDocument17 pagesGlukoneogeneza I GlikogenolizaWaifuNoLaifuNo ratings yet
- neuron 2022Document23 pagesneuron 2022Katarzyna KowalczykNo ratings yet
- PM2015 Biologia ArkuszDocument16 pagesPM2015 Biologia Arkusznever mindNo ratings yet
- Karty Pracy Ucznia CZ 1 Klucz OdpowiedziDocument23 pagesKarty Pracy Ucznia CZ 1 Klucz OdpowiedziAgnieszka Magdalena Rentflejsz80% (5)
- Powtórzyć Testy Z Klasy I (Bakterie, Tkanki, Organy Udział W Odżywianiu) !Document10 pagesPowtórzyć Testy Z Klasy I (Bakterie, Tkanki, Organy Udział W Odżywianiu) !Dominik WoleńNo ratings yet