Professional Documents
Culture Documents
Producción y usos del ácido sulfúrico
Uploaded by
SantiagoAlcantaraOriginal Description:
Original Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Producción y usos del ácido sulfúrico
Uploaded by
SantiagoAlcantaraCopyright:
Available Formats
http://www.100ciaquimica.net/temas/tema11/punto7b.
htm
http://www.indec.cl/man_asp.html
http://html.rincondelvago.com/acido-sulfurico_3.html
http://www.fisicanet.com.ar/quimica/inorganica/ap01_acido_sulfurico.php
http://www.textoscientificos.com/sulfurico/produccion
http://www.textoscientificos.com/sulfurico/introduccion
http://www.sc.ehu.es/iawfemaf/archivos/materia/01415.htm
http://es.slideshare.net/EmilioOvando/produccion-acido-sulfurico
http://webdelprofesor.ula.ve/ingenieria/marquezronald/wpcontent/uploads/2009/08/Quimica-Industrial-II-Acido-Sulfurico.pdf
http://es.slideshare.net/yormanzambrano/industria-del-cido-sulfrico
https://procesoacidosulfurico.wikispaces.com/Proceso+de+Acido+Sulfurico
http://foundrynews.com.br/upload/artigos/acido-sulfurico-tostacion-deblenda512de820e4d78.pdf
El cido sulfrico (H2SO4) es un compuesto qumico corrosivo que cuenta
con la propiedad de ser fuertemente cido y contar con un gran poder
deshidratante. Es un producto qumico de origen industrial, derivado del
azufre, el cido sulfrico cuenta con diversas aplicaciones en la industria . siendo su
uso ms importante la utilizacin como insumo en la produccin de fertilizantes. otros
usos en procesos de la industria de refinacin del petrleo, la petroqumica y qumica,
siderurgia, minera, textiles, curtiembres, alimentos, generacin de energa,
potabilizacin de agua para consumo humano, etc.
es llamado aceite de vitriolo, cido de bateras y cido de fertilizantes.
El cido sulfrico es un lquido viscoso, de densidad 1,83 g/ml,
transparente e incoloro cuando se encuentra en estado puro, y de
color marrn cuando contiene impurezas. Es un cido fuerte que,
cuando se calienta por encima de 30C desprende vapores y por
encima de 200C emite trixido de azufre.
Los consumidores ms importantes son los productores de cido fosfrico (sector
agroqumico).
Los consumidores ms importantes son los productores de cido fosfrico (sector
agroqumico). Sin embargo, es tambin usado ampliamente en la produccin de sales
sulfatadas, celofn, rayn, detergentes, cido clorhdrico, cido ntrico, tintes,
pigmentos, explosivos, refinacin de petrleo, en la produccin de bateras para
vehculos, en el tratamiento de agua industrial, y en el blanqueado de minerales.
Tambin se utiliza en la industria metalrgica y minera, tanto en los procesos de
purificacin o refinacin (cobre, zinc, etc.) como en tratamientos de eliminacin de
impurezas (decapado).
En el mercado mundial existen fundamentalmente dos tipos de cido sulfrico: cido
sulfrico puro o virgen y cido sulfrico impuro o residual.
La obtencin del cido sulfrico se realiza a partir del SO 2, ste se
oxida a SO3 y luego se obtiene cido sulfrico por reaccin con el agua.
En la actualidad hay dos variantes para la
obtencin del trixido de azufre (proceso
lento), denominadas el mtodo de contacto y
el mtodo de las cmaras de plomo. El
primero es ms caro pero produce cido
sulfrico muy concentrado (95%) y de elevada
pureza. El segundo es ms econmico, tiene
mayor capacidad de produccin, pero el cido
sulfrico obtenido es de menor concentracin
(70%) y de menor pureza.
En ambos mtodos, se parte del dixido de
azufre previamente obtenido (a partir de la
tostacin de la pirita) y se oxida a trixido de
azufre utilizando un catalizador. El mtodo de
contacto necesita un trixido de azufre muy
puro para no envenenar el catalizador que
suele ser arsnico u xido de hierro, y es por
esta razn por lo que resulta ms caro.
El trixido de azufre obtenido, se enfra y se
hace pasar por una torre de absorcin donde
se combina con cido sulfrico concentrado
formndose el cido pirosulfrico:
H2SO4 + SO3
H2S2O7
que luego se descompone por accin del agua
segn la reaccin:
H2S2O7 + H2O
2 H2SO4
No es conveniente mezclar directamente el
trixido de azufre sobre agua para obtener el
cido sulfrico segn la reaccin:
SO3 + H2O
H2SO4
porque en dicha reaccin se desprende muchsima energa, haciendo que la
mayor parte del trixido de azufre se volatilice sin reaccionar para formar el
cido sulfrico.
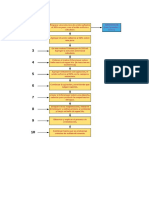
Caracteristicas del reactor
You might also like
- 14-Planta de Produccion de Ácido SulfúricoDocument3 pages14-Planta de Produccion de Ácido SulfúricoCaro Villa MoraNo ratings yet
- Ácido SulfúricoDocument20 pagesÁcido SulfúricoAlexandra ArroyoNo ratings yet
- El Ácido SulfúricoDocument3 pagesEl Ácido SulfúricoMarina Patón AriasNo ratings yet
- INORGANICA (1)Document6 pagesINORGANICA (1)Dayanne Nicoll Guerrero AstohuamanNo ratings yet
- ProcesoDocument2 pagesProcesoEdher Tueros YaceNo ratings yet
- Gerardo SulfuricoDocument7 pagesGerardo SulfuricoDevolep BabariaNo ratings yet
- Ácido SulfúricoDocument4 pagesÁcido SulfúricoEdison Javier BarraganNo ratings yet
- Ácido SulfúricoDocument4 pagesÁcido SulfúricoEdison Javier BarraganNo ratings yet
- Acido Sulfúrico en IndustriasDocument5 pagesAcido Sulfúrico en IndustriasSebastian Martinez BadilloNo ratings yet
- Acido SulfúricoDocument14 pagesAcido SulfúricoKarina GutierrezNo ratings yet
- PROYETO FINAL Acido Sulfurico Mejorado 20 Junio 2017Document70 pagesPROYETO FINAL Acido Sulfurico Mejorado 20 Junio 2017alitha50% (2)
- Acido SulfuricoDocument13 pagesAcido SulfuricoHemily CalderaNo ratings yet
- Aca 2 Fundamentos de QuimicaDocument8 pagesAca 2 Fundamentos de QuimicaURIEL GÓMEZ GÓMEZNo ratings yet
- Acido CitricoDocument417 pagesAcido CitricoAndres PluasNo ratings yet
- Acido SulfuricoDocument6 pagesAcido SulfuricoFabian FlorezNo ratings yet
- Produccion Del Acido Sulfurico YulyDocument6 pagesProduccion Del Acido Sulfurico YulyAlexandra ArroyoNo ratings yet
- Análisis Energético de Un Proceso Industrial de Producción de Ácido SulfúricoDocument5 pagesAnálisis Energético de Un Proceso Industrial de Producción de Ácido SulfúricoLaura Torres BarbaNo ratings yet
- Producción Del Ácido Fosfórico (Industria Química) : Proceso 1Document68 pagesProducción Del Ácido Fosfórico (Industria Química) : Proceso 1Jeff Rojas AncietaNo ratings yet
- Proyecto de QuimicaDocument27 pagesProyecto de QuimicaAnonymous f0mbEisntaNo ratings yet
- Obtencion IndustrialDocument10 pagesObtencion IndustrialHerrera Jose ManuelNo ratings yet
- Obtencion de Acido Sulfurico Concentrado A Menor ConcentracionDocument6 pagesObtencion de Acido Sulfurico Concentrado A Menor ConcentracionCarlos Alberto Caicedo MoreiraNo ratings yet
- Producción y usos del ácido sulfúricoDocument24 pagesProducción y usos del ácido sulfúricoAna CampoverdeNo ratings yet
- Visita a empresas químicas básicas en Caloto y ManizalesDocument15 pagesVisita a empresas químicas básicas en Caloto y ManizalesjhoajoNo ratings yet
- Ácido sulfúrico: producción, usos e importancia de este compuesto químicoDocument4 pagesÁcido sulfúrico: producción, usos e importancia de este compuesto químicoMelissa PaezNo ratings yet
- Practica 3 ShampooDocument16 pagesPractica 3 ShampooJuan CarlosNo ratings yet
- Acido Citrico MMMDocument417 pagesAcido Citrico MMMPilar Drm100% (1)
- Acido Sulfurico 1Document22 pagesAcido Sulfurico 1FernandoRoblesNo ratings yet
- Acido FulfuricoDocument10 pagesAcido FulfuricoElard Dennis TorresNo ratings yet
- Proceso lixiviación cobre planta MetakavDocument21 pagesProceso lixiviación cobre planta MetakavCarmen VillasanteNo ratings yet
- Obtencion de Acido Citrico a Partir de Melaza DocxDocument15 pagesObtencion de Acido Citrico a Partir de Melaza Docxadelendatti1No ratings yet
- Importancia Industrial y Económica Del Proceso CloroDocument7 pagesImportancia Industrial y Económica Del Proceso CloroKrakón PuenteNo ratings yet
- Obtención Del Ácido SulfúricoDocument14 pagesObtención Del Ácido SulfúricoFernanda Del Carmen Alegre GongoraNo ratings yet
- Tarea Quimica SO2-1Document6 pagesTarea Quimica SO2-1eziomortalNo ratings yet
- Quimica Ácido Sulfúrico CunDocument1 pageQuimica Ácido Sulfúrico CunSTEFFANNY VASQUEZ CUELLARNo ratings yet
- Acido SulfuricoDocument39 pagesAcido Sulfuricoalejo-acosta-castro-9272No ratings yet
- ÁCIDO SULFÚRICO.. TrabajoDocument38 pagesÁCIDO SULFÚRICO.. Trabajoadrianaemilys0% (2)
- PRACTICA No. 2 Obtención de Un Shampoo Liquido Por Sulfatación Del Alcohol LauricoDocument23 pagesPRACTICA No. 2 Obtención de Un Shampoo Liquido Por Sulfatación Del Alcohol LauricoRodrigo Rodriguez100% (1)
- Produccion de Acido SulfuricoDocument36 pagesProduccion de Acido SulfuricoAlejandra QuintinNo ratings yet
- Practica N2 de Laboratorio de Quimica Grupo 5Document5 pagesPractica N2 de Laboratorio de Quimica Grupo 5Joaquin AltamiranoNo ratings yet
- Industria Del Acido Sulfurico2 Final-1Document29 pagesIndustria Del Acido Sulfurico2 Final-1Carlos BustamanteNo ratings yet
- Recursos 2do ParcialDocument17 pagesRecursos 2do ParcialDavid LeonNo ratings yet
- Manejo de Acido SulfuricoDocument53 pagesManejo de Acido SulfuricoJaime PalaciosNo ratings yet
- Acido SulfuricoDocument18 pagesAcido SulfuricoLeidy Viviana Calvo ArenasNo ratings yet
- Clase 7-Ácido CítricoDocument17 pagesClase 7-Ácido CítricoWILSON DAVID RODRIGUEZ HERRERANo ratings yet
- Producción de ácido sulfúricoDocument32 pagesProducción de ácido sulfúricoRogelio RdNo ratings yet
- Guía ácido sulfúrico seguridad almacenamiento transporteDocument25 pagesGuía ácido sulfúrico seguridad almacenamiento transporteGonzalo Urrutia0% (1)
- ObtenciónDeÁcidoSulfúrico LosFernandoConcha CortesChacanaVillablancaDocument16 pagesObtenciónDeÁcidoSulfúrico LosFernandoConcha CortesChacanaVillablancaMartín Villablanca100% (1)
- Tarea #03 PisDocument15 pagesTarea #03 PisPIERO MATIAS HERRERA SUAREZNo ratings yet
- Trabajo Termo EcuacionDocument15 pagesTrabajo Termo EcuacionALEXANDRA BELOT CALLA MARQUEZNo ratings yet
- Taller 3Document5 pagesTaller 3DAVIDNo ratings yet
- Producción de ácido sulfúricoDocument12 pagesProducción de ácido sulfúricoKaren CeuraNo ratings yet
- Síntesis H2SO4 a partir SDocument3 pagesSíntesis H2SO4 a partir SJesus PerezNo ratings yet
- Obtención de sulfato de amonioDocument5 pagesObtención de sulfato de amonioKevin Soller CardenasNo ratings yet
- Trabajo Termo Ecuacion OficialDocument15 pagesTrabajo Termo Ecuacion OficialUna Universitaria másNo ratings yet
- Proceso innovador para producir carbonato de sodio y ácido sulfúrico a partir de sulfatoDocument10 pagesProceso innovador para producir carbonato de sodio y ácido sulfúrico a partir de sulfatoNaidelin Paola Calle MorochoNo ratings yet
- Fermentadores para Cultivo SumergidoDocument3 pagesFermentadores para Cultivo SumergidowendyNo ratings yet
- NEO-22 Acido Sulfúrico - Almacenamiento - Carguío - Transporte - Descarga.Document36 pagesNEO-22 Acido Sulfúrico - Almacenamiento - Carguío - Transporte - Descarga.Paulo Diego Aguilera100% (2)
- Ácido sulfúrico: perfiles de conversión y temperaturaDocument11 pagesÁcido sulfúrico: perfiles de conversión y temperaturaFio LuciaNo ratings yet
- UF1720 - Organización y gestión de las operaciones de conformado y secado de productos cerámicosFrom EverandUF1720 - Organización y gestión de las operaciones de conformado y secado de productos cerámicosNo ratings yet
- Lavado y colmatado de tapones de corcho. MAMA0109From EverandLavado y colmatado de tapones de corcho. MAMA0109No ratings yet
- Como Instalar ManimDocument2 pagesComo Instalar ManimSantiagoAlcantaraNo ratings yet
- Caída de Presión y Pérdida de CargaDocument4 pagesCaída de Presión y Pérdida de CargaSantiagoAlcantaraNo ratings yet
- 1 Domingo de ResurreccionDocument2 pages1 Domingo de ResurreccionSantiagoAlcantaraNo ratings yet
- Ejercicio 10.9Document4 pagesEjercicio 10.9SantiagoAlcantaraNo ratings yet
- Carbon ActivadoDocument1 pageCarbon ActivadoSantiagoAlcantaraNo ratings yet
- Trabajo de CondensadorDocument2 pagesTrabajo de CondensadorSantiagoAlcantaraNo ratings yet
- Presentacion Metodos NumericosDocument9 pagesPresentacion Metodos NumericosSantiagoAlcantaraNo ratings yet
- Keys of The Vip 1-4Document1 pageKeys of The Vip 1-4SantiagoAlcantaraNo ratings yet
- Misa para Cantar en BaniDocument5 pagesMisa para Cantar en BaniSantiagoAlcantaraNo ratings yet
- Espectroscopia de Absorción Atómica y de LlamaDocument7 pagesEspectroscopia de Absorción Atómica y de LlamaSantiagoAlcantaraNo ratings yet
- Clase de Regresion ExcelDocument10 pagesClase de Regresion ExcelJhonyPerezNo ratings yet
- 1 Domingo de ResurreccionDocument2 pages1 Domingo de ResurreccionSantiagoAlcantaraNo ratings yet
- Sy MB Ola B: PasosDocument6 pagesSy MB Ola B: PasosSantiagoAlcantaraNo ratings yet
- Ejercicio 10.2 RegresionDocument6 pagesEjercicio 10.2 RegresionSantiagoAlcantaraNo ratings yet
- Ejercicios Metodos Numericos FinalDocument21 pagesEjercicios Metodos Numericos FinalSantiagoAlcantaraNo ratings yet
- Ali MentosDocument1 pageAli MentosSantiagoAlcantaraNo ratings yet
- Propiedades Del CarbonDocument2 pagesPropiedades Del CarbonSantiagoAlcantaraNo ratings yet
- Habitos Que Evitan Los RícosDocument1 pageHabitos Que Evitan Los RícosSantiagoAlcantaraNo ratings yet
- SelectionDocument4 pagesSelectionSantiagoAlcantaraNo ratings yet
- Sy MB Ola B: PasosDocument5 pagesSy MB Ola B: PasosSantiagoAlcantaraNo ratings yet
- Primer Domingo de AdvientoDocument1 pagePrimer Domingo de AdvientoSantiagoAlcantaraNo ratings yet
- 66 2.3 Por PartesDocument1 page66 2.3 Por PartesSantiagoAlcantaraNo ratings yet
- Queda Revelado Ante La Verdad de La EscrituraDocument6 pagesQueda Revelado Ante La Verdad de La EscrituraSantiagoAlcantaraNo ratings yet
- Adsorción ResumenDocument4 pagesAdsorción ResumenSantiagoAlcantaraNo ratings yet
- Estudio BiblicoDocument46 pagesEstudio BiblicoSantiagoAlcantaraNo ratings yet
- Analisis Vectorial y TensorialDocument22 pagesAnalisis Vectorial y TensorialSantiagoAlcantaraNo ratings yet
- Estudio BiblicoDocument46 pagesEstudio BiblicoSantiagoAlcantaraNo ratings yet
- Calificaciones de Ingenieria QuimicaDocument5 pagesCalificaciones de Ingenieria QuimicaSantiagoAlcantaraNo ratings yet
- Desarrollo SostenibleDocument11 pagesDesarrollo SostenibleSantiagoAlcantaraNo ratings yet
- Trabajo Final Piña Colada en Polvo InstantaneaDocument29 pagesTrabajo Final Piña Colada en Polvo InstantaneaSantiagoAlcantaraNo ratings yet
- Recuperacion de OroDocument14 pagesRecuperacion de OroJohana AracellyNo ratings yet
- Diapositivas Del AzufreDocument14 pagesDiapositivas Del AzufreEnmanuel RaveloNo ratings yet
- Captación y Reutilización Del Agua de Lluvia y Más Info.Document11 pagesCaptación y Reutilización Del Agua de Lluvia y Más Info.Lisandro BarembergNo ratings yet
- Mendoza Gualito Edgar FranciscoDocument95 pagesMendoza Gualito Edgar FranciscoMarco Antonio Calle VillaNo ratings yet
- Sal de AlumbreDocument5 pagesSal de AlumbreLAURA ALEJANDRA LOPEZ ERAZONo ratings yet
- ColorantesDocument8 pagesColorantesMyriamNo ratings yet
- Biotecnologia en La Industria de La Mineria y PetroleoDocument23 pagesBiotecnologia en La Industria de La Mineria y PetroleojoseNo ratings yet
- Practica 5 Acido SulfanílicoDocument9 pagesPractica 5 Acido SulfanílicoJavier Vargas Ornelas100% (1)
- Guía Didáctica Unidad 6. Tema 1 - Propiedades Físico QuímicasDocument76 pagesGuía Didáctica Unidad 6. Tema 1 - Propiedades Físico QuímicasISRAEL RIOSNo ratings yet
- Reacciones químicasDocument6 pagesReacciones químicasmartin menoscalNo ratings yet
- ESTEQUIOMETRIA EjerciciosDocument2 pagesESTEQUIOMETRIA EjerciciosvikyNo ratings yet
- Biorremediacion de Lodos Petroquimicos Mediante El Uso de La Biota Microbiana Autoctona en Un Oxisol Del Municipio Lagunillas Del Estado Zulia VenezuelaDocument8 pagesBiorremediacion de Lodos Petroquimicos Mediante El Uso de La Biota Microbiana Autoctona en Un Oxisol Del Municipio Lagunillas Del Estado Zulia VenezuelaPenelope MeloNo ratings yet
- Hoja de Resumen de Seguridad para El Transporte Terrestre de Materiales y Residuos PeligrososDocument38 pagesHoja de Resumen de Seguridad para El Transporte Terrestre de Materiales y Residuos PeligrososCesar SarayasiNo ratings yet
- Lauril Eter Sulfato de Sodio (Final)Document16 pagesLauril Eter Sulfato de Sodio (Final)Ronny Prieto Gonzalez100% (1)
- Formación de oxácidosDocument11 pagesFormación de oxácidosGabrielNo ratings yet
- Patente Europea Dioxido de CloroDocument8 pagesPatente Europea Dioxido de CloroCM JulioNo ratings yet
- Reacciones Químicas LaboratorioDocument3 pagesReacciones Químicas LaboratorioLeydy Sullcaray HNo ratings yet
- Informe de Metalurgia Del ZincDocument19 pagesInforme de Metalurgia Del ZincIngrid Espiritu BastidasNo ratings yet
- RGM 002Document588 pagesRGM 002ABDUSKAÑ PAL0M0No ratings yet
- Lixiviacion CajamarquillaDocument16 pagesLixiviacion Cajamarquillaclucero9No ratings yet
- S 5 Q1109 (12-2)Document9 pagesS 5 Q1109 (12-2)Diego de la CabadaNo ratings yet
- Técnicas de preparación y análisis de muestras químicasDocument2 pagesTécnicas de preparación y análisis de muestras químicasSof Romero100% (1)
- SaponinasDocument7 pagesSaponinasCarmen Marisol Rufino SegoviaNo ratings yet
- Síntesis de Ácido AcetilsalicílicoDocument3 pagesSíntesis de Ácido AcetilsalicílicoMaar IvaniNo ratings yet
- Taller de Reapaso Tabla y ConfiguracionDocument5 pagesTaller de Reapaso Tabla y ConfiguracionJuan Sebastian Elvira GiraldoNo ratings yet
- SUNAT - Relacion de Subpartida NacionalDocument132 pagesSUNAT - Relacion de Subpartida NacionalMicado Tineo CamposNo ratings yet
- P1 Cuestionario Del LaboratorioDocument7 pagesP1 Cuestionario Del LaboratorioLight YagamiNo ratings yet
- Fabricación de Dulces EstramboticosDocument7 pagesFabricación de Dulces EstramboticosMoises Valdivia BaldomeroNo ratings yet
- PROPIEDADES FISICOQUIMICAS DEL AGUA InformeDocument12 pagesPROPIEDADES FISICOQUIMICAS DEL AGUA InformeAndrea OsunaNo ratings yet
- Problemario 1Document6 pagesProblemario 1lightninfire0% (1)