Professional Documents
Culture Documents
Ensayos de Valoración de Medicamentos
Uploaded by
Lili Vera RieraOriginal Description:
Original Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Ensayos de Valoración de Medicamentos
Uploaded by
Lili Vera RieraCopyright:
Available Formats
Guas de problemas 1 - 10
Anexos
Hojas para traer al parcial
Gua de
problemas
Control de Calidad de
Medicamentos
2016
CONTROL DE CALIDAD DE MEDICAMENTOS
Docentes 2016
Pablo Quiroga [PT]
Mara Esperanza Ruiz [PA]
Susana Gmez [AD]
Claudia Marano [AD]
Anala Nolasco [AD]
Patricia Retaco [AD]
Sebastin Scioli Montoto [AD]
Luisina Rivera [AD prestacin]
Marianela Rohrer [Colaboradora]
INDICE
Pg.
1. Ensayo de Valoracin ...........................................
2. Determinacin de agua........
3. Validacin de mtodos analticos............
11
4. Espectroscopa UV-Visible........
21
5. Mtodos volumtricos y anlisis funcional ........
27
6. Cromatografa en capa fina (TLC)...........
31
7. Ensayo de disolucin........
37
8. Uniformidad de unidades de dosificacin (UUD).......
43
9. HPLC..........
47
10. Estabilidad.........
55
Anexo I. Calibracin de Equipos........
59
Problemas de Aplicacin..........
65
Anexo II. UUD.........
69
Hojas para traer al parcial..........
73
CONTROL DE CALIDAD DE MEDICAMENTOS ENSAYO DE VALORACIN
1. ENSAYO DE VALORACIN
PROBLEMA 1
Estndar Externo, mtodo unipuntual
En un laboratorio de control de calidad se procede a valorar por espectrofotometra UV-Visible un lote de
comprimidos con la siguiente composicin:
Pa .150 mg
Excip. csp.600 mg
Especificacin: los comprimidos deben contener 90,0 110,0% del valor declarado de pa.
Preparacin de la solucin de la Sustancia de Referencia (SR): se pesan 16,5 mg de SR de pa (98,5% sdtc), se
disuelven en 25 ml de agua y se realiza una dilucin 1:25 con el mismo solvente, la Absorbancia a 245 nm fue de
0,561.
Preparacin de la muestra de comprimidos: se pesan individualmente 10 comprimidos (pesos: 602,1 603,1
599,7 600,0 601,0 603,4 601,6 592,1 599,5 603,1 mg), a partir de los mismos se realiza un pool y se
pesan tres alcuotas de polvo que contengan una cantidad equivalente a 150 mg del pa, respectivamente, se
trasvasa cada alcuota a matraz de 100 ml y se completa a volumen con agua, se agita durante 10 minutos, se
centrifuga y a partir del sobrenadante se mide 1 ml, se lleva a 50 ml con dicho solvente y se lee la Absorbancia a
245 nm. Resultados:
Peso Alcuota (mg)
603,5
602,1
602,3
Absorbancia (245 nm)
0,653
0,651
0,656
a. Calcula la concentracin de la SR (en g/ml)
b. Calcula la cantidad (en masa o concentracin) de pa terica (segn el valor declarado) en cada alcuota, y
luego la hallada experimentalmente, en las mismas unidades.
c. De acuerdo a los resultados obtenidos, cumple el lote de comprimidos con la especificacin?
d. En un ensayo posterior, el analista valora 10 comprimidos en forma individual, siguiendo el mismo protocolo
anteriormente descripto. Los resultados que obtuvo para tres de ellos fueron:
Peso Comprimido (mg)
597,2
603,5
600,4
Absorbancia (245 nm)
0,614
0,648
0,688
e. Calcula el contenido en cada uno de los tres comprimidos, cul es la principal diferencia de clculo que notas
entre valoraciones a partir de un pool respecto a las valoraciones de unidades individuales?
PROBLEMA 2
Ejemplo de un pa que se formula como sal
Para cuantificar el principio activo presente en la siguiente especialidad medicinal (cpsulas) se utiliza un mtodo
UV en medio acuoso.
1
CONTROL DE CALIDAD DE MEDICAMENTOS ENSAYO DE VALORACIN
Pantoprazol (Na.1 H2O)..40 mg
Excip. csp....150 mg
C16H14F2N3O4S
C16H14F2N3O4SNa . 1 H2O
PM: 382,37
PM: 432,37
Especificacin: El contenido de C16H14F2N3O4S en las capsulas debe encontrarse entre 90,0 110,0% SVD
Los pesos de polvo contenido en 10 cpsulas fueron los siguientes: 152,0 - 149,3 - 150,6 - 149,6 - 151,2 - 150,6 149,2 - 151,2 - 150,9 - 149,7 mg
Preparacin de la solucin de la Sustancia de Referencia (SR): 16,8 mg de SR (C16H14F2N3O4SNa. 1 H2O) de pureza
94,6% sdtc se disuelven en 100 ml de agua y se realiza una dilucin 1:10 siendo el valor de la Absorbancia a 260 nm
= 0,452
Preparacin de las muestras: Cada una de las alcuotas pesadas se coloc en un matraz de 50 ml al que se
agregaron 40 ml de agua destilada, se sonic durante 15 minutos, se complet a volumen con el mismo medio,
se centrifug una porcin de cada muestra y se realiz una dilucin 1:50 a partir del sobrenadante, leyndose la
Absorbancia a 260 nm.
Los resultados obtenidos se muestran en la tabla a continuacin:
a.
b.
Alcuota (mg)
Absorbancia (260 nm)
144,6
0,496
144,8
0,500
132,0
0,451
Por qu crees que en la frmula cuali-cuanti de la especialidad el anin y el agua se encuentran entre
parntesis? A qu especie qumica corresponden los 40 mg?
Cumple la especialidad con las especificaciones?
Nota: en general, hay dos maneras de resolver este tipo de problemas. Lo importante es la coherencia: como la
especificacin, al igual que la dosis, est expresada como base (es decir, sin el anin ni el agua), los resultados
finales deben estar expresados de la misma manera. Para lograrlo, se puede:
Convertir el ttulo de la SR al inicio del problema, de esa forma la cantidad hallada ser de base (porque se calcula
empleando esa SR), y se puede relacionar directamente con la dosis que tambin es de base
Convertir la dosis (40 mg) a su equivalente con el anin y el agua, y trabajar con el ttulo de la SR sin convertir.
Pero en ese caso los resultados finales debern ser convertidos a base para cotejarlos con la especificacin.
PROBLEMA 3
Otro ejemplo de un pa que se formula como sal
En un laboratorio de control de calidad se procede a valorar por espectrofotometra UV-Visible un lote de cpsulas
con la siguiente frmula:
Amantadina HCl ..100 mg
Excip. csp.250 mg
Especificacin: 95,0 105,0% de la cantidad declarada como Amantadina HCl.
Preparacin de la solucin de la SR: se pesan 49,7 mg de SR de Amantida HCl (97,6% sdtc), se disuelven en 50 ml
de metanol y se realiza una dilucin 1:25 con el mismo solvente, la Absorbancia a = 312 nm fue de 0,378.
CONTROL DE CALIDAD DE MEDICAMENTOS ENSAYO DE VALORACIN
Preparacin de la muestra de comprimidos: se pesa individualmente el contenido de 10 cpsulas (pesos: 251,3
244,6 257,2 250,8 258,4 249,3 248,1 253,1 252,4 255,8 mg), a partir de los mismos se realiza un pool y
se pesan tres alcuotas de polvo que contengan una cantidad equivalente a 100 mg del pa, respectivamente, se
trasvasa cada alcuota a matraz de 100 ml y se completa a volumen con metanol, se agita durante 10 minutos, se
centrifuga, a partir del sobrenadante se realiza una dilucin 2:50 con el mismo solvente y se lee la absorbancia a
312 nm. Resultados:
Peso Alcuota (mg)
Absorbancia (312 nm)
240,3
239,6
242,5
0,365
0,372
0,37
a. De acuerdo a los resultados, crees que el lote de cpsulas analizado cumple con la especificacin?
b. Compara este problema con el anterior. Notas las diferencias?
PROBLEMA 4
Ejemplo de clculos de volumetra
Un analista debe valorar la siguiente materia prima (MP) que posteriormente utilizar para elaborar una
especialidad medicinal. La MP tiene un grupo cido y un PM de 144,21, por lo que decide utilizar una volumetra
cido-base en medio no acuoso, empleando Hidrxido de Tetrabutilamonio (HTBA) como solucin valorante.
Procedimiento
1. Para asignarle un ttulo a la solucin de HTBA la misma se estandariza el mismo da contra un patrn primario
(cido Benzoico, PM=122) disuelto en dimetilformamida, determinndose el punto final con azul de timol.
Resultados en Tabla 1.
2. Para valorar la MP, se pesan exactamente 5 alcuotas de MP, se disuelven en 100 ml de acetona, y se titula
cada alcuota con la solucin de HTBA del punto anterior, con deteccin potenciomtrica del punto final. Se
realiza un blanco con acetona.
Resultados:
a.
b.
Tabla 1
cido Benzoico (mg)
Vol. de HTBA (ml)
302,5
304,6
300,8
306,9
Blanco
20,3
20,6
20,5
20,8
0,1
Tabla 2
Alcuota de MP (mg)
207,0
204,1
207,5
211,3
209,8
Blanco
Vol. de HTBA (ml)
11,5
11,4
11,6
11,8
11,7
0,20
Calcula el ttulo del reactivo valorante (media y SD).
Calcula el ttulo de la materia prima.
PROBLEMA 5
Estndar Externo, con curva de calibracin
Se desea realizar la valoracin de comprimidos de Atenolol 50 mg. Para ello se emplea la siguiente tcnica
adaptada a partir de la que se encuentra en la BP 2013:
3
CONTROL DE CALIDAD DE MEDICAMENTOS ENSAYO DE VALORACIN
Procedimiento: Pulverizar 20 comprimidos. Transferir una alcuota equivalente a 100 mg de Atenolol a un matraz
de 100 ml utilizando alrededor de 60 ml de metanol, calentar la suspensin resultante a 60 C y agitar durante 15
minutos. Enfriar, diluir a 100 ml con metanol, y filtrar. Tomar 1 ml del filtrado y llevar a 10 ml con metanol en un
matraz aforado. Medir la absorbancia de la solucin resultante a 275 nm.
Se prepararon tres muestras independientes a partir del pulverizado de 20 comprimidos, los cuales tenan un
peso medio de 124,3 mg. Por otro lado, se realiz una curva de calibracin con soluciones de Atenolol (Sustancia
de Referencia, 99,7% stdc) en metanol. Resultados:
Curva de calibracin
Concentracin (mg/ml) Abs (275 nm)
0,0284
0,186
0,0551
0,364
0,0854
0,583
0,1106
0,751
0,1293
0,897
a.
Muestras
Peso alcuota (mg) Abs (275 nm)
250,1
248,8
249,6
0,688
0,674
0,691
Si la farmacopea establece que el contenido de los comprimidos debe estar dentro del 92,5 - 107,5% del
valor declarado, cumple el lote analizado con dicha especificacin?
PROBLEMA 6
Estndar Interno
En un laboratorio de Control de Calidad se debe valorar materia prima de cido Flico (AF). La tcnica codificada
en la farmacopea (FA 7) es la siguiente:
Sistema Cromatogrfico: Columna RP-18, 4,0 x 25 mm, flujo 1,2 ml/min, deteccin a 280 nm.
Fase Mvil (FM): Transferir 2,0 g de fosfato monobsico de potasio a un matraz aforado de 1 litro y disolver en
aproximadamente 650 ml de agua. Agregar 15,0 ml de solucin de hidrxido de tetrabutilamonio 0,5 M en
metanol, 7,0 ml de cido fosfrico 3 N y 270 ml de metanol. Enfriar a temperatura ambiente y ajustar a pH 5,0 con
cido fosfrico 3 N o con hidrxido de amonio 6 N. Completar a volumen con agua, mezclar y filtrar.
Solucin del estndar interno (SI): Disolver aproximadamente 50 mg de metilparabeno en 1,0 ml de metanol,
diluir a 25,0 ml con fase mvil y mezclar.
Preparacin estndar: Pesar exactamente alrededor de 100 mg de AF-SR (97,45% stdc), transferir a un matraz de
100 ml y llevar a volumen con FM. Transferir 4,0 ml de dicha solucin a un matraz de 50 ml, agregar 4,0 ml de SI,
completar a volumen con FM y mezclar.
Preparacin muestra: Pesar exactamente alrededor de 100 mg de AF, transferir a un matraz de 100 ml y agregar
40 ml de FM y 1 ml de hidrxido de amonio al 10%. Completar a volumen con FM y mezclar. Transferir 4,0 ml de
dicha solucin a un matraz de 50 ml, agregar 4,0 ml de SI, completar a volumen con FM y mezclar.
Procedimiento: Inyectar por separado en el cromatgrafo volmenes iguales de la Preparacin estndar y la
Preparacin muestra, registrar los cromatogramas y medir las respuestas de los picos principales. Calcular la
cantidad de AF en las muestras ensayadas.
Peso
rea AF
rea SI
Muestra
1
101,5
21569
28247
Trabajando por cuatriplicado, se obtuvieron los siguientes
Muestra 2
100,8
24058
31586
resultados:
Muestra 3
99,9
24856
32145
Muestra 4
100,6
23874
30874
Estndar
99,3
23058
31328
CONTROL DE CALIDAD DE MEDICAMENTOS ENSAYO DE VALORACIN
a.
b.
Realiza los clculos segn el mtodo del estndar interno. Cul es el ttulo de la materia prima analizada?
Informa la media de las cuatro muestras y el coeficiente de variacin.
Repite los mismos clculos pero sin tener en cuenta el SI (como si fuera el mtodo del estndar externo) y
compralos con los del inciso a.
PROBLEMA 7
Normalizacin Interna
Como parte del control de calidad de ampollas conteniendo solucin inyectable de Dipiridamol (10 mg/ 2 ml), se
realiza el ensayo de pureza cromatogrfica (USP 34). El mismo se realiza por HPLC segn:
Sistema Cromatogrfico: Columna RP-18, 3,9 x 30 mm, flujo 1 ml/min, deteccin a 276 nm.
Fase Mvil: mezcla filtrada y desgasificada de Metanol y buffer Acetato de Sodio (6,8 mg/ml, pH=5,1) (65:35)
Solucin de prueba: transferir un volumen de la solucin inyectable medido con exactitud, que equivalga
aproximadamente a 25 mg de dipiridamol, a un matraz de 25 ml, diluir a volumen con fase mvil y mezclar.
Procedimiento: Inyectar la Solucin de Prueba en el cromatgrafo, registrar el cromatograma y medir las
respuestas correspondientes a los picos. Calcular el % de cada impureza mediante normalizacin interna.
Especificacin: no se encuentra ms del 2,0% de ninguna impureza individual, ni ms de 4,5% de impurezas totales.
Se procede acorde a la tcnica descripta, trabajando por triplicado, y se obtienen los siguientes resultados:
N
Pico
1
2
3
4
a.
Muestra 1
Tiempo de
retencin
3,45
4,88
6,07
15,9
rea
10956
8256
972482
10055
N
Pico
1
2
3
4
Muestra 2
Tiempo de
retencin
3,44
4,9
6,02
15,97
rea
11597
8267
968452
10121
N
Pico
1
2
3
4
Muestra 3
Tiempo de
retencin
3,47
4,62
6,12
15,95
rea
11248
8194
970254
10091
Cumplen las ampollas con el ensayo realizado?
b. Crees que es adecuado realizar la cuantificacin por normalizacin interna en este caso? Justifica.
CONTROL DE CALIDAD DE MEDICAMENTOS ENSAYO DE VALORACIN
CONTROL DE CALIDAD DE MEDICAMENTOS DETERMINACIN DE AGUA
2. DETERMINACIN DE AGUA
PROBLEMA 1
a.
b.
c.
d.
Qu mtodos conoces para determinar la humedad de drogas?
Cmo se realizan?
Cmo seleccionaras el mtodo adecuado para un pa determinado?
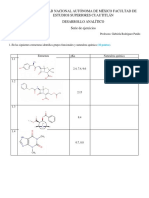
Completa la siguiente tabla:
Principio activo
Ttulo
SDA/SDD
Contenido de Agua
Carbamazepina
(C15H12N2O)
99,32%
SDD
0,37%
Metildopa
(C10H13NO4.3/2H2O
100,64%
SDA
Etosuximida
(C7H11NO2)
Piperazina
(C4H10N2)
SDA
Citrato de K
(C6H5K3O7.H2O)
101,37%
Tartrato de Na y K
(C4H4KNaO6.4H2O)
100,22%
USP <921> Mt. I
99,12%
USP <731>
94,89%
1,55%
5,48%
Clorhidrato de
Ranitidina
(C13H22N4O3S.HCl)
%sdtc
88,72%
0,40%
98,61%
Mtodo*
SDD
99,72%
23,4%
USP <921> Mt. I
* Prdida por Secado <731> o Determinacin de Agua <921>. El captulo <921> de la USP incluye tres mtodos: Mtodo
I (por titulacin), Mtodo II (destilacin azeotrpica con tolueno) y Mtodo III (gravimtrico). El Mtodo I, por su
parte, se presenta en tres versiones:
Ia. Titulacin directa (o de Karl Fischer)
Ib. Titulacin residual (o KF por retorno)
Ic. Titulacin colorimtrica.
A menos que se indique lo contrario en la monografa individual, cuando se indica Mtodo I debe realizarse el Ia.
PROBLEMA 2
Se disuelven 0,462 g de un pa en 10 ml de metanol y se valora con un reactivo de Karl Fischer (KF), de ttulo 12,42
mg/ml. Se requieren 2,4 ml de KF para valorar el agua de la muestra. Se realiz un ensayo en blanco con 50 ml de
metanol y se obtuvo un consumo de 0,3 ml de KF.
Cul es el porcentaje de agua en la muestra?
CONTROL DE CALIDAD DE MEDICAMENTOS DETERMINACIN DE AGUA
PROBLEMA 3
La determinacin de H20 por Karl Fischer para la siguiente materia prima fue de 5,0%:
Las alcuotas pesadas y los volmenes
de reactivo gastados fueron:
Muestra (mg) Volumen reactivo (ml)
302,1
3,10
299,7
3,00
PM = 336,15
a.
b.
Cul era el ttulo del reactivo de Karl Fischer utilizado?
Si el ttulo de la droga calculado sobre base anhidra es de 99,0%, cul ser el ttulo sdtc?
PROBLEMA 4
Llega a nuestro laboratorio de Control de Calidad la siguiente materia prima (MP) para una re-valoracin de la
misma, ya que se ha pasado su fecha de re-anlisis. El protocolo del proveedor indicaba un ttulo de 99,8% SDD y
3% de PPS (prdida por secado), con fecha de re-anlisis de hace dos aos.
Las especificaciones de farmacopea para dicha sustancia son:
Contenido: 95,0% 105,0% SDD
Prdida por secado: menor al 4,0%
Valoracin: volumetra en fase heterognea
Por lo tanto, se procede de la siguiente manera:
En dos cpsulas previamente secadas, se pesan aproximadamente 1,5000 g de MP y se llevan a estufa (120
2 C). Luego de 8 hs, se retiran y tapan las cpsulas, se dejan enfriar en desecador y se vuelven a pesar.
Resultados:
Cpsula 1
Cpsula 2
Peso original
1,4865
1,5263
Peso luego del secado
1,4321
1,4699
Se pesan cuatro alcuotas de la misma MP (Pmeq = 197), se disuelven en 50 ml de una mezcla agua:
cloroformo (1:1) y se valoran con Lauril Sulfato de Sodio 0,050 N, previamente estandarizado contra
papaverina. Se realiza un ensayo en blanco y se emplea azul de metileno como indicador del punto final.
Resultados:
CONTROL DE CALIDAD DE MEDICAMENTOS DETERMINACIN DE AGUA
a.
Alcuota (mg)
Volumen de LS Na (ml)
--
0,2
203,2
19,7
204,4
19,9
211,5
20,7
193,2
18,5
Cumple an la MP con las especificaciones de farmacopea?
PROBLEMA 5
Se dispone de dos materias primas (MP), cuyos certificados de anlisis indican lo siguiente:
Materia Prima 1
Cefalexina Monohidrato USP
C16H17N3O4S.H2O
Valoracin: 98,70% de Cefalexina SDA
Contenido de agua: 5,3%
Materia Prima 2
Cefalexina Clorhidrato Monohidrato USP
C16H17N3O4S.HCl.H2O
Valoracin: 89,33% de Cefalexina SDA
Contenido de agua: 5,3%
Informacin de Farmacopea:
Cefalexina - C16H17N3O4S.H2O PM=365,4
La Cefalexina tiene una potencia de no menos de 950 g y de
no ms de 1030 g de C16H17N3O4S por mg, calculado con
respecto a la sustancia anhidra
- Agua, Mtodo I <921>: entre 4,0% y 8,0%
Clorhidrato de Cefalexina
C16H17N3O4S.HCl.H2O PM=401,87
El Clorhidrato de Cefalexina contiene el equivalente a no menos
de 800 g y no ms de 880 g de cefalexina (C16H17N3O4S) por mg
- Agua, Mtodo I <921>: entre 3,0% y 6,5%
a.
Completa las siguientes tablas:
MP 1
Ttulo sdtc como base
Ttulo sdtc como monohidrato
Ttulo sdtc como clorhidrato
---------------
Ttulo sdtc como clorhidrato monohidrato
---------------
MP 2
Pero cul de
esos ttulos se usa?
Depende
CONTROL DE CALIDAD DE MEDICAMENTOS DETERMINACIN DE AGUA
Formulaciones:
MP
Cefalexina (como C16H17N3O4S.H2O)..500 mg
Excipientes csp.......... 750 mg
II
Cefalexina (como C16H17N3O4S.HCl.H2O).. 500 mg
Excipientes csp.. 750 mg
III
Cefalexina Monohidrato... 500 mg
Excipientes csp..... 750 mg
IV
Cefalexina Clorhidrato ..500 mg
Excipientes csp.. 750 mg
Cefalexina Clorhidrato Monohidrato... 500 mg
Excipientes csp.. 750 mg
b.
Cunto deberas
pesar de MP?
Dosis (mg)
Cefalexina Base
1
2
Cul es la diferencia (en % de dosis de Cefalexina base) entre las formulaciones I y III? entre la I y la IV? y
entre la I y la V?
10
CONTROL DE CALIDAD DE MEDICAMENTOS VALIDACIN
3. VALIDACIN DE MTODOS ANALTICOS
PROBLEMA 1
Linealidad y rango LD y LC
Se estudi la linealidad, entre otros parmetros, durante la validacin de un mtodo analtico instrumental (seal
vs. concentracin) a ser utilizado para la valoracin de un pa en su forma farmacutica comprimidos. Se
prepararon por duplicado 5 soluciones a partir de pa (SR, Sustancia de Referencia) para un rango de
concentraciones que representa aproximadamente el equivalente a 50-75-100-125 y 150% de la concentracin de
trabajo elegida. Posteriormente se obtuvo la seal de cada una de estas soluciones por duplicado. Resultados:
Porcentaje (%)
50
75
100
125
150
a.
b.
c.
d.
Concentracin (mg/ml)
Seal (prom, n=2)
10,1
28
11,0
29
15,3
40
15,0
42
20,2
54
20,0
52
24,8
64
25,0
68
30,0
80
31,0
85
Cul es el objetivo del ensayo de linealidad? Determina la recta de regresin, el coeficiente de correlacin y
los intervalos de confianza para la pendiente y la ordenada al origen.
Qu opinas de la linealidad del mtodo? Se cumplen los criterios de linealidad?
La tercera columna de la tabla dice prom, n=2 Por qu crees que se promediaron las seales? Provenan
de soluciones independientes?
Cul es el rango del mtodo analtico? Estima los lmites de deteccin y cuantificacin.
PROBLEMA 2
Ensayo de recuperacin tpico
Para determinar la exactitud de un mtodo analtico a ser utilizado en la valoracin de un pa en su forma
farmacutica comprimidos, se procede de la siguiente manera:
Se preparan, por cuatriplicado, soluciones muestra conteniendo pa SR + excipientes en la proporciones
declaradas para cada uno de los niveles de concentracin a evaluar (80, 100 y 120% del valor declarado).
Se inyecta, por triplicado, cada solucin en el cromatgrafo y para cada solucin muestra se calcula la
Concentracin hallada, utilizando un estndar de pureza reconocida. Una vez obtenida la Concentracin
hallada, se evala la relacin entre la Concentracin terica y la Concentracin hallada, mediante el
porcentaje de recuperacin. Resultados:
11
CONTROL DE CALIDAD DE MEDICAMENTOS VALIDACIN
Nivel %
80
100
120
a.
b.
c.
d.
e.
C terica (g/ml)
C hallada (g/ml)
40,16
39,92
40,16
40,04
40,16
40,10
40,16
39,57
50,20
50,03
50,20
50,70
50,20
50,61
50,20
50,00
60,24
59,58
60,24
60,05
60,24
60,05
60,24
59,34
%Recuperacin
%Recup medio y CV
Cul es la concentracin de trabajo? Describe una forma posible para preparar las soluciones de trabajo
(peso, volumen, diluciones).
Cmo se realizan los clculos para conocer C terica y C hallada?
Evala la exactitud del mtodo analtico ensayado mediante la prueba t y mediante el mtodo de la recta C
terica vs. C hallada. Se cumplen los criterios de exactitud segn ambos mtodos?
Tiene alguna relacin el mtodo de C terica vs. C hallada con la linealidad del mtodo?
Evala la precisin del mtodo analtico a cada nivel de trabajo. De qu nivel de precisin se trata? Se
cumplen los criterios?
PROBLEMA 3
Importante para el TP grupal
Para un estudio de equivalencia farmacutica entre las diferentes marcas disponibles en el mercado argentino,
se ha desarrollado un mtodo por espectrofotometra UV directa en agua para la determinacin de Ibuprofeno
en la siguiente formulacin:
Ibuprofeno.. 400 mg
Excipientes csp... 600 mg
El mtodo fue validado en trminos de su linealidad, rango y precisin, cumpliendo con los criterios de aceptacin
en todos los casos. En cuanto a la especificidad del mtodo, la misma se determina para cada marca en una etapa
previa a la valoracin de las mismas, por el mtodo del cociente a dos longitudes de onda (). A continuacin se
presentan los resultados obtenidos para tres de las 36 marcas analizadas:
Solucin
Ibuprofeno SR
Solucin
Marca 1
Solucin
Marca 2
Solucin
Marca 3
Abs 1
0,365
0,388
0,346
0,315
Abs 2
0,682
0,652
0,654
0,591
12
CONTROL DE CALIDAD DE MEDICAMENTOS VALIDACIN
a.
b.
c.
Realiza los clculos correspondientes a la evaluacin de la especificidad. Independientemente de que se
considere numerador o denominador, debes verificar que slo la Marca 3 cumple con el criterio del 1%
Qu actitud tomaras en aquellos casos donde no se cumple el criterio? Trataras de igual manera a las
marcas 1 y 2?
Si el espectro del ibuprofeno en el medio de trabajo es el siguiente, cules crees que podran ser 1 y 2?
1
Abs
0,8
0,6
0,4
0,2
0
200 220 240 260 280 300 320 340 360 380
Long. de onda
PROBLEMA 4
Robustez
Un laboratorio de control de calidad desea evaluar la robustez de un mtodo analtico. Para ello, se eligen
primero las variables a evaluar y sus respectivos lmites:
Variable
Da del ensayo
pH del buffer
Analista
Columna
T horno (C)
Flujo de FM (ml/min)
(nm)
Lmite inferior
08/09
2,4
S
Usada (U)
48
0,8
214
Lmite superior
10/09
2,6
C
Nueva (N)
52
1,1
216
Una vez elegidas las variables, se disea el ensayo utilizando la matriz de Placket-Burman:
Da del ensayo
pH del buffer
Analista
Columna
T horno (C)
Flujo fase mvil (ml/min)
(nm)
1
10/09
2,4
S
U
52
1,1
216
2
10/09
2,4
C
U
48
0,8
214
3
10/09
2,6
S
N
52
0,8
214
Ensayo N
4
5
10/09
08/09
2,6
2,4
C
S
N
N
48
48
1,1
1,1
216
214
6
08/09
2,4
C
N
52
0,8
216
7
08/09
2,6
S
U
48
0,8
216
8
08/09
2,6
C
U
52
1,1
214
Luego se preparan por duplicado soluciones de pa SR + excipientes correspondientes a cada uno de los niveles
de concentracin a evaluar (80, 100 y 120% del valor terico, 150 g/ ml). Cada solucin se inyecta por duplicado
en el cromatgrafo y posteriormente se calcula el porcentaje recuperado utilizando contra una solucin de pa SR
sin excipientes. Resultados:
13
CONTROL DE CALIDAD DE MEDICAMENTOS VALIDACIN
Porcentaje
Recuperado
a.
b.
c.
d.
80%
100%
120%
1
81,38
100,68
119,80
2
81,70
100,90
119,61
3
81,42
100,79
119,52
Ensayo N
4
5
80,78
80,59
100,27 100,35
119,17
119,08
6
81,03
100,22
118,76
7
81,48
100,22
119,02
8
81,81
101,05
118,48
Determina si el mtodo es robusto frente a las variables estudiadas.
Cmo crees que se procedi para las lecturas del pH de la fase mvil?
Qu actitud tomaras frente a aquellas variables para las cuales el mtodo no resulta robusto?
Describe detalladamente cmo crees que se obtuvo experimentalmente el valor de SD en repetibilidad
que se emplea para el clculo del estadstico en robustez (SD: desviacin estndar).
80%
Diferencia calculada (valor absoluto)
100%
120%
Da del ensayo
pH del buffer
Analista
Columna
T horno (C)
Flujo de FM (ml/min)
(nm)
SD en repetibilidad
Estadstico
0,330
0,45
0,41
PROBLEMA 5
Se realiz la validacin de un mtodo analtico por HPLC-UV el cual ser aplicado a la valoracin de comprimidos
de Amitriptilina con la siguiente composicin:
Amitriptilina Clorhidrato................................ 25 mg
Excipientes csp ...............................................175 mg
Condiciones cromatogrficas:
Columna: RP-18 de 30 cm x 4 mm, 5 m
Fase mvil: Buffer fosfato pH 2.5 : Acetonitrilo (58 : 42)
Flujo: 2 ml/min - : 254 nm.
Se pesaron 40,3 mg de Amitriptilina Clorhidrato SR (99,5% sdtc) y se
disolvieron en 50 ml de fase mvil, a partir de esta solucin se realiz una
dilucin 1/10 tambin con fase mvil, la que se filtr e inyect en el
cromatgrafo por sextuplicado. Resultados:
Nota: El mtodo ajusta a un modelo
lineal en el rango de concentraciones
entre: 35 - 150 g/ml, y es selectivo
respecto a los excipientes.
Inyeccin N
1
2
3
4
5
6
rea de pico
85439
84285
85603
84952
85553
84852
14
CONTROL DE CALIDAD DE MEDICAMENTOS VALIDACIN
Por otro lado, se prepararon soluciones de la siguiente manera:
Muestras (M): Los mg de amitriptilina clorhidrato SR (99,5 % sdtc) indicados en la tabla a continuacin ms 150
mg de una mezcla de excipientes se colocaron en un matraz de 25 ml con fase mvil, se sonic durante 10 minutos
y se centrifug 10 minutos a 2500 rpm. A partir del sobrenadante se realiz una dilucin 1/10 con fase mvil, se
filtr y se inyect en el cromatgrafo por duplicado. Resultados:
a. Calcula la precisin del sistema. Qu evala este parmetro?
b. Calcula la exactitud y precisin del mtodo. Se cumplen los
criterios de aceptacin de stos ensayos?
Muestra
Peso SR
M1.1
20,8
M1.2
20,7
M1.3
20,9
M2.1
24,8
M2.2
24,6
M2.3
24,7
M3.1
30,4
M3.2
30,3
M3.3
30,4
rea de pico
86891
88639
87940
88633
87129
88636
104253
105267
104754
104258
101947
102543
128456
126057
127429
125647
123970
123547
PROBLEMA 6
Se desea controlar una especialidad medicinal de un principio activo por espectrofotometra UV-VIS, por lo que
se comienza por validar dicho mtodo. Formulacin:
Sertralina HCl .............................................. 100 mg
Aerosil 200 .................................................. 32 mg
Celulosa microcristalina ............................. 50 mg
Povidona ..................................................... 32 mg
Almidn glicolato de sodio......................... 100 mg
Talco ............................................................ 28 mg
Estearato de magnesio ...............................10 mg
Se realiza una curva de calibracin a partir de Sertralina HCl SR (Pureza: 98% sdtc), para lo cual se pesan 5 alcuotas,
se disuelven en 100 ml de agua destilada, se diluyen (ver tabla) y se leen a 300 nm:
Mg Pesados
10,8
16,1
10,6
12,0
14,9
Dilucin
1/20
1/20
1/10
1/10
1/10
Abs (300 nm)
0,256
0,398
0,520
0,596
0,730
15
CONTROL DE CALIDAD DE MEDICAMENTOS VALIDACIN
El mismo da de trabajo se realiza un ensayo de recuperacin (a un solo nivel) pesando con exactitud alrededor
de 100,0 mg de la misma SR a los que se agregan 400 mg de una mezcla de excipientes y se llev a volumen con
100 ml. Luego de realizarse diluciones 1/100 se procedi a la lectura por UV (300 nm), obtenindose los siguientes
resultados:
Mg pesados
Abs (300 nm)
100,0
0,514
100,8
0,516
100,3
0,500
101,0
0,532
a. Qu parmetros de validacin fueron evaluados?
b. Detalla cmo crees que se prepararon las soluciones con las que se obtuvieron los espectros.
c. De acuerdo a los resultados, consideras que el mtodo es confiable? Justifica tu respuesta.
d. Qu modificaciones le haras al mtodo analtico propuesto?
0,9
pa (10 ug/ml)
excip.(10 ug/ml)
0,7
Absorbancia
Espectros:
(los excipientes se mezclaron en las
mismas proporciones en que se
encuentran en la formulacin)
0,5
0,3
0,1
-0,1 180
230
280
330
380
430
long. onda (nm)
PROBLEMA 7
Un analista desarrolla un mtodo por UV-derivativo (UV-D) para la determinacin de Levotiroxina Sdica en
comprimidos. Como no cuenta con SR del principio activo, decide evaluar la exactitud mediante la comparacin
de los resultados que arroja dicho mtodo con aquellos que se obtienen al aplicar un mtodo por HPLC extrado
de la farmacopea a las mismas muestras.
Condiciones mtodo UV-D: se utiliza la segunda derivada del espectro de absorcin a 253 nm (2D253) en
metanol:agua (50:50; v/v) (pH 11.2) como medio.
Condiciones mtodo HPLC: columna RP18 (125 x 4 mm, 5 m) y fase mvil metanol:cido fosfrico (0.1%) (70:30,
v/v) (pH 3). El flujo es de 1,5 ml/min y la deteccin a 225 nm.
Nota: el mtodo farmacopeico cumpli con el test de Aptitud del Sistema y result especfico para las muestras.
Preparacin de las muestras: se pesan individualmente 10 comprimidos y se pulverizan en mortero hasta lograr
un polvo homogneo. A partir de all se pesa la cantidad de muestra necesaria para lograr las concentraciones
deseadas, se coloca en un matraz de 50 ml que se lleva a volumen con metanol. Se sonica durante 20 min, se
centrifuga una porcin durante 10 min a 3500 rpm y a partir del sobrenadante se procede de la siguiente manera:
Para el mtodo por UV-D, se lee directamente la 2D253
Para el mtodo por HPLC, se realiza una dilucin 1:10 con fase mvil, se filtra y se inyecta en el
cromatgrafo. Posteriormente se registra el valor de rea obtenido.
16
CONTROL DE CALIDAD DE MEDICAMENTOS VALIDACIN
Cuando analiza las muestras preparadas (N=6) por ambos mtodos, y grafica Concentracin hallada UV-D vs.
Concentracin hallada HPLC, obtiene lo siguiente:
Valor
Error tpico (s)
Ordenada (a)
0,223607
1,283646
Pendiente (b)
0,999007
0,011282
Coef. Determinacin (r2)
0,999235
Conc. hallada UV-D
120,0
100,0
80,0
60,0
40,0
20,0
0,0
0
20
40
60
80
100
120
Conc. hallada HPLC
Por otro lado, los valores por UV-D al analizar muestras independientes (n=3 para cada nivel) fueron:
Muestra
1
2
3
4
5
6
Concentracin hallada por UV-D (mg/L)
Replic. 1
Replic. 2
Replic. 3
4,35
4,28
4,40
10,42
10,29
10,64
12,33
12,56
12,16
37,05
35,69
36,06
66,45
66,88
66,21
105,03
106,13
104,75
a. Qu opinas de la exactitud y precisin del mtodo desarrollado?
b. Si contaras con SR del pa, cmo habras procedido para determinar ambos parmetros?
PROBLEMA 8
Muy importante para el TP grupal
Se desea validar un mtodo analtico para la determinacin de Ranitidina Clorhidrato (HCl) en comprimidos por
UV directo, en agua destilada y a 314 nm. Frmula:
Ranitidina (HCl).. 300 mg
Excipientes csp 500 mg
Para todo el protocolo de validacin se emple Ranitidina HCl SR, de ttulo 98,7% sdtc
Peso Molecular Ranitidina HCl: 350,87
Peso Molecular Ranitidina base: 314,37
17
CONTROL DE CALIDAD DE MEDICAMENTOS VALIDACIN
En primer lugar, se construye una curva de calibracin con cinco niveles de concentracin en el rango 4 16 g/ml
de Ranitidina Base, preparados a partir de dos soluciones madre (S1 y S2) madre de Ranitidina Clorhidrato SR.
Nota: llamamos soluciones madre a aquellas que se preparan directamente por pesada del slido y disolucin en
el medio de trabajo. A partir de dichas madres se preparan el resto de las soluciones por simple dilucin.
Preparacin de S1 y S2: se disolvieron alrededor de 11 mg de Ranitidina HCl SR (ver el valor exacto en el grfico
debajo) en 50 ml de agua destilada.
S1
(11,18 mg)
M1
1 / 50
Absorbancia a 314 nm: 0,198
M2
2 / 50
0,411
S2
(11,15 mg)
M3
5 / 100
0,505
M4
3 / 50
0,614
M5
2 / 25
0,815
A continuacin se lee seis veces la absorbancia de la solucin M3, obtenindose los siguientes valores:
0,505 0,505 0,504 0,503 0,506 0,504.
Por ltimo, se prepara una tercera solucin madre (S3) de la misma manera que las anteriores, pesando 11,20 mg
de Ranitidina HCl SR. De esa forma, se logra tener tres soluciones independientes a la concentracin de trabajo:
M3, M3 y M3:
S1
(11,18 mg)
Absorbancia a 314 nm:
M3
5 / 100
0,505
S2
(11,15 mg)
M3
5 / 100
0,499
S3
(11,20 mg)
M3
5 / 100
0,510
a.
Calcula las concentraciones de las soluciones M de la curva de calibracin como Ranitidina Base, y explica
por qu crees que se trabaja con base y no HCl, como en el problema 5 (Amitriptilina Clorhidrato).
b. Cul es la concentracin de trabajo? Qu porcentajes de dicha concentracin abarca el rango de linealidad
del mtodo?
c. Evala si se cumplen los criterios de linealidad. Por qu se realizan diluciones cruzadas?
d. Calcula la precisin del mtodo y del sistema. Por qu no es necesario calcular %Recuperado como en los
problemas 2, 4 y 5?
PROBLEMA 9
Aptitud del Sistema
Un analista de control de calidad desea determinar Pantoprazol Sdico en su forma farmacutica comprimidos
de liberacin retardad, y elige para tal fin el mtodo codificado en la farmacopea de los EE UU (USP 34). Cuando
busca la monografa correspondiente, encuentra la informacin que se presenta en la pgina a continuacin.
a.
b.
Crees que el analista debera validar el mtodo de valoracin?
Cul crees que es el objetivo del ensayo de Aptitud del Sistema que figura en la monografa?
18
CONTROL DE CALIDAD DE MEDICAMENTOS VALIDACIN
c.
d.
Explica brevemente cmo lo haras, y muestra grficamente cmo mediras las magnitudes necesarias para
evaluar la resolucin y el factor de asimetra.
En cuanto al requisito para la SD relativa, con qu parmetro de validacin que conoces se relaciona?
PARA RECORDAR
En los problemas anteriores, el mtodo de regresin por cuadrados mnimos se puede emplear tanto para
determinar la linealidad de un mtodo analtico (ej. problema 1) como la exactitud del mismo (por el mtodo
de Conc. hallada vs. Conc. terica -ej. problema 2- y/o por comparacin entre dos mtodos analticos
diferentes -ej. problema 7-). Matemticamente los clculos son iguales, sin embargo el objetivo del ensayo
es totalmente distinto, y por lo tanto tambin se modifican los criterios de aceptacin.
Se consideran muestras independientes aquellas que provienen de pesadas independientes. Si en una tabla
se presentan ms de un valor de respuesta (absorbancia, rea de pico, etc.) para una misma pesada, dichos
valores se deben promediar antes de realizar los clculos. Por el contrario, para muestras independientes los
datos no se promedian hasta el final.
Los clculos de un ensayo de recuperacin son iguales a los de una valoracin. La diferencia es que en el
primer caso, expresamos el resultado como %Recuperado porque confiamos en las muestras (preparadas
con SR) y desafiamos al mtodo, mientras que en el segundo caso confiamos en el mtodo (ya validado) y
estamos evaluando las muestras.
19
CONTROL DE CALIDAD DE MEDICAMENTOS VALIDACIN
20
CONTROL DE CALIDAD DE MEDICAMENTOS ESPECTROSCOPA UV-VISIBLE
4. ESPECTROSCOPA UV-VISIBLE
PROBLEMA 1
A continuacin se presentan los espectros de absorcin de dos principios activos (pa 1 y pa 2), realizados en agua
y a una concentracin de 10 g/ml. Considerar que los excipientes no absorben en el rango de longitudes de onda
entre 200 350 nm.
1
p.a.1
Absorbancia
0,8
p.a.2
0,6
0,4
0,2
0
-0,2
200
250
300
350
long. onda (nm)
a.
A partir de los datos anteriores, cmo valoraras dichos pa en la siguiente especialidad?
Pa 1.......................................................... 2,0 mg
Pa 2...................................... 75,0 mg
Excipientes csp................................... 100,0 mg
PROBLEMA 2
En un laboratorio de control de calidad se recibe la muestra de un producto con la frmula detallada debajo,
cuyos espectros de absorcin UV (medio: etanol) se muestran en la figura correspondiente. El analista decide
cuantificar el principio activo por UV-derivativo y para ello elije trabajar a 260 nm.
1,4
Pa... 100 mg
Excipientes csp..150 mg
pa - 20 g/ml
1,2
Excipientes - 20 g/ml
1
0,8
0,6
Especificacin: el contenido de pa en
los comprimidos debe encontrarse
entre 90 110% SVD.
0,4
0,2
0
220
230
240
250
260
270
280
290
300
Preparacin de la solucin de la Sustancia de Referencia (SR): se pesaron 20,8 mg del pa SR (97,3% stdc) y se
colocaron en un matraz de 100 ml. Se agregaron aproximadamente 80 ml de etanol, se sonic hasta disolucin
total del slido y se llev a volumen. A partir de all, se realiz una dilucin 1:10 con el mismo medio y se ley la
Amplitud de la derivada primera a 260 nm. Se obtuvo el valor de 0,158.
Preparacin de las muestras (M): se pulverizaron 10 comprimidos (peso medio: 163,2 mg) en el mortero y luego
se pesaron cuatro alcuotas de polvo equivalentes a 20 mg del pa. Cada una se coloc en un matraz de 100 ml al
que se agregaron aproximadamente 80 ml de etanol para llevar a sonicar durante 15 minutos. Se llev a volumen,
21
CONTROL DE CALIDAD DE MEDICAMENTOS ESPECTROSCOPA UV-VISIBLE
se centrifug una porcin de cada muestra y se realiz una dilucin 1:10 a partir del sobrenadante. Por ltimo, se
ley la Amplitud de la derivada primera a 260 nm. Los resultados obtenidos se resumen en la tabla a continuacin:
a.
b.
c.
Muestra
Peso (mg)
Amplitud a 260nm
M1
32,50
0,113
M2
33,01
0,115
M3
32,20
0,110
Por qu crees que el analista decidi trabajar mediante UV-derivativa? Podra haber hecho el anlisis por
UV-directo? Justifica tu respuesta con los clculos correspondientes.
Qu opinas de los resultados obtenidos? A qu pueden deberse?
Muestra con un grfico la forma aproximada que tendr el espectro derivado del pa y de los excipientes en
la zona cercana a 260 nm.
PROBLEMA 3
Se procede a evaluar por UV-D de primer orden un lote de comprimidos con la siguiente formulacin:
Losartan (pa A)........ 50 mg
Hidroclorotiazida (pa B).......... 12,5 mg
Especificacin (ambos pa): 90 - 110% SVD
Sustancia de Referencia del pa A: se pesan 13,5 mg de SR de pa A (99,3% sdtc), se disuelven en 25 ml de acetonitrilo
y se realiza una dilucin 1:25. La amplitud a 244 nm fue de -0,399.
Sustancia de Referencia del pa B: se pesan 13,8 mg de SR de pa B (99,8% sdtc), se disuelven en 50 ml de
acetonitrilo y se realiza una dilucin 1:50 con el mismo solvente. La amplitud a 322 nm fue de 0,423.
0,8
pa A (20 g/ml)
Espectros
Derivados
0,6
pa B (20 g/ml)
0,4
0,2
0
200
220
240
260
280
300
320
340
-0,2
-0,4
-0,6
Preparacin de la muestra: se pesaron y pulverizaron 10 comprimidos de la especialidad (peso medio: 122,3 mg).
Del pool obtenido se pesaron tres alcuotas de polvo y se trasvasaron a matraces de 100 ml utilizando como
solvente acetonitrilo. Se agitaron 20 min, para luego centrifugar 10 min a 2000 rpm, se midieron 200 L del
sobrenadante, se diluyeron a 10 ml con el mismo medio y se ley su amplitud. Resultados:
22
CONTROL DE CALIDAD DE MEDICAMENTOS ESPECTROSCOPA UV-VISIBLE
a.
b.
Alcuota (mg)
Amplitud 244nm
Amplitud 322nm
262,3
-0,392
0,452
260,0
-0,388
0,450
264,1
-0,400
0,458
De acuerdo a los resultados obtenidos, qu puedes concluir respecto al lote de comprimidos?
Crees que el mtodo seleccionado fue el adecuado?
PROBLEMA 4
Un laboratorio de control de calidad recibe la siguiente especialidad medicinal (jarabe) para la valoracin de los
principios activos 1 y 2:
Pa 1...... 350 mg
Pa 2...... 1500 mg
Excipientes csp.............. 100 ml
Valoracin del pa 2
Mtodo: UV directo a = 300 nm en agua
Especificacin: 90-110% SVD
A1%1cm de pa 1 a 300 nm en agua destilada = 20. Los excipientes no interfieren.
Preparacin de la SR del pa 2: 25 mg de SR (96,5% sdtc) se disuelven en 25 ml de agua destilada y se realiza una
dilucin 0.1:10 con dicho medio. Se mide la absorbancia a 300 nm, obtenindose una absorbancia promedio (n =
3) de 0,615
Preparacin de la muestra: se toman 3 alcuotas de 10 ml de jarabe, que se trasvasan a matraces de 100 ml, se
agrega 25 ml de agua destilada, se sonica durante 10 minutos, se completa a volumen con agua destilada y se
centrifuga a 2500 rpm, a partir del sobrenadante se realiza una dilucin 0,35:50 con dicho medio, se mide la
absorbancia de cada alcuota a 300 nm obtenindose los resultados que se muestran en la tabla:
Alcuota (ml)
10,0
10,0
10,0
Abs. (=300 nm)
0,660
0,652
0,658
Valoracin del pa 1
0,8
A continuacin se presentan los espectros realizados en
medio de NaOH 0,1 N, a 10 g/ml de cada pa.
0,6
pa 1
pa 2
Abs
0,4
0,2
0
a.
b.
c.
Con qu elementos volumtricos se debieron
200
250
300
tomar y diluir las alcuotas de jarabe?
Long. de onda
Cumple el pa 2 con las especificaciones?
En funcin de los espectros presentados, indica cmo procederas para valorar el pa 1. Los excipientes no
interfieren.
23
CONTROL DE CALIDAD DE MEDICAMENTOS ESPECTROSCOPA UV-VISIBLE
PROBLEMA 5
Llega a un laboratorio de Control de Calidad el siguiente producto para analizar:
pa (HCl)........ 300 mg
Excipientes csp........ 1000 mg
1,4
Excip. 2000 mg/L
1,2
pa 300 mg/L
PM pa (base): 314,4
PM pa.HCl: 350,9
0,8
0,6
0,4
El mtodo codificado en farmacopea para dicha
especialidad consiste en una determinacin por UV
directo a 255 nm.
0,2
0
200
220
240
260
280
300
320
340
Especificacin: 90 - 110% SVD
1.
2.
Cuando el analista determina el pa por dicho mtodo, obtiene un resultado de 111% SVD.
Decide entonces cambiar de metodologa, y determinar el principio activo por UV-Derivativo a 300 nm.
Obtuvo los siguientes resultados:
Solucin de Referencia (SR): pesa 34,12 mg de pa.HCl SR (97,4% sdtc) y los disuelve en 50 ml de metanol, y a partir
de all realiza una dilucin 1:25. Amplitud a 300 nm: 0,253
Muestras: pesa 10 comprimidos (peso medio: 1112,6 mg) y los pulveriza en mortero. A partir de all pesa alcuotas
de aproximadamente 30 mg de pa y las coloca en 50 ml de metanol. Sonica, centrifuga y del sobrenadante realiza
una dilucin 1:25.
Alcuota
Peso
Amplitud a 300 nm
M1
110,8
0,215
M2
111,1
0,216
M3
108,9
0,209
M4
109,4
0,211
a. Por qu crees que se obtuvo un valor tan elevado por UV-directo a 255 nm? Justifica con cuentas.
b. Qu resultado arroj el mtodo por UV-derivativo? Explica los mismos en base a los espectros mostrados
en la figura.
c. En base a los resultados anteriores, elige las condiciones de trabajo (mtodo, longitud de onda) a las que
determinaras el principio activo.
PROBLEMA 6
Se desea cuantificar los principios activos presentes en la siguiente especialidad medicinal (comprimidos):
Hidroclorotiazida........................... 50 mg
Amilorida Clorhidrato.................... 5 mg
Excipientes csp.............................. 200 mg
24
CONTROL DE CALIDAD DE MEDICAMENTOS ESPECTROSCOPA UV-VISIBLE
Espectro directo de las SR (sustancias de referencia)
Absorbancia
1,5
Amilorida
hidroclorotiazida
0,5
0
200
-0,5
a.
250
300
350
400
longitud de onda (nm)
Cmo procederas para cuantificarlos por UV-D usando la derivada primera y el Mtodo de Ceros
Cruzados?
b. Dibuja (aproximadamente) cmo se vera el espectro derivado (UV-D) de los principios activos en la zona de
las longitudes de onda de trabajo que hayas elegido.
c. Podras aplicar este mtodo si existiera interaccin entre los pa? Cmo lo verificaras?
25
CONTROL DE CALIDAD DE MEDICAMENTOS ESPECTROSCOPA UV-VISIBLE
26
CONTROL DE CALIDAD DE MEDICAMENTOS MTODOS VOLUMTRICOS Y ANLISIS FUNCIONAL
5. MTODOS VOLUMTRICOS Y ANLISIS FUNCIONAL
PROBLEMA 1
En un laboratorio de Control de Calidad, se realiza la valoracin de Mebendazol en su forma farmacutica
comprimidos utilizando como mtodo volumtrico una valoracin cido - base en medio no acuoso.
Frmula Unitaria
Mebendazol............. 200 mg
Dixido de Silicio Coloidal................... 27 mg
Glicolato de almidn sdico........................ 40 mg
Lauril Sulfato de sodio..................... 14 mg
Polivinilpirrolidona....... 20 mg
Estearato de magnesio........ 7 mg
Celulosa microcristalina csp............ 340 mg
Mebenzadol: C16H13N3O3
PM: 298,30
Procedimiento: se pesaron 10 comprimidos de Mebendazol, se determinar el peso medio, se pulverizaron los
comprimidos, se pesaron 3 alcuotas de polvo equivalentes a 300 mg de Mebendazol, se transfirieron cada una
de las mismas a un erlenmeyer, se disolvieron en 40 ml de cido actico glacial., posteriormente se agregaron 0,1
ml del indicador Verde de Malaquita y se titul con cido Perclrico 0,0976 N.
Pmedio (de los 10 comprimidos): 353,5 mg
Especificacin: debe contener no menos de 90,0% y no ms de 110,0% del valor declarado de C16H13N3O3
Peso Alcuota (mg)
529,5
529,7
530,4
Blanco
Vol. de Reactivo (ml)
11,0
11,0
11,3
0,7
a. El peso de cada alcuota fue el correcto? Justifica con clculos.
b. Con qu componentes deberas contar para hacer el blanco? Cmo lo prepararas? (Componentes y
cantidades).
c. Qu conclusiones extraes de los resultados obtenidos en la valoracin?
PROBLEMA 2
Para calcular el ttulo de la siguiente Materia Prima (MP), se aplic
un mtodo volumtrico cido-base en medio no acuoso
Especificaciones:
Debe contener no menos de 98,0% y no ms de 102,0% de C14N2H14.HCl, calculado
con respecto a la sustancia seca.
Prdida por secado: debe ser inferior al 0,5%.
.HCl
PM: 246,7
El contenido de agua determinado en estufa a 105 C hasta peso constante fue de 0,28%.
27
CONTROL DE CALIDAD DE MEDICAMENTOS MTODOS VOLUMTRICOS Y ANLISIS FUNCIONAL
Procedimiento: se pesaron 4 alcuotas de la MP y se disolvieron en 20 ml de cido actico glacial, posteriormente
se agregaron 10 ml de solucin de Acetato Mercrico 0,2 M en cido actico glacial y 0,1 ml de indicador verde de
malaquita, y se adicion desde bureta la solucin valorante (HCLO4 en medio de cido actico y anhdrido
actico), con agitacin continua. El reactivo valorante fue estandarizado previamente contra Biftalato de Potasio
(Patrn Primario).
Patrn Primario (mg)
PM: 204,22
204,6
207,3
207,9
206,5
Blanco
Vol. HCLO4(ml)
10,1
10,3
10,3
10,2
0,1
Peso inicial
MP (mg)
251,92
249,71
263,88
255,51
Blanco
Vol. HCLO4(ml)
10,2
10,2
10,9
10,4
0,1
a. Teniendo en cuenta los resultados, cumple la MP con las especificaciones?
b. Explica detalladamente el fundamento del mtodo utilizado para el anlisis de la materia prima.
c. Explica cmo procederas para preparar 250 ml del reactivo valorante utilizado para el anlisis de la materia
prima si cuentas con las siguientes soluciones:
Solucin de HCLO4 70% p/p (PM = 100,46) y = 1,68 g/ml
Solucin de anhdrido actico 99,9% p/p (PM = 102,09) y = 1,08 g/ml
PROBLEMA 3
En un laboratorio de Control de Calidad se debe valorar la siguiente Materia Prima (MP):
Especificacin: 98 - 102% calculado como C14H22ClN3O2.HCl anhidra, contenido de agua entre 4,5 - 6%.
Para calcular el ttulo de la misma se aplic la volumetra con Nitrito de Sodio.
Preparacin del reactivo valorante: se pesaron 1,8 g de nitrito de sodio, se transfirieron a un erlenmeyer y se
diluyeron con 250 ml de agua destilada. Se estandariz el reactivo valorante con cido sulfanlico (PM = 173,19).
Procedimiento: se disuelve cada alcuota de la MP en agua destilada y se agregan 5 ml de HCl concentrado. Se
sumerge el recipiente conteniendo la solucin en un bao de agua-hielo y se adiciona desde bureta la solucin
valorante. Indicador: externo.
cido sulfanilico
(mg)
176,5
177,4
175,9
174,8
Blanco
Vol. Nitrito de
Sodio (ml)
9,7
9,8
9,5
9,3
0,1 ml
Materia Prima
(mg)
355,9
354,5
357,6
356,2
Blanco
Vol. Nitrito de
Sodio (ml)
11,0
10,9
11,1
11,0
0,1 ml
28
CONTROL DE CALIDAD DE MEDICAMENTOS MTODOS VOLUMTRICOS Y ANLISIS FUNCIONAL
Determinacin de agua: Mtodo de Karl Fisher
Se disuelve una alcuota de la muestra en 10 ml de metanol y se valora con el Reactivo de Karl Fisher (RKF), ttulo
10,2 mg/ml. Se realiza un ensayo en blanco con 50 ml de metanol y se obtiene un consumo de 0,45 ml de RKF.
Materia Prima (g)
Vol. Reactivo KF (ml)
0,502
2,53
0,507
2,54
0,510
2,55
a.
Explica detalladamente el fundamento e interferencias del mtodo utilizado para el anlisis de la materia
prima.
b. Teniendo en cuenta los resultados, cumple la MP con las especificaciones?
c. Cul o cules de los mtodos alternativos que se describen a continuacin podras utilizar para valorar la
MP? Justifica y explica brevemente fundamento e interferencias del mismo:
* Formacin de iminas con 2,4 pentanodiona
* Adicin de bisulfito
* Saponificacin
PROBLEMA 4
En un laboratorio de Control de Calidad se valor el cido acetilsaliclico (AAS)
Materia Prima, mediante un mtodo volumtrico cido-base en medio acuoso.
Especificacin:
# Debe contener no menos de 99,5% y no ms de 100,5% de Aspirina calculada sobre
sustancia seca (FA 7)
# Prdida por secado: menor al 0,5%
PM: 180,16
Valoracin:
Se pesan cuatro alcuotas de AAS materia prima, se trasfiere a un erlenmeyer. Se agregan 20 ml de hidrxido de
sodio 0,5 N y se calienta a reflujo durante 15 minutos. Se utiliza como indicador fenolftalena, y se titula el exceso
de hidrxido de sodio con cido sulfrico 0,5075 N.
La determinacin de la prdida por secado de la MP arroj un valor de 0,4%.
Alcuota (mg)
302,12
301,52
310,65
306,40
Blanco
a.
b.
Volumen Rvo. (ml)
13,2
13,2
13,0
13,1
19,8
Qu conclusiones extraes a partir de los resultados obtenidos?
De los mtodos volumtricos que conoces, cul/es otros utilizaras para la valorar la MP? Justifica tu
respuesta.
29
CONTROL DE CALIDAD DE MEDICAMENTOS MTODOS VOLUMTRICOS Y ANLISIS FUNCIONAL
PROBLEMA 5
Para controlar la siguiente especialidad:
Pa...250 mg
Excipientes csp. 520 mg
PM: 171,2
Se procedi de la siguiente manera:
Preparacin de la muestra: luego de pulverizar 10 comprimidos (Peso medio: 520,5 mg), se pesaron 3 alcuotas
del polvo, las cuales fueron sometidas a una acilacin con anhdrido actico, hidrolizando el exceso y valorando
el cido actico generado con NaOH 0,117 N. Un blanco con anhdrido actico solo y otro con anhdrido actico +
excipientes consumieron en ambos casos 20 ml de NaOH 0,117 N.
Especificaciones: 90 - 110 % SVD
Alcuota (mg)
516,1
517,6
515,8
Vol. NaOH 0,117 N (ml)
10,10
10,30
9,90
a. A partir de los resultados obtenidos, qu conclusiones extraes sobre la especialidad?
b. Propone 2 mtodos volumtricos para controlar el siguiente pa. Justifica tu eleccin y descrbelos
brevemente.
30
CONTROL DE CALIDAD DE MEDICAMENTOS TLC
6. CROMATOGRAFA EN CAPA FINA (TLC)
PROBLEMA 1
En un laboratorio de Control de Calidad se debe realizar el ensayo de pureza cromatogrfica por TLC de
Clorhidrato de Amitriptilina, materia prima, de acuerdo a las especificaciones indicadas en USP 34.
CH3
H3C
Las condiciones del ensayo por TLC son las siguientes:
Fase fija: Silicagel F254
Fase mvil: Cloroformo: Metanol: Hidrxido de amonio (135:15:1)
Revelador: UV ( = 254 nm)
Criterio de aceptacin USP 34: Ninguna mancha secundaria presente en el cromatograma de la muestra en
estudio deber ser ms intensa que la mancha correspondiente al 0,5%, y la suma de las intensidades de todas las
manchas secundarias obtenidas a partir de la preparacin en estudio debe corresponder a no ms del 1%.
a.
b.
c.
Teniendo en cuenta dicho criterio, cmo realizaras el ensayo propuesto?
Describe detalladamente qu soluciones y cmo las prepararas, calles que sembraras y volmenes de
siembra.
Muestra con un dibujo un posible resultado para tu placa (manchas, intensidades).
PROBLEMA 2
Un farmacutico recibe una consulta sobre una posible falta de accin farmacolgica del siguiente preparado
magistral, en la forma farmacutica cpsulas:
Paracetamol..................... 500 mg
Aspirina.............................500 mg
Excipientes csp............ 1500 mg
HO
H3C
HO
O
O
Aspirina
N
H
CH3
Paracetamol
Por lo que el farmacutico decide realizar:
1) Identificacin y pureza cromatogrfica de las materias primas (MP).
2) Identificacin y semi-cuantificacin de los principios activos en el preparado magistral.
Nota: en todos los ensayos realizados utiliza TLC, con iguales condiciones cromatogrficas (fase fija, fase mvil,
revelador UV 254 nm)
Las especificaciones para el ensayo de Pureza Cromatogrfica que se encuentra en USP 32 son:
Paracetamol (PCM): el contenido de p-aminofenol (p-AF) (producto de degradacin) no debe ser superior al
0,5%.
Aspirina (AAS): el contenido de cido saliclico (AS) (producto de degradacin) no debe ser superior al 0,1%.
31
CONTROL DE CALIDAD DE MEDICAMENTOS TLC
Los resultados obtenidos fueron los siguientes:
Placa 1 (PCM):
PCM
MP
Placa 2 (AAS):
p-AF
AAs
MP
Placa 3 (cpsulas):
AS
PCM
AAs
Cps.
Detalles del ensayo (de todas las soluciones se sembraron 10 l):
A. Identificacin y Pureza cromatogrfica de las materias primas (placas 1 y 2):
Preparacin de la SR de PCM: se pesaron 50 mg de PCM SR y se disolvieron en 10 ml de metanol.
Preparacin de la SR de p-AF: 50 mg de p-AF SR se disolvieron en 100 ml de metanol, de esta solucin se
midieron 0,5ml y se llev a un volumen final de 10 ml con metanol (lmite de deteccin del p-AF: 0,10 g)
Preparacin de la muestra de materia prima (MP) de PCM: 50 mg de PCM MP se disolvieron en 10 ml de
metanol.
Preparacin de la SR de AAS: se pesaron 50 mg de AAS SR y se disolvieron en 10 ml de metanol.
Preparacin de la SR de AS: se pesaron 50 mg de AS SR y se disolvieron en 100 ml de metanol, de esta solucin
se midieron 0,1 ml y se llev a un volumen final de 10 ml con metanol (lmite de deteccin del AS: 0,01 g)
Preparacin de la muestra de AAS, MP: se pesaron 50 mg de MP y se disolvieron en 10 ml de metanol.
B. Evaluacin de las cpsulas (placa 3):
Preparacin de la solucin SR de PCM: 25 mg de PCM SR (100% sdtc) se disolvieron en 10 ml de metanol.
Preparacin de la solucin SR de AAS: 25 mg de AAS SR (100% sdtc) y se disolvieron en 10 ml de metanol.
Preparacin de la muestra: se pesaron 750 mg de polvo de un pool del contenido de 5 cpsulas y se
disolvieron en 100 ml de metanol, se sonic durante 10 minutos, se centrifug 15 minutos y se sembr a partir
del sobrenadante.
a.
Qu opinin te merecen los resultados obtenidos? Justifica.
PROBLEMA 3
Un paciente que presenta un problema de acn se encuentra medicado con un preparado magistral conteniendo
cido Trans Retinoico y Eritromicina. Luego de las primeras aplicaciones comienza a manifestar sntomas de
irritacin, edema, inflamacin y prurito. Consulta al farmacutico que lo elabor quin decide realizar algunos
controles sobre el preparado.
La frmula es la siguiente:
cido trans retinoico ................................................ 0,025 g
Eritromicina base ...................................................... 4 g
Gel hidroalcohlico csp ............................................ 100 g
32
CONTROL DE CALIDAD DE MEDICAMENTOS TLC
El farmacutico planifica un control de las materias primas con las que elabor la formulacin como as tambin
del producto final (gel) mediante la aplicacin de una TLC.
Luego de realizar el estudio por TLC, obtiene estos resultados:
1.
2.
3.
4.
5.
Se sembraron 0,1 g de Sustancia de Referencia (SR) de cido Trans retinoico.
Se sembraron 0,1 g de la materia prima de cido Trans Retinoico con la que se prepar el gel.
Se sembraron 16 g de Sustancia de Referencia (SR) de Eritromicina.
Se sembraron 16 g de la materia prima de Eritromicina con la que se prepar el gel.
Se sembraron 40 l de una solucin preparada disolviendo 1 g de gel en 100 ml de alcohol.
De acuerdo a los resultados obtenidos, evala qu crees que ha ocurrido con la preparacin.
PROBLEMA 4
Entre los ensayos de control de calidad codificados en farmacopeas para la especialidad medicinal Fluorouracilo
Inyectable 50 mg/ml, se encuentra el ensayo de Sustancias Relacionadas, que se realiza aplicando un mtodo de
TLC. Los lmites de aceptacin para dicho ensayo segn Farmacopea Britnica (BP) 2005 son:
Ninguna sustancia relacionada, independientemente de su identidad, deber estar presente en un porcentaje
mayor al 0,5%.
La sustancia relacionada 5-Hidroxiuracilo no deber estar presente en un porcentaje mayor al 0,1%.
Frmula cuali - cuantitativa:
Fluorouracilo .50 mg
Agua p/iny. csp. 1 ml
Condiciones cromatogrficas:
FF: Silicagel F254
FM: Acetato de Etilo: Metanol: Agua (70: 15: 15)
Revelador: UV ( 254 nm)
a.
b.
c.
Describe detalladamente como planificaras el ensayo, considerando que cuentas solamente con Sustancia
de Referencia (SR) de 5-Hidroxiuracilo.
Detalla qu soluciones y cmo las prepararas, y los volmenes de siembra.
Muestra con un dibujo un posible resultado para tu placa.
33
CONTROL DE CALIDAD DE MEDICAMENTOS TLC
PROBLEMA 5
Se realiz el ensayo de Pureza Cromatogrfica de una especialidad comprimidos con la siguiente formulacin:
Pa ... 60 mg
Excip. csp....150 mg
El pa presenta diferentes impurezas entre las que se encuentra la impureza Z, de conocida toxicidad.
Condiciones: Fase Fija: Silicagel 0,25 mm, Fase Mvil: Cloroformo: Metanol: Tolueno: Hidrxido de amonio
(140:60:20:1) Revelador: UV (254 nm)
Criterio de aceptacin: ninguna impureza presente en el cromatograma de la muestra con diferente Rf de Z debe
superar el 0,6%; la impureza Z presente en el cromatograma de la muestra debe ser menor al 0,4% y; la suma de
las intensidades de todas las manchas secundarias correspondientes a las impurezas presentes en el
cromatograma de la muestra no debe superar el 3,0%.
Se determin el lmite de deteccin para el pa
y la impureza Z obtenindose los 0,3 g
para el pa y 0,6 g para la impureza Z.
Nota: De todas las soluciones
se sembraron 10 l.
M
A1
A2
B1
Preparacin de las soluciones
Solucin A: 90,36 mg de la SR del pa 99,6 % SDTC se disolvieron en 50 ml de metanol, y se realiz una dilucin 1:
10 con metanol.
Solucin A1: 1 ml de la solucin A se diluy con 1 ml de metanol.
Solucin A2: 1 ml de la solucin A se diluy con 5 ml de metanol
Solucin B: 30 mg de la SR (100% SDTC) de la Impureza Z se disolvieron en 25 ml de metanol y se realiz una dilucin
1: 10 con metanol.
Solucin B1: 1 ml de la solucin B se diluy con 1 ml de metanol.
Solucin M: se pesaron 10 comprimidos individualmente (Peso medio: 152,5 mg), se pulverizaron y se pesaron
317,7 mg del polvo y se trasvasaron a un matraz de 25 ml, se complet a volumen con metanol, se sonic durante
15 minutos y se centrifug a 2500 rpm durante 10 minutos, a partir del sobrenadante se realiz una dilucin 5 en
10 ml.
a. De acuerdo al protocolo de trabajo descripto, puedes decir si la especialidad medicinal cumple con el ensayo
de pureza cromatogrfica?
b. Propondras modificaciones al protocolo? Explica cules.
PROBLEMA 6
Se realiz el ensayo de Sustancias Relacionadas de un principio activo, tanto en su forma materia prima (MP)
como en una especialidad comprimidos con la siguiente formulacin:
Pa................................................... 75 mg
Excip. csp....................................... 200 mg
34
CONTROL DE CALIDAD DE MEDICAMENTOS TLC
Condiciones cromatogrficas
Fase fija: Silicagel
Fase mvil: ter: cloroformo: dimetilformamida: alcohol deshidratado (70: 15: 10: 5)
Revelador: UV 254 nm
Criterio de aceptacin (tanto para MP como para comprimidos): la mancha secundaria correspondiente a la sr A,
en el cromatograma de la muestra, no debe ser mayor que el 0,1% y la mancha secundaria correspondiente a la sr
B, no debe ser mayor que el 0,05%.
Los lmites de deteccin son 0,05 g para A y 0,1 g para B.
Preparacin de las soluciones de siembra
Solucin 1: se pesan 12,5 mg de la Sustancia de Referencia (SR) de la sustancia relacionada A (100% sdtc) y se
disuelven en 25 ml de metanol. De esta solucin se mide 0,1 ml y se diluye a 10 ml con metanol. El volumen de
siembra es de 10 l.
Solucin 2: se pesan 12,5 mg de la Sustancia de Referencia (SR) de la sustancia relacionada B (100% sdtc) y se
disuelven en 25 ml de metanol. De esta solucin se mide 0,1 ml y se diluye a 10 ml con metanol. El volumen de
siembra es de 20l.
Solucin 3: del pulverizado de 10 comprimidos (Peso medio: 151 mg) se pesan 201,4 mg y se disuelven en 50 ml de
metanol. El volumen de siembra es de 50 l.
Solucin 4: se pesan 100 mg de la MP y se disuelven en 50 ml de metanol. El volumen de siembra es de 50 l.
Luego de la corrida cromatogrfica los resultados obtenidos fueron los siguientes:
SC 1
a.
b.
SC 2
SC 3
SC 4
Analiza los resultados obtenidos.
Realizaras modificaciones al protocolo de trabajo?
PROBLEMA 7
Llega a su laboratorio la materia prima rotulada Nitrato de Econazol. Adems de otros ensayos, ud. decide
estudiar la pureza cromatogrfica de dicha materia prima, y recurre para ello a la USP. All encuentra la siguiente
informacin:
Mtodo: TLC
Fase estacionaria: Silicagel
Fase mvil: 1,4-dioxano/tolueno/NH4OH 13,5 M (60/40/1)
Revelado: exposicin a vapores de yodo por 1 hora
35
CONTROL DE CALIDAD DE MEDICAMENTOS TLC
Criterio de aceptacin: Ninguna mancha secundaria encontrada en la muestra puede ser ni ms grande ni ms
intensa que el 0,375%, y el total de todas las manchas secundarias observadas no puede superar el 2,0%.
Nota: si no conoces el lmite de deteccin del principio activo, cmo lo determinaras experimentalmente?
a. Si posees Nitrato de Econazol Sustancia de Referencia (SR), cmo procederas para realizar el ensayo?
b. Describe detalladamente las soluciones que utilizaras, concentraciones y volmenes sembrados, as como
tambin la placa que esperas obtener.
PROBLEMA 8
Se evalu la pureza cromatogrfica de una materia prima que se va a usar en la elaboracin de una especialidad
medicinal en su forma farmacutica comprimidos, cuya composicin es la siguiente:
Paracetamol...500 mg
Excipiente csp...750 mg
Condiciones cromatogrficas
Fase Fija: silica gel HF254R
Fase Mvil: metanol: 1,1,1-tricloroetano: di-isopropileter (10: 40: 50)
Lmite de deteccincloroacetanilida: 0,2 g
Lmite de deteccinparacetamol: 0,5 g
Preparacin de las soluciones
Solucin 1: 2 g de la materia prima a analizar se disolvieron en 10 ml de metanol. Se sembraron 20 l.
Solucin 2: 250 mg de la materia prima a analizar se disolvieron en 10 ml de metanol y a partir de esta solucin se
realiz una dilucin 1:25. Se sembraron 10 l.
Solucin 3: se disolvieron 12,7 mg de Cloroacetanilida SR (98,5% sdtc) en 25 ml de metanol. Se hizo una dilucin
0,2:10 con el mismo medio. Se sembraron 20 l.
Criterio de Aceptacin:
La mancha secundaria correspondiente a Cloroacetanilida presente en el cromatograma de la muestra no
debe ser ms intensa que 0,005%.
Ninguna mancha secundaria presente en el cromatograma de la muestra debe ser ms intensa que 0,25%.
SC 1
a.
SC 2
SC 3
De acuerdo a los resultados observados, puedes determinar si la MP cumple el ensayo de pureza
cromatogrfica?
36
CONTROL DE CALIDAD DE MEDICAMENTOS ENSAYO DE DISOLUCIN
7. ENSAYO DE DISOLUCIN
Nota: en aquellos problemas donde se realiza un test de disolucin, realiza tus clculos, establece si el o los producto/s
cumple/n con los criterios de aceptacin de dicho test y, en caso negativo, indica siempre si tendra sentido continuar
ensayando las etapas posteriores (E2 o E3).
PROBLEMA 1
En un laboratorio de especialidades medicinales se est realizando un estudio de estabilidad en estante de
comprimidos de Naproxeno con la siguiente formulacin:
Naproxeno .............................................. 250 mg
Excipientes csp ................................ 400 mg
A tiempo cero se le realizaron los siguientes ensayos:
Valoracin del pa por HPLC: 104,9% SVD (especificacin USP 34: 90% - 110% SVD)
Uniformidad de dosis: cumple las especificaciones de USP 34
Test de disolucin
Compr.
%disuelto SVD (UV)
% disuelto SVD (HPLC)
1
2
3
4
5
6
95
97
96
98
98
97
96
97
97
98
97
98
Condiciones: aparato 2, 50 rpm
Medio: 900 ml de buffer fosfato pH: 7,4
Tiempo: 45 min
Cuantificacin: UV a 332 nm
1%
1 Naproxeno: 545
1%
1 Prod. degrad: 576
Tolerancia: no debe disolverse menos del 80% de la cantidad declarada.
En esta etapa se realiz la cuantificacin del Naproxeno disuelto por UV y por HPLC como una manera de validar el
mtodo UV.
Transcurridos 12 meses se toman muestras y se le realizan los mismos ensayos mencionados anteriormente,
obtenindose los siguientes resultados:
Valoracin pa (HPLC): 96,5% SVD
Uniformidad de dosis: cumple con las especificaciones de
USP 34
Test de disolucin: se realiza en las mismas condiciones
indicadas anteriormente:
Comprimido
Peso comp. mg
Abs UV 332 nm
1
2
3
4
5
6
418,5
425,2
419,2
420,3
421,5
422,6
0,558
0,552
0,558
0,546
0,552
0,563
Preparacin de la solucin de la SR: se pesaron 15 mg de
Naproxeno SR (97,5% sdtc), se disolvieron en 10 ml de buffer fosfato pH 7,4 y se realiz una dilucin 0,1:10. Abs a 332
nm: 0,545.
Preparacin de las muestras: a los 45 min se tomaron 5 ml de cada vaso, se centrifugaron 10 min. a 2500 rpm y del
sobrenadante se realiz una dilucin 0,55:10. Se ley cada muestra a 332 nm.
De acuerdo con los resultados obtenidos, qu puedes decir con respecto a:
a. Mtodos empleados
b. Estabilidad de la formulacin
37
CONTROL DE CALIDAD DE MEDICAMENTOS ENSAYO DE DISOLUCIN
PROBLEMA 2
Se realiz un estudio de control de calidad comparativo de dos marcas comerciales de Carbamacepina 200 mg de los
laboratorios A y B. Se realizaron los ensayos de identificacin, valoracin de principio activo y UUD, todos los cuales
cumplieron con los lmites de aceptabilidad para ambos productos (valoracin: 90-110% SVD de Carbamacepina y UUD
segn criterio USP). Se realiz tambin el ensayo de disolucin segn USP 34 y un perfil de disolucin en las mismas
condiciones obtenindose los siguientes resultados:
Ensayo de Disolucin (USP 34)
Medio: 900 ml de laurilsulfato de sodio 1%
Tolerancia: no menos del 75% (Q) de la cantidad rotulada es disuelta en 60 min.
Perfil de disolucin:
Condiciones: dem ensayo de Disolucin
Muestreo: se toman muestras a los 15, 30, 45, 60, 90 min. Con reposicin de medio fresco a 37 C
Preparacin de la solucin de SR: se pesan 24,4 mg de SR (97,8% sdtc) se disuelven en 2 ml de metanol y se lleva a 50
ml con medio, se filtra y se toman 2 ml y se completa a 50 ml con medio. Absorbancia: 0,744
Preparacin de las muestras: a cada tiempo se toman 5 ml de muestra y se reponen con 5 ml de medio fresco; se
centrifuga, se toman 2 ml y se lleva a 25 ml con medio.
Laboratorio A (%SVD)
a.
b.
c.
Laboratorio B (Abs)
Peso
15
30
45
60
90
Peso
15
30
45
60
90
392
72,1
89,5
101
100,5
100,1
280
0,378
0,566
0,630
0,614
0,649
399
75,9
91,3
101,5
102,2
102,2
282
0,324
0,462
0,610
0,575
0,585
388
80,4
89,2
99,5
100,0
98,9
278
0,307
0,533
0,552
0,574
0,648
403
62,8
93,2
103,6
103,6
103,2
275
0,358
0,521
0,590
0,653
0,679
405
67,4
93,7
104,1
104,1
104,1
276
0,378
0,528
0,569
0,631
0,635
407
76,1
93,9
104,3
104,3
104,2
278
0,351
0,522
0,577
0,631
0,659
Calcula el perfil de disolucin del producto correspondiente al Laboratorio B, y haz un grfico aproximado de
ambos perfiles superpuestos.
Cumplen ambos productos con el Test de Disolucin?
Compara los perfiles mediante el factor de similitud (f2). Podran estos productos ser Equivalentes Farmacuticos?
PROBLEMA 3
Se debe realizar el test de disolucin del producto Sulfato de Quinidina Dihidrato, Tabletas de liberacin prolongada
por 200 mg. Se recurre a la farmacopea y se encuentra lo siguiente:
Definicin: las tabletas de LP de Sulfato de Quinidina contienen cantidades de sulfato de quinidina y de sulfato de
dihidroquinidina que suman no menos de 90% y no ms de 110% de la cantidad declarada de sulfato de quinidina
indicada en la etiqueta, calculado como (C20H24N2O2)2.H2SO4.2H2O (PM=782,94)
Ensayo de Disolucin:
Aparato: Aparato 1 USP, canastillo, 100 rpm
Temperatura: 37,0 0,5 C
Muestreo: 10 ml, con reposicin
Medio: HCl 0,1N, 900 ml
Tiempos de muestreo (h)
1
4
12
Tolerancias
Entre 20% y 50%
Entre 43% y 73%
No menor de 70%
38
CONTROL DE CALIDAD DE MEDICAMENTOS ENSAYO DE DISOLUCIN
Se prepar una SR pesando 23,2 mg de Sulfato de Quinidina SR ((C20H24N2O2)2.H2SO4 94,6% sdtc), se colocaron en un
matraz de 25 ml y se llev a volumen con agua. A partir de all se realiz una dilucin 1:50 con el medio de disolucin
y su absorbancia a 248 nm fue de 0,587.
Las muestras extradas a los tiempos correspondientes se centrifugaron durante 10 minutos a 3500 rpm y a partir del
sobrenadante se realiz una dilucin 1:10 con el medio de disolucin y se ley su absorbancia a 248 nm. Los resultados
se muestran en la tabla a continuacin:
a.
b.
c.
Cumple el lote analizado con el test de disolucin?
Por qu crees que la farmacopea especifica mltiples
tiempos de muestreo? Qu se desea asegurar?
Por qu se centrifugan las muestras y no la solucin de
referencia?
Compr.
1
2
3
4
5
6
Peso
253,1
264,5
259,7
258,0
262,1
261,4
1h
4h
12 h
0,204
0,211
0,227
0,210
0,204
0,216
0,432
0,438
0,454
0,429
0,443
0,440
0,707
0,713
0,716
0,707
0,708
0,709
PROBLEMA 4
En un laboratorio de control de calidad se realiz el test de disolucin a una partida de comprimidos recientemente
elaborada de Ibuprofeno 400 mg.
Ensayo de Disolucin (USP 34)
Medio de disolucin: 900 ml de buffer fosfato pH 7,2
Temperatura: 37 + 0.5C
Aparato I a 150 rpm.
Tolerancia (Q): no menos del 70% disuelto en 30 min.
Preparacin de la solucin referencia: 45,2 mg de Ibuprofeno SR (98,2% sdtc) se
disolvieron en un matraz de 100 ml, y a partir de esta solucin se realiz una dilucin
1:50. La abs a 221 nm fue de 0,420.
Compr.
1
2
3
4
5
6
Abs
0,216
0,231
0,223
0,218
0,229
0,221
Preparacin de la muestra: se tomaron 10 ml de cada vaso a los 30 min, se filtraron por papel Whatman n 4 y a partir
del filtrado se realiz una dilucin 1:50 con medio de disolucin. Se ley la absorbancia de cada muestra a 221 nm y se
obtuvieron los resultados de la tabla.
a. Calcula el % disuelto de cada comprimido a los 30 minutos.
b. A partir de los resultados anteriores, realizaras modificaciones al procedimiento operativo?
PROBLEMA 5
Se desea evaluar la disolucin del producto Diclofenac Sdico, tabletas de liberacin prolongada (dosis: 75 mg). Las
condiciones codificadas son:
Aparato 2 (paletas), 900 ml de buffer fosfato pH 6,8, 50 rpm.
Tolerancia: A los 15 minutos, debe disolverse entre el 10 y el 25% SVD del pa, y a las dos horas debe disolverse ms del 85%
SVD del pa.
Preparacin de la solucin de referencia (SR): transferir alrededor de 65 mg de Diclofenac Sdico SR (ttulo 97,1% stdc)
exactamente pesado a un matraz de 100 ml, llevar a volumen con agua. Realizar una dilucin 3:100 tambin con agua
y leer la absorbancia a 276 nm.
Preparacin de las muestras: a los tiempos correspondientes, extraer 10 ml de cada vaso, centrifugar 5 min. a 2500
rpm y a partir del sobrenadante realizar una dilucin adecuada con agua. Leer la abs a 276 nm.
39
CONTROL DE CALIDAD DE MEDICAMENTOS ENSAYO DE DISOLUCIN
Compr.
Peso
1
2
3
4
5
6
SR
121,2
122,5
120,8
118,7
119,2
121,9
65,4
15 min
SIN DILUIR
0,411
0,489
17,83%
20,00%
21,31%
20,15%
2 horas
DILUCIN 3:10
0,487
0,495
79,08%
81,11%
77,83%
74,79%
0,511
a. Realiza los clculos correspondientes para
evaluar si el lote analizado cumple o podra cumplir
con el ensayo de disolucin codificado.
Si el producto a analizar fuera Diclofenac Sdico, tabletas de liberacin retardada (dosis: 75 mg) y el ensayo codificado
fuera el siguiente:
Disolucin <711> Formas farmacuticas de liberacin retardada, mtodo B:
1. Etapa cida: 2 hs en HCl 0,1 N, 900 ml, aparato 2 (paletas), 50 rpm.
Tolerancia: No debe disolverse ms del 10% SVD.
2. Etapa Buffer: buffer fosfato pH 6,8, 900 ml, aparato 2, 50 rpm.
Tolerancia: Q45 = 75%
b.
c.
Cmo procederas para realizar el ensayo?
En funcin de tu respuesta anterior, cmo calcularas el %Disuelto durante la etapa buffer? tendras en cuenta
masa de pa retirada anteriormente? en qu volumen?
PROBLEMA 6
Se realiza un estudio comparativo sobre dos especialidades medicinales del mercado con la siguiente frmula:
Pa ..............................................
Excip. csp...................................
12,5 mg
100 mg
Se analiz un lote de cada producto obtenindose los siguientes resultados:
Nota: todos los mtodos fueron convenientemente validados.
Ensayos realizados
Identificacin del pa
Valoracin del pa (HPLC)
Lte. de aceptacin: 90-110% SVD
Uniformidad de Dosis
Ensayo de disolucin:
Aparato: 1 (canastillo), 50 rpm
Medio: agua, 900 ml
Tolerancia Q45: 75%SVD
Peso
103,2
98,6
99,3
100,5
100,2
99,9
Marca A
cumple
99,2% SVD
cumple
cumple
Marca A
Abs. 45
0,498
0,511
0,518
0,519
0,510
0,514
Marca B
cumple
106,5% SVD
cumple
cumple
Peso
106,2
101,2
100,5
100,9
99,8
99,7
Marca B
Abs. 45
0,478
0,456
0,461
0,251
0,358
0,454
40
CONTROL DE CALIDAD DE MEDICAMENTOS ENSAYO DE DISOLUCIN
Preparacin de la solucin de referencia: se pesaron 15,9 mg de SR (99,2% sdtc) y se llevaron a 50 ml con medio. Se
realiz una dilucin 1:25 de esa solucin, y su absorbancia a 331 nm fue de 0,563.
Preparacin de la muestra: se toman 10 ml del medio de disolucin a los 45 minutos, se centrifuga y se lee la
absorbancia a 331 nm sin diluir las muestras.
a.
b.
Analiza los resultados obtenidos.
Cumplen ambos productos con el ensayo de disolucin? Podran cumplir?
PROBLEMA 7
Se realiza el control de calidad de una especialidad conteniendo Enalapril Maleato (EM) e Hidroclortiazida (HTZ) en
su forma farmacutica comprimidos, con la siguiente formulacin:
Enalapril Maleato ..................................... 10 mg
Hidroclorotiazida ..................................... 25 mg
Excipientes csp . ....................... 150 mg
Ensayo de Disolucin:
Medio: agua, 900 ml
Aparato 2; rpm 50; tiempo 30 min
Tolerancia: debe disolverse en 30 minutos no menos del 80% (Q) de la cantidad declarada de Enalapril Maleato y no
menos del 65% de la cantidad declarada de Hidroclorotiazida.
Cuantificacin del EM disuelto (HPLC-UV, USP 34)
Preparacin de la SR de EM: se pesan 10,5 mg de SR de EM (98,9% sdtc), se disuelven en matraz de 25 ml con buffer,
de esta solucin se toman 0,6 ml y se completa a volumen con buffer en matraz de 25 ml, la solucin se filtra y se
inyecta por triplicado en el HPLC. Resultados: 61533 61570 61550.
Preparacin de la muestra: a los 30 min, se toman 10 ml de cada vaso de disolucin, se filtran y se inyecta en el HPLC.
Cuantificacin de la HTZ disuelta (UV directo a 320 nm, USP 34)
Preparacin de la SR de HTZ: se pesan 15 mg de HTZ SR (99,3% sdtc), se disuelven con metanol en matraz de 25 ml, se
toma 0,1 ml y se completa a volumen en matraz de 10 ml con medio de disolucin, se lee la absorbancia a 320 nm,
resultando 0,597.
Preparacin de la muestra: a partir de la muestra de los 30 minutos se toman 3 ml y se completa a volumen en matraz
de 10 ml con medio de disolucin, se centrifuga 5 min a 2500 rpm y se lee la absorbancia a 320 nm. Resultados:
Enalapril Maleato
Compr.
Area
1
62192
2
64756
3
62833
4
64115
5
62835
6
62197
a.
b.
Hidroclorotiazida
Compr.
Abs
1
0,507
2
0,605
3
0,499
4
0,610
5
0,611
6
0,590
Cumple la partida el ensayo? Justifica.
Qu otros ensayos deberas realizar para evaluar la calidad del producto?
41
CONTROL DE CALIDAD DE MEDICAMENTOS ENSAYO DE DISOLUCIN
PROBLEMA 8
Se desea realizar el ensayo de disolucin al producto Omeprazol, cpsulas de liberacin retardada (dosis 20 mg). Al
buscar en la farmacopea, se encuentra codificado el siguiente ensayo:
1. Etapa cida: 900 ml de HCl 0,1 N; Aparato 1 (canastilla); 100 rpm; 2 horas.
2. Etapa Buffer: 900 ml de buffer fosfato 0,05 M pH 6,8; Aparato 1; 100 rpm - Tolerancia: Q45 = 75%
Se realiza el ensayo de las cpsulas en las condiciones detalladas, y transcurridas las 2 horas en medio cido el mismo
se retira y se reemplaza por el medio buffer, continuando la prueba 45 minutos ms.
Preparacin de las muestras:
Etapa cida: se toma de cada vaso una alcuota a las 2 hs, se centrifuga y se lee directamente la absorbancia del
sobrenadante a 305 nm.
Etapa buffer: se toma de cada vaso una alcuota a los 45 min, se centrifuga y se realiza una dilucin 3:25 del
sobrenadante con buffer fosfato pH 6,8. Se lee la absorbancia a 305 nm.
Preparacin de la solucin de SR:
Se pesan 22,1 mg de la SR (99,4% sdtc) y se disuelven en 100 ml de metanol, se sonica durante 10 min. A partir de all
se realiza una dilucin 1:100 con el medio de disolucin correspondiente (HCl y buffer fosfato pH 6,8) y se lee la
absorbancia a 305 nm.
Peso cpsula (mg)
277,2
284,2
276,0
281,0
261,0
266,1
SR
Abs 2 hs (HCl)
0,354
0,321
0,297
0,361
0,327
0,288
0,426
Abs 45 min (pH 6,8)
0,410
0,399
0,397
0,403
0,400
0,407
0,445
a. Realiza los clculos para determinar si las cpsulas cumplen con el test de disolucin
b. Qu consecuencias podra tener, al tratarse de un producto de liberacin retardada, que el producto no
cumpliera con lo establecido para la etapa cida?
42
CONTROL DE CALIDAD DE MEDICAMENTOS UNIFORMIDAD DE UNIDADES DE DOSIFICACIN
8. UNIFORMIDAD DE UNIDADES DE DOSIFICACIN
PROBLEMA 1
Durante el control de calidad de una especialidad medicinal en su forma farmacutica comprimidos con la siguiente
formulacin:
Pa ....................................50 mg
Excipientes csp..175 mg
Se realizaron los ensayos que se detallan a continuacin, obtenindose los siguientes resultados:
Valoracin (mtodo HPLC-UV validado): 107,3 % SVD especificacin USP 32 (90 - 120% SVD)
Ensayo de disolucin: cumple en etapa S1
Ensayo de uniformidad de dosis
Preparacin de la solucin de la SR: 41,5 mg de pa SR (97,6% sdtc), se disuelven en un matraz de 25 ml con agua grado
HPLC, y a partir de esa solucin se mide 1 ml y se completa a volumen en matraz de 10 ml con el mismo medio. Se filtra
y se inyecta por triplicado en el cromatgrafo, obtenindose las siguientes reas: 93725 - 94008 93742.
Preparacin de la muestra: se pesa cada comprimido y se trasvasa a un matraz de 50 ml, se adicionan 30 ml de agua,
se sonica durante 15 minutos y se completa a volumen con dicho medio. Se centrifuga durante 10 minutos a 5000 rpm
y a partir del sobrenadante se miden 1,5 ml y se completa a volumen en matraz de 10 ml con agua grado HPLC. Cada
muestra as obtenida se filtra y se inyecta por duplicado en el cromatgrafo, obtenindose los siguientes resultados:
Comprimido
1
2
3
4
5
6
7
8
9
10
a.
b.
c.
Peso Compr. (mg)
176,4
177,2
175,6
177,4
175,9
179,3
178,5
177,6
175,8
176,9
Area (n=2)
94693,7
98169,0
99906,7
95562,5
102513,0
92956,4
90378,0
103381,2
92521,9
100427,5
Crees que el mtodo empleado para el ensayo de UUD fue el correcto? Justifica.
A partir de los resultados obtenidos, cumple el lote analizado con las especificaciones de USP? y con las de FA?
Qu podras decir acerca de la calidad del mismo?
PROBLEMA 2
Un farmacutico recibe una consulta sobre el producto Diclofenac sdico 50 mg, sobres para reconstituir, por
referir el paciente variabilidad en la respuesta teraputica luego de la administracin.
Acorde a la frmula cuali-cuantitativa declarada, cada sobre monodosis contiene:
Diclofenac Na ............................50 mg
Excipiente csp.............................2 g
43
CONTROL DE CALIDAD DE MEDICAMENTOS UNIFORMIDAD DE UNIDADES DE DOSIFICACIN
a.
Qu ensayos de control de calidad ms relevantes realizaras para poder definir si existe correlacin entre
calidad del producto y la variabilidad en la respuesta teraputica manifestada por el paciente? Justifica por qu
realizara los mismos.
b.
Realizada la UUD del producto, se obtienen los resultados que se muestran en la tabla. En funcin de los mismos,
Qu opinin te merece el producto, y qu concluyes acerca de lo consultado por el paciente?
Valoracin del pa: 95% SVD (lmites: 90 - 110% SVD
expresado como Diclofenac Na USP 34)
Uniformidad de Dosis (Mtodo UV; : 275 nm; medio: NaOH 0,1 N)
Preparacin de la Solucin de SR: en un matraz de 50 ml se pesan 50 mg de SR (99,0%
sdtc de Diclofenac Na), se disuelve y se lleva a volumen con medio. Se sonica 10 min,
se toman 2 ml y se lleva a 50 ml con medio. Cuando se lee su abs a 275 nm, se obtiene
un valor de 0,650.
Preparacin de la muestra: para cada uno de los 10 sobres individuales, se coloca el
contenido en un matraz de 100 ml, se disuelve y se lleva a volumen con medio. Luego
se sonica 10 min, se centrifuga y se realiza una dilucin 2:25 a partir del sobrenadante.
Peso (g)
2,0
1,6
1,7
2,0
2,0
1,6
1,6
2,0
2,0
1,6
Abs 275 nm
0,690
0,540
0,582
0,687
0,683
0,549
0,551
0,681
0,690
0,551
PROBLEMA 3
Se realiza el ensayo de Uniformidad de Dosis sobre dos productos A y B, ambos conteniendo Fenitona 100 mg en su
forma farmacutica cpsulas. Previamente se realiz la valoracin del principio activo (por el mismo mtodo
analtico) encontrndose los dos productos dentro del lmite de aceptacin establecido por la USP 34 (90 - 110% SVD).
Producto A:
Fenitona (como fenitona sdica) ................100 mg
Excipiente csp................................................200 mg
Producto B:
Fenitona (como fenitona sdica)................100 mg
Excipientes csp..............................................300 mg
Protocolo y resultados: Mtodo analtico: HPLC convenientemente validado
PRODUCTO A:
Preparacin de SR: se disuelven 52,6 mg de SR (95% de fenitona base sdtc) en 50 ml de fase mvil. Se toman 2 ml y se
lleva a 100 ml con fase mvil. Se filtra y se inyecta por triplicado.
Preparacin de la muestra: de un pool del contenido de 10 cpsulas se pesa exactamente una cantidad de polvo
equivalente a 100 mg de pa, se disuelve con 100 ml de fase mvil, se sonica 10 minutos y se centrifuga. Se toman 2 ml
de sobrenadante y se llevan a 100 ml con fase mvil. Se filtra y se inyecta por triplicado. La muestra se prepara por
triplicado.
Peso del contenido de las cpsulas (mg): 222 - 174 - 198 - 218 - 188 - 178 - 176 - 222 - 178 178.
Resultados:
44
CONTROL DE CALIDAD DE MEDICAMENTOS UNIFORMIDAD DE UNIDADES DE DOSIFICACIN
M1
M2
M3
SR
Peso (mg)
200
205
214
52,6
Area Media
18899
19440
20100
18650
Nota: El rea media indicada en la tabla corresponde al valor medio obtenido con tres inyecciones.
PRODUCTO B
Preparacin de la solucin de SR: se disuelven 52,6 mg de SR
(95% de fenitona base sdtc) en 50 ml de fase mvil. Se
toman 2 ml y se lleva a 100 ml con fase mvil. Se filtra y se
inyecta por triplicado.
Preparacin de la muestra: cada una de 10 cpsulas se trata
individualmente de la siguiente manera: se coloca el
contenido de la cpsula en un matraz de 100 ml, se agrega
fase mvil, se sonica 10 minutos y se lleva a volumen con
fase mvil. Posteriormente se sonica nuevamente 10. Se
centifuga. Se toman 2 ml de sobrenadante y se llevan a 100
ml con fase mvil. Se filtra y se inyecta por triplicado. Los
resultados se muestras en la tabla.
a.
b.
c.
Cp.
Peso del contenido (mg)
rea Media
284,7
17705
285,0
17754
251,0
15652
285,0
17729
252,0
15677
285,6
17761
284,0
17688
252,0
15675
285,0
17747
10
252,0
15674
SR
52,6
18650
Crees que los mtodos para realizar la UUD fueron elegidos correctamente para cada producto?
Analiza todos los resultados en su conjunto y establece si detectas un problema, y cul sera la medida correctiva
apropiada.
Cul sera la consecuencia sobre la respuesta teraputica de un paciente, que se encuentra en tratamiento
crnico y estabilizado con otra especialidad medicinal que contiene esta misma droga (de estrecha ventana
teraputica) en la misma concentracin y forma farmacutica, si se le administra uno de estos dos productos?
Justifica.
PROBLEMA 4
En un laboratorio de control de calidad se realiz el ensayo de Uniformidad de Unidades de Dosificacin (UUD) a un
lote de una especialidad medicinal en su forma farmacutica comprimidos con la siguiente composicin:
Pa ...... 500 mg
Excip csp .. ..800 mg
Especificacin de contenido: [90-110 % SVD]
Para llevar a cabo el ensayo se procedi de la siguiente manera:
Mtodo analtico: espectrofotometra UV directa (=276 nm). Medio: agua destilada
Preparacin de la solucin de la Sustancia de Referencia: se pesaron exactamente alrededor de 20 mg de pa SR (98,6%
sdtc) se trasvasaron a un matraz de 100 ml, se disolvieron en 25 ml de agua destilada y se sonicaron 10 min. Se dej
reposar la solucin 15 min y se complet a volumen con dicho medio. Posteriormente se realiz una dilucin 3:100
con agua destilada y se ley la absorbancia a =276 nm.
45
CONTROL DE CALIDAD DE MEDICAMENTOS UNIFORMIDAD DE UNIDADES DE DOSIFICACIN
Preparacin de la muestra: se pesaron individualmente 10 comprimidos (794,16; 754,05; 860,27; 715,73; 730,41; 779,32;
803,78; 801,82; 858,39; 831,49) y se realiz un pool a partir de los mismos. A continuacin se pesaron tres alcuotas
del polvo, cada una de las cuales se trasvas a un matraz de 100 ml. Se adicionaron 50 ml de agua destilada y se sonic
durante 20 min. Se dej reposar la suspensin 15 min y se complet a volumen con dicho medio. Se centrifug una
porcin de la misma y a partir del sobrenadante se realiz una dilucin 3:100 con agua destilada, luego de lo cual se
ley la absorbancia a =276nm.
Los resultados obtenidos se detallan en la siguiente tabla:
a.
b.
Alicuota N
Peso (mg)
1
2
3
SR
32,16
32,11
31,81
20,6
Absorbancia =276nm
0,608
0,609
0,610
0,612
Calcula los %SVD de cada una de las 10 unidades de dosificacin evaluadas.
Indica si el lote cumple el ensayo de UUD segn FA VII Ed y segn USP 35.
PROBLEMA 5
En un laboratorio de especialidades medicinales multinacional, instalado en Argentina, se efectu el control de
calidad de una especialidad farmacutica en su forma comprimidos con la siguiente formulacin:
pa 20 mg
Excipientes csp..100 mg
Se realizaron los ensayos que se detallan a continuacin, obtenindose los siguientes resultados:
-
Valoracin (mtodo: espectrofotometra UV directa validado): 90,30% SVD.
Especificaciones USP 34: 90 110% SVD
Ensayo de disolucin: cumple en S3
Ensayo de uniformidad de unidades de dosificacin:
Preparacin de la solucin de pa SR: se pesaron 28,5 mg de pa SR (98,7 % sdtc) se disolvieron en un matraz de 100 ml
con agua destilada. A partir de esta solucin, se efectu una dilucin 1,5:25 con dicho medio. La absorbancia a 314 nm
fue 0,623.
Preparacin de las muestras: se pesaron individualmente 10
comprimidos y se trasvas cada uno a un matraz de 50 ml. Se
adicionaron 30 ml de agua destilada. Se sonic 10 minutos. Se
complet a volumen con el mismo medio. Una porcin de esta
solucin se centrifug durante 10 minutos a 2500 rpm y a partir del
sobrenadante se realiz una dilucin 1:25 con el mismo medio. Cada
muestra as obtenida se ley al UV a 314 nm.
a.
b.
Comp n
1
2
3
4
5
6
7
8
9
10
Peso Comp. (mg)
100,1
100,0
99,9
100,2
108,0
101,0
99,8
100,0
101,2
100,0
Abs
0,505
0,501
0,506
0,503
0,507
0,505
0,504
0,512
0,505
0,506
Indica si el mtodo empleado segn FA VII Ed y USP 34 fue
correcto. Justifica
A partir de los resultados obtenidos, cul debera ser la actitud del Departamento de Control de Calidad del
laboratorio respecto de la calidad de la especialidad? Por qu?
46
CONTROL DE CALIDAD DE MEDICAMENTOS HPLC
9. HPLC
PROBLEMA 1
Para realizar la valoracin del producto Difenhidramina Clorhidrato 0,25 g/100 ml Jarabe se recurre a la FA 8 y se
encuentra codificada la solucin oral, para la cual se especifica lo siguiente:
Especificacin: la solucin oral de Clorhidrato de Difenhidramina (DFH.HCl) debe contener no menos de 90 y no ms de
110% de la cantidad declarada de C17H21NO.HCl.
VALORACIN:
Sistema cromatogrfico: emplear un equipo de HPLC-UV con deteccin a 254 nm, con una columna de 250 mm x 4,6
mm con fase estacionaria constituida por grupos nitrilo qumicamente unidos a partculas porosas de slice de 3 a 10 m
de dimetro. Caudal: 1,0 ml/min. Fase mvil: metanol, agua y trietilamina (50:50:0,5). Ajustar a pH 6,5 con cido actico
glacial. Filtrar y desgasificar.
Preparacin de la solucin de referencia: disolver una cantidad exactamente pesada de DFH.HCl SR en agua para
obtener una solucin de aproximadamente 0,5 mg/ml.
Preparacin de la muestra: transferir un volumen exactamente medido de la solucin oral de DFH.HCl, equivalente a 50
mg de DFH.HCl, a un matraz de 100 ml, completar a volumen con agua y mezclar.
Siguiendo dicha tcnica, se analizan muestras provenientes del
jarabe (dos inyecciones por muestra), y se obtiene los siguientes
resultados:
Muestra
1
2
3
4
SR*
Volumen (ml)
20
20
20
20
rea (n=2)
162965
158769
163257
160854
126358
* Se pesaron 24,7 mg de SR (97,32% stdc) y se llevaron a 50 ml
Cuando se analizan los cromatogramas
obtenidos, se observa lo siguiente:
250
Jarabe
SR
200
150
100
50
0
0
10
15
20
a. Realiza tus cuentas y calcula el contenido de DFH.HCl en el jarabe. Cumple con la especificacin?
b. Intenta explicar los resultados en funcin de lo que observas en el cromatograma.
c. Qu parmetro de validacin deberas analizar? (observa que, aunque se trata de un mtodo farmacopeico,
dicho parmetro siempre debe evaluarse... por qu?).
47
CONTROL DE CALIDAD DE MEDICAMENTOS HPLC
PROBLEMA 2
En un laboratorio, se pone a punto la siguiente tcnica para la determinacin de la droga Carbamacepina (CBZ) en
muestras salivales de pacientes:
Sistema Cromatogrfico: columna LiChrospher 60 RP-Select B 250x4 mm, 5 m (Merck, Darmstadt, Alemania). Se trabaj
de manera isocrtica a 0,8 ml/min. Deteccin UV a 220 nm
Fase mvil: mezcla de buffer KH2PO4 (10 mM, pH 7,0): acetonitrilo: tetrahidrofurano: isopropanol (63:29:5:3 en volumen),
desgasificada y filtrada por membrana de nylon de 0,45 m. Los solventes utilizados eran calidad HPLC.
Soluciones madre o stock:
Carbamazepina: se pesaron 13,2 mg de CBZ sustancia de referencia (98,42% sdtc), se colocaron en un matraz de 100
ml, se adicionaron alrededor de 60 ml de metanol, se sonic hasta disolucin completa de la droga y se llev a
volumen con metanol. Esta solucin, conservada en freezer, se mantiene estable por al menos 6 meses.
Nitrazepam ( NTZ): se pesaron 25,8 mg de NTZ sustancia de referencia (99,23% sdtc), se colocaron en un matraz de
100 ml, se adicionaron alrededor de 60 ml de metanol, se sonic hasta disolucin completa de la droga y se llev a
volumen con metanol. Esta solucin, conservada en freezer, se mantiene estable por al menos 6 meses.
Preparacin de la solucin de referencia: sobre 0,5 ml de saliva blanco (matriz biolgica limpia, sin droga) se adicionaron
20 l de la solucin stock de CBZ, 15 l de la de NTZ y 2 ml de acetato de etilo. Se agit en vortex durante 1 min y se
centrifug a 3500 rpm 10 min. Se separ el sobrenadante y se evapor hasta sequedad bajo corriente de N 2 a 40 C en
bao de agua. El residuo obtenido se resuspendi en 250 l de fase mvil (sin tetrahidrofurano), se centrifug 10 min a
13000 rpm y por ltimo se inyectaron 20 l en el cromatgrafo.
Preparacin de las muestras: idem anterior, sin el agregado de solucin stock de CBZ.
Luego de la aplicacin del mtodo sobre la muestra de un paciente, se obtuvieron los siguientes resultados (las reas
de la tabla son el promedio de 2 inyecciones, y las tres muestras preparadas corresponden a tres rplicas del mismo
paciente):
Muestra
SR
M1
M2
M3
a.
b.
c.
d.
Area CBZ
63257
48635
53698
59301
Area NTZ
45201
35751
40056
43668
De qu mtodo de cuantificacin se trata? Por qu crees que se eligi dicho mtodo?
Realiza las cuentas para conocer la concentracin salival de CBZ en el paciente.
Repite tus clculos sin tener en cuenta el agregado de NTZ (como si fuera un mtodo con estndar externo).
Qu diferencia principal encuentras?
Qu caractersticas debe poseer la sustancia elegida como estndar interno?
PROBLEMA 3
Se desea realizar la valoracin de la materia prima Doxorubicina Clorhidrato (DoxHCl), por lo que se recurre a la
farmacopea USP 30 y se encuentra el siguiente mtodo:
48
CONTROL DE CALIDAD DE MEDICAMENTOS HPLC
Fase mvil: preparar una mezcla de agua, acetonitrilo, metanol y H 3PO4 (540/290/170/2). Disolver 1 g de Lauril Sulfato de
Na en 1 L de dicha solucin, ajustar el pH a 3,6 0,1 con NaOH 2 N y desgasificar.
Solucin de resolucin: disolver alrededor de 10 mg de DoxHCl en 5 ml de agua, agregar 5 ml de cido fosfrico y dejar
reposar 30 minutos. Ajustar a pH 2,6 0,1 con NaOH 2 N (alrededor de 37 ml), agregar 15 ml de acetonitrilo y 10 ml de
metanol, mezclar y filtrar.
Solucin de referencia: disolver una cantidad exactamente pesada de sustancia de referencia de DoxHCl en fase mvil,
para obtener una solucin de concentracin aproximada 100 g/ml.
Solucin de muestra: transferir alrededor de 20 mg de DoxHCl materia prima (exactamente pesados) a un matraz de 200
ml, agregar fase mvil y mezclar.
Sistema cromatogrfico: emplear una columna con relleno L13, de 4,6 x 25 cm, fijar el detector a 254 nm y el flujo en 1,5
ml/min.
Inyectar la solucin de referencia y verificar que:
El factor de tailing para el pico de Doxorubicina se encuentre entre 0,7 y 1,2
La eficiencia de la columna (determinada para el pico de la Dox) sea > 2250 platos tericos
El CV para inyecciones repetidas de la misma solucin no sea mayor al 1%
Por otro lado, inyectar la solucin de resolucin, y verificar que:
Los tiempos de retencin relativos sean alrededor de 0,6 para Doxorubicinona y 1,0 para Dox
La resolucin (Rs) entre ambos picos no sea menor que 5,5
Los cromatogramas a continuacin corresponden a la solucin de referencia y a la de resolucin, y en la tabla se
muestran los resultados luego de 5 inyecciones de la solucin de referencia.
180
Solucin de Referencia
180
160
160
140
140
120
120
100
100
80
80
60
60
40
40
20
20
0
0
a.
b.
c.
d.
Solucin de Resolucin
8 10 12 14 16 18 20 22 24 26 28
8 10 12 14 16 18 20 22 24 26 28
Por qu se deben realizar las verificaciones de asimetra, eficiencia, resolucin, CV? Cmo se denomina dicho
procedimiento?
Inyec.
PH
En particular, qu objetivo tiene la preparacin de la solucin de resolucin?
1
60909
Crees que el sistema cromatogrfico es apto para ser usado en la valoracin
2
60830
propuesta?
3
61003
En funcin de tus resultados, qu crees que se debera mejorar? Plantea posibles
4
60992
acciones correctivas.
5
60879
49
CONTROL DE CALIDAD DE MEDICAMENTOS HPLC
PROBLEMA 4
Al consultar la monografa correspondiente a raz de Angelica sinensis en la farmacopea britnica (BP 2009), se
encuentra la siguiente informacin:
Raz de Angelica Sinensis
Definicin: es la raz seca entera de Angelica sinensis (Oliv.) Diels. (Angelica polymorpha Maxim. var. sinensis Oliv.).
Contiene al menos 0,1% de Z-ligustilida (C12H14O2), calculada sobre base seca.
Prdida por secado: al secarse a 100 - 105C durante 2 hs, la prdida de peso no supera el 12% (usar 1 g).
Valoracin - Se realiza por HPLC empleando las siguientes soluciones:
(1) Reducir a polvo fino alrededor de 5,0 g de la droga, y transferir 0,5 g del polvo a un matraz de 25 ml. Agregar 20
ml de metanol, sonicar en bao de hielo durante 100 minutos, dejar llegar a tempertura ambiente y llevar a volumen
con metanol. Centrifugar 5 min a 5000 rpm. Separar el sobrenadante, filtrar (0,45 m) e inyectar.
(2) 0,025% p/v de Z-ligustilida R en acetonitrilo.
CONDICIONES CROMATOGRFICAS
(a) Columna: RP-18 (15 cm 4,6 mm, 5 m).
(b) Elucin isocrtica con una mezcla de 8 volumes de agua y 12 volumes de acetonitrilo como fase mvil.
(c) Flujo = 1 ml/min
(d) Deteccin a 350 nm.
(e) Injectar 10 l de cada solucin.
APTITUD DEL SISTEMA
Inyectar la solucin (2) al menos 5 veces. El test es vlido si el CV del rea de pico correspondiente a Z-ligustilida es
menor al 3,0%, y el CV entre los tiempos de retencin del mismo pico tambin es menor al 3,0%. La eficiencia de la
columna debe ser mayor o igual a 5000 platos tericos, determinada en el pico de Z-ligustilida, y el factor de
simetra del mismo pico es menor o igual a 1,3.
Inyectar la solucin (1). El test es vlido si el factor de resolucin entre el pico de Z-ligustilida y el pico ms cercano
(retencin relativa alrededor de 0,9 respecto a Z-ligustilida) es mayor o igual a 1,5.
Se procede a realizar los ensayos de prdida por secado y valoracin, obteniendo los siguientes resultados:
Prdida por secado
Peso (g) antes del ensayo
Peso (g) a las 2 horas
Cpsula 1
0,9875
0,8895
Cpsula 2
1,0250
0,9265
Cpsula 3
1,0181
0,9168
Valoracin
Referencia (Solucin 2): se pesaron 24,8756 mg de Z-ligustilida R (94,23% sdtc) y se disolvieron en 100 ml de
acetonitrilo
Muestra (Solucin 1): se pulverizaron 5,2698 g de la droga hasta convertirla en polvo fino. A partir de all, se tomaron
aprox 0.5 g (por triplicado), se colocaron en un matraz, se adicionaron 20 ml de MeOH y se sonic 2 hs a 0 C. Al llegar
a temperatura ambiente se llev a 25 ml con MeOH, se centrifug 10 min a 5000 rpm, se filtr y se inyect en el
cromatgrafo.
Referencia 1 Inyec.
Tiempo de
ret. (min)
9,42
rea
212,39
Inicio de
pico (min)
9,21
Fin de pico
(min)
9,69
Factor de Simetra
1,22
50
CONTROL DE CALIDAD DE MEDICAMENTOS HPLC
Referencia 2 Inyec.
9,42
213,05
9,2
9,70
1,17
Referencia 3 Inyec.
Referencia 4 Inyec.
Referencia 5 Inyec.
9,43
9,41
9,43
215,74
214,57
211,5
9,27
9,18
9,22
9,79
9,67
9,72
1,19
1,28
1,21
8,48
9,42
8,48
9,43
8,47
9,41
12,36
102,87
15,46
118,43
14,02
110
8,28
9,2
8,3
9,22
8,3
9,17
8,87
9,7
8,91
9,74
8,9
9,69
SC 1 (1)
0,4961 g
SC 1 (2)
0,5341 g
SC 1 (3)
0,5123 g
Pico 1
Pico 2
Pico 1
Pico 2
Pico 1
Pico 2
a. Cumple la droga con los requerimientos farmacopeicos de contenido y prdida por secado?
b. Establece la validez del anlisis por HPLC (adecuabilidad del sistema)
c. Si el contenido de agua de la droga aumenta, el resultado expresado en base seca, aumenta o disminuye?
PROBLEMA 5
Se desea valorar el siguiente producto:
Betametasona (como Valerato).. 0,10 g
Excipientes csp. 100 g
PM Betametasona = 392,46
PM Betametasona Valerato = 476,59
Se va a seguir la tcnica descripta en la USP 38, la cual incluye las siguientes soluciones:
Solucin de Estndar Interno (SI): se pesaron 40,1 mg de Beclometasona Dipropionato (98,3% sdtc) y se llevaron a
100 ml en un matraz volumtrico con una solucin de cido actico glacial en metanol (1 en 1000).
Soluciones de Referencia: se pes una cantidad adecuada de Betametasona SR (97,24% sdtc), la cual se coloc en un
matraz de 50 ml y se llev a volumen solucin de cido actico glacial en metanol (1 en 1000). Se transfirieron 5 ml de
dicha solucin a un recipiente adecuado, en el cual se adicionaron 10 ml de la solucin SI.
Solucin Test: transferir una porcin de crema pesada con exactitud, que equivalga aproximadamente a 2,0 mg de
Betametasona, a un tubo de centrfuga de 50 ml (por triplicado). Agregar 10 ml de la solucin del SI y 5 ml de una
solucin 1:1000 de cido actico glacial en metanol. Tapar el tubo, y colocar en un bao de agua a 60 C hasta que
funda la muestra. Retirar del bao y agitar vigorosamente hasta que la muestra vuelva a solidificarse. Volver a calentar
y agitar dos veces ms. Colocar el tubo en un bao de hielo-metanol durante 20 min, centrifugar a continuacin para
separar las fases. Decantar el sobrenadante transparente en un matraz con tapa adecuado y dejar que llegue a
temperatura ambiente.
Luego de filtrar todas las soluciones, las mismas se analizan en las condiciones cromatogrficas indicadas en la
monografa. Resultados:
SC 1
SC 2
SC 3
SC 4
SC 5
Peso Betametasona SR
rea SR
rea SI
11,4
15,9
21,56
43,2
65,7
3951
6371
8421
16549
26945
7023
7423
7058
6458
7057
M1 (2,013 g)
M2 (2,163 g)
M3 (2,214 g)
rea Betametasona
rea SI
8763
8677
8903
7452
7089
7008
51
CONTROL DE CALIDAD DE MEDICAMENTOS HPLC
a.
Si la especificacin establece que la crema de Valerato de Betametasona debe poseer entre un 90 110% de la
cantidad declarada de Betametasona, cumple la droga con el ensayo de valoracin?
b. Cmo habra sido el resultado de no haber trabajado con SI?
PROBLEMA 6
Se desea realizar el ensayo de Sustancias Relacionadas de la materia prima Hidroclorotiazida (HCTZ). Para ello se
recurre a la farmacopea USP 34 y se encuentra el siguiente mtodo:
Sistema cromatogrfico: columna RP-18 de 4,6 mm x 5 cm y 3,5 m, a 35 C. La velocidad de flujo es 1 ml/min y la
longitud de onda de deteccin es 275 nm.
Diluyente: mezcla de buffer NaH2PO4 pH = 2,7 y Acetonitrilo (7:3).
Solucin A: mezcla desgasificada de acetonitrilo y metanol (3:1).
Solucin B: cido frmico anhidro en agua (5 en 1000). Desgasificar.
Fase Mvil:
Tiempo (min)
0
05
5 14
14 18
18 20
%Solucin A
3
3
3 36
36 3
3
%Solucin B
97
97
97 64
64 97
97
Elucin
Equilibrio
Isocrtica
Grad. Lineal
Grad. Lineal
Re-equilibrio
Solucin de aptitud del sistema: disolver cantidades apropiadas de HCTZ SR, Clorotiazida SR (CT) y Compuesto
Relacionado A de Benzotiadiazina SR (CR-A) en diluyente, sonicar si es necesario y diluir para obtener una solucin
que contenga aproximadamente 0,32 mg/ml de HCTZ y 0,0032 mg/ml de las otras dos SR. Filtrar.
Preparacin estndar: dem anterior (HCTZ SR 0,32 mg/ml), sin CT ni CR-A.
Solucin de prueba: transferir aproximadamente 32 mg de HCTZ, pesados con exactitud, a un matraz de 100 ml.
Agregar alrededor de 70 ml de diluyente, sonicar 10 minutos, dejar enfriar y completar a volumen. Filtrar.
Procedimiento:
1.
2.
Inyectar la solucin de aptitud del sistema y registrar las respuestas de los picos. Los tiempos de retencin
relativos son aproximadamente 0,5 para CR-A, 0,8 para CT y 1 para HCTZ. La resolucin (R) ente CR-A y CT no es
menor a 2, y entre CT y HCTZ no es menor a 1,5. El factor de asimetra para los tres picos no es mayor a 1,5.
Cromatografiar la preparacin estndar: el CV para inyecciones repetidas no es mayor a 1%.
Inyectar la solucin de prueba, registrar el cromatograma y medir las respuestas correspondientes a todos los
picos observados. Calcular el porcentaje de cada impureza en la porcin de HCTZ tomada con la frmula:
% =
100
En donde Ric es el cociente entre el rea del pico de cada impureza y su factor de respuesta, y Rsc es la suma de los
cocientes de las reas de todos los picos y sus respectivos factores de respuesta, siendo los factores de respuesta
0,54; 0,63 y 1,0 para CR-A, CT y todos los dems picos, respectivamente.
Especificacin: no se encuentra ms del 1% de CR-A y no ms de 0,5% de cualquier otra impureza. No se encuentra
ms de 0,9% de impurezas totales (excluido el CR-A).
52
CONTROL DE CALIDAD DE MEDICAMENTOS HPLC
Luego de aplicar el mtodo descripto (la solucin prueba por duplicado), se obtuvo el siguiente reporte:
Solucin de aptitud del sistema
N pico
1
2
3
Tr (min)
3,3
5,38
6,64
rea
8542
1809
526356
Ancho en la base (min)
0,85
0,51
1,08
Asimetra
1,43
1,13
1,28
Preparacin estndar
1 Iny
2 Iny
3 Iny
Tr (min)
6,639
6,64
6,638
Solucin de prueba
Muestra 1
N pico
Tr (min)
1
3,312
2
4,15
3
5,381
4
6,641
5
8,124
a.
b.
c.
d.
rea
528695
530487
527562
4 Iny
5 Iny
6 Iny
rea
2087
2479
1278
526842
867
N pico
1
2
3
4
5
Tr (min)
6,642
6,641
6,639
rea
531004
529485
529006
Muestra 2
Tr (min)
3,309
4,156
5,378
6,639
8,126
rea
2157
2591
1344
527038
907
Cul es el objetivo de este ensayo?
Por qu crees que el mtodo propone el uso de un gradiente de Fase Mvil?
Cul es el objetivo de la prueba de aptitud del sistema? Cumple este mtodo?
Establece si la materia prima cumple con el ensayo de Sustancias Relacionadas.
PROBLEMA 7
Propone una o ms posibles soluciones a las siguientes situaciones problemticas, explicando brevemente por qu:
Debes analizar una muestra que posee dos seales principales (por ejemplo, un medicamento con dos principios
activos), y los picos obtenidos se solapan (no se resuelven). Propone soluciones que no impliquen cambiar de
columna.
Dispones de un equipo HPLC-UV, y el principio activo que tienes que analizar no absorbe al UV-Vis.
Los picos obtenidos son muy anchos (pierdes resolucin)
La presin es excesiva
Debes analizar una muestra de un nico analito, y con las condiciones que pruebas el tiempo de retencin es 16
minutos (excesivo).
Debes analizar un analito en una matriz muy compleja, por ejemplo plasma
Debes analizar un analito en una matriz que no puedes reproducir, por ejemplo una crema o ungento.
53
CONTROL DE CALIDAD DE MEDICAMENTOS HPLC
54
CONTROL DE CALIDAD DE MEDICAMENTOS ESTABILIDAD
10. ESTABILIDAD
PROBLEMA 1
Con el objetivo de evaluar la estabilidad de la siguiente formulacin:
Pa.... 100 mg
Excip. csp ... 500 mg
Cuya especificacin es 90 110% SVD, se realizaron los correspondientes estudios en condiciones aceleradas,
intermedias y a largo plazo. Resultados:
-
a.
Se observaron cambios significativos en el contenido de pa en condiciones aceleradas
Sin embargo, el estudio en condiciones intermedias no mostr cambios
El estudio a largo plazo cubri un intervalo de 12 meses. Cuando se calcul el tiempo correspondiente a
una degradacin del 90% (mediante el correspondiente IC95%), el mismo resulta ser 22 meses
(extrapolacin)
Acorde al rbol de decisin, qu perodo de vida til solicitaras?
PROBLEMA 2
Un laboratorio se encuentra realizando los estudios de estabilidad de un lote de comprimidos de Ranitidina 150
mg. El estudio de estabilidad acelerado se lleva a cabo a 40 C y 75 % de HR, en los envases primario y secundario
que se han propuesto como definitivos. A tiempos 0, 2, 4 y 6 meses se realiza el ensayo de valoracin del principio
activo intacto; a los 0 y 6 meses se realiza el test de disolucin. Se muestran los resultados a tiempos 0 y 6 meses,
para ambos ensayos.
Valoracin del principio activo:
Tiempo 0: 99,5 % SVD.
Tiempo 6 meses: 99,0 % SVD.
Lmites especificados por USP 26: 90,0 110,0 % SVD.
Mtodo: HPLC validado
Ensayo de disolucin
Tolerancia: Q45 = 80%.
Medio: 900 ml agua destilada.
Aparato: 2 paletas.
Velocidad: 50 rpm.
Tiempo 0
Comprimido
Altura pico
1
43164
2
42679
3
42436
4
43050
5
42560
6
42588
Tiempo 6 meses
Comprimido
Altura pico
1
41322
2
41564
3
41370
4
41709
5
41419
6
41032
Procedimiento: se toman 10 ml de cada vaso, se centrifugan y se realiza una dilucin 2/10. Se filtra y valora.
Referencia: solucin de concentracin 30,69 g/ml - altura pico: 44639
a.
b.
Se modifica la disolucin de los comprimidos a lo largo del estudio de estabilidad acelerada? (test t para dos
muestras, =0,05)
Cmo se denomina este fenmeno? Cmo lo evitaras o solucionaras?
55
CONTROL DE CALIDAD DE MEDICAMENTOS ESTABILIDAD
PROBLEMA 3
A continuacin se presentan los resultados de un estudio de estabilidad a largo plazo realizado sobre tres lotes
(A, B y C, en escala piloto) de comprimidos de Acenocumarol 4 mg, mantenidos a 25 2 C y 60 5% de HR. El
anlisis de la covarianza de dichos datos (ANCOVA) indic que no pueden combinarse las pendientes ni las
ordenadas de las tres rectas.
Tiempo
0
3
6
9
12
18
24
a.
%SVD remanente
Lote A
Lote B
101,58
102,42
99,42
99,67
97,22
97,22
95,64
95,60
93,79
93,04
91,06
90,42
87,81
85,28
Lote C
99,01
98,01
96,18
94,61
93,27
90,33
87,13
Si la especificacin de farmacopea para dicho
producto indica que el contenido debe estar
comprendido entre 90 110% SVD, cmo
procederas para calcular la fecha de vencimiento? Indica la forma grfica, la frmula correspondiente y si
crees que te falta algn dato.
b. A continuacin, calcula el mximo tiempo que te asegurara un contenido de pa dentro del lmite
especificado. Qu perodo de vida til solicitaras?
PROBLEMA 4
a.
Indica qu fecha de vencimiento mxima solicitaras en cada caso (completa la ltima fila de la tabla):
E. Acelerada:
E. Intermedia:
Caso A
Comprimidos
Sin cambios
Sin cambios
Caso B
Materia Prima
Con cambios
Sin cambios
Especificacin:
90 110 %SVD
98 102 %SDA
Estabilidad
a largo
plazo:
Clculo a partir
de la recta:
s(0 )
t(0.05; N-2)
Vto. mximo:
(sin redondear)
b.
c.
Datos hasta 6
meses, sin
cambios en el
contenido de pa
(se acepta H0 de
la correlacin)
Datos hasta 18
meses, se
calcula la recta
de regresin
-----
y0 = 98%
0 = 35,8 meses
----1,895 (N=9)
2,763
1,746 (N=18)
Caso C
Comprimidos
Sin cambios
Sin cambios
90 110 %SVD (pa)
Menor al 1% (impureza A)
Con datos hasta 24 meses, se
calculan las dos rectas de
regresin (para el pa y para la
impureza A)
Para el pa:
Para imp. A:
y0 = 90%
y0 = 1%
0 = 23,2 meses 0 = 21,4 meses
3,68
1,56
1,729 (N=21)
Caso D
Crema
Producto
magistral
elaborado en
la farmacia. A
partir de un pa
cuya fecha de
re-anlisis es
en 2017.
Con qu objetivo se realizan los diferentes tipos de estudios de estabilidad? (degradacin forzada,
estabilidad acelerada, intermedia y a largo plazo)
Si quisieras obtener un perodo de vencimiento mayor para los comprimidos, qu deberas hacer?
56
CONTROL DE CALIDAD DE MEDICAMENTOS ESTABILIDAD
PROBLEMA 5
Para evaluar la fotoestabilidad de un principio activo, un analista prepara las siguientes muestras:
Control 1: Por cuatriplicado, coloca el principio activo en un recipiente qumicamente inerte y transparente, el
cual se conserva en la oscuridad.
Muestra 1: Por cuatriplicado, coloca el principio activo en un recipiente qumicamente inerte y transparente,
expuesto a luz UV (200 watt h/m2) en una cmara adecuada, durante 24 hs.
Los resultados obtenidos (expresados como %sdtc) fueron:
a. Evala si se produjeron cambios significativos entre la
muestra y el control (test t para dos muestras, =0,05)
Rplica
1
2
3
4
Control 1
98,7
99,3
100,0
99,7
Muestra 1
96,3
97,43
97,2
96,1
Posteriormente, le surgen dudas acerca del motivo de las diferencias encontradas entre el control y la muestra.
A raz de ello repite el ensayo, pero ahora con las siguientes condiciones:
Control 2: Por cuatriplicado, coloca el principio activo en un recipiente qumicamente inerte y transparente, el
cual se coloca al lado de la muestra (en la misma cmara, expuesto a la misma luz durante 24 hs) pero envuelto
en papel de aluminio.
Rplica
Control 2
1
98,5
2
99,6
3
98,3
b. Evala si se produjeron cambios significativos entre los controles 1 y 2 (test
4
99,8
t para dos muestras, =0,05)
c.
Por qu crees que el analista dud acerca del origen de la variacin en el contenido de la muestra respecto
al Control 1? Cul crees que es el objetivo del Control 2?
d. Correctamente diseado, el experimento debi realizarse en una etapa, incluyendo ambos controles y la
muestra. En dicho caso, cmo hubiera sido el tratamiento estadstico de los datos? (indica de qu diseo se
tratara, qu ensayo realizaras y cmo procederas en caso de rechazar H0).
PROBLEMA 6
Un laboratorio productor desea establecer el perodo de vida til de producto, en la forma farmacutica
comprimidos, cuya frmula es:
Pa.500 mg
Excip csp. 750 mg
Durante ese perodo, las especificaciones del producto establecen que debe contener 90-110% SVD de pa, y menos
del 0,5% SVD de la sustancia relacionada A (SR-A), producto de degradacin principal que puede resultar txico
en altas concentraciones.
Se realiza entonces un estudio de estabilidad en condiciones normales de conservacin (envase definitivo,
temperatura ambiente) y se determina el porcentaje de SR-A a los tiempos indicados.
Si estudios previos demostraron que el contenido de pa se mantiene superior al 90% hasta por 48 meses, estima
el perodo de vida til del producto de manera que cumpla con ambas especificaciones.
57
CONTROL DE CALIDAD DE MEDICAMENTOS ESTABILIDAD
0,7
y = 0,0193x - 0,0089
0,6
R = 0,9914
0,5
0,4
0,3
0,2
0,1
s( y ) 0,020137
0
10
20
30
-0,1 0
Tiempo (meses)
0
%SVD SR-A
0,0050
0,0032
0,0926
0,1040
12
0,2358
12
0,1876
18
0,3200
18
0,3463
24
0,4836
24
0,4410
30
0,5522
30
0,5887
58
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO I: CALIBRACIN Y VERIFICACIN DE EQUIPOS
ANEXO I. CALIBRACIN Y VERIFICACIN DE EQUIPOS
La Farmacopea Argentina 7a. Ed. (FA 7) define, en su captulo <1020> Buenas Prcticas de Fabricacin y Control, el
trmino Calibracin como:
Conjunto de operaciones que establece, bajo condiciones especificadas, la relacin entre los valores indicados por un
instrumento o sistema de medicin (especialmente de pesada), registro y control, o los valores representados por una
medida material y los correspondientes valores conocidos de un patrn de referencia. Es preciso establecer los lmites
de aceptacin de los resultados de las mediciones
Asimismo, establece que se deben calibrar y revisar los aparatos de medicin, pesaje, registro y control a intervalos
definidos, mediante mtodos apropiados (adecuadamente descriptos en procedimientos operativos para tal fin), y
se debe mantener un adecuado registro de estas verificaciones. Es decir que trabajando bajo GMP, se debe seguir el
siguiente esquema para los principales equipos de laboratorio:
Procedimientos Operativos
(POs) de Calibracin
(periodicidad, metodologa)
CALIBRACIN
Registro de los datos
obtenidos
(fecha, resultado, analista)
Por otro lado hay equipos que, adems del protocolo de calibracin peridica, requieren de control o verificacin
adicional cada vez que van a ser utilizados (ej. pH-metro, algunas balanzas, etc.).
A continuacin se encuentran descriptas algunas de las caractersticas principales de los procedimientos de
calibracin de los equipos que utilizaremos en el trabajo prctico grupal de la materia: pH-metro, espectrofotmetro
UV-Visible y balanza. Se puede encontrar ms informacin sobre estas calibraciones, como as tambin sobre
calibraciones de otros equipos, en las siguientes fuentes bibliogrficas (entre otras):
Centro Espaol de Metrologa (www.cem.es). En su pgina web se pueden encontrar numerosos
procedimientos de calibracin, entre ellos:
- pH-metro (http://www.cem.es/sites/default/files/qu-003_digital.pdf);
- Equipos de HPLC (http://www.cem.es/sites/default/files/qu-004_digital.pdf);
- Masas para balanzas (http://www.cem.es/sites/default/files/me-007_y_me-015_digital.pdf); etc.
Farmacopea de los Estados Unidos (USP 34 y anteriores)
Farmacopea Argentina 7 Ed.
CALIBRACIN DEL PH-METRO
En su captulo general de pH <741>, la USP establece que el pH es definido como el valor dado por un instrumento
potenciomtrico (pH-metro) adecuado y correctamente estandarizado, capaz de reproducir valores de pH de 0,02
unidades empleando un electrodo indicador sensible a la actividad del ion hidrgeno: el electrodo de vidrio, y un
electrodo de referencia adecuado.
El instrumento debe ser capaz de detectar el potencial entre el par de electrodos y, con fines de estandarizacin,
aplicar un potencial ajustable al circuito mediante la manipulacin de un control (que segn el equipo puede
denominarse control de estandarizacin, de cero, de asimetra, de calibracin, etc.), como as tambin debe ser capaz
59
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO I: CALIBRACIN Y VERIFICACIN DE EQUIPOS
de control el cambio en miliVolts producido por el cambio en unidades de pH, a travs de un control de temperatura
y/o pendiente. Las medidas se realizan a 252 C a menos que se especifique otra cosa en la monografa individual.
Debe destacarse, por lo tanto, que esta definicin de pH, como as tambin los valores asignados a las Soluciones
Buffer para Estandarizacin, son adoptadas con el fin de establecer un sistema prctico y operativo, para que los
resultados puedan ser comprados entre laboratorios. Los valores de pH as medidos o asignados, por lo tanto, pueden
no corresponder exactamente con los valores obtenidos acorde a la definicin pH=-log aH+.
Asimismo, tanto la monografa de la USP como el correspondiente captulo de la FA 7 (<250> Determinacin del pH)
establecen la composicin (y forma de preparacin) de las mencionadas Soluciones Buffer para Estandarizacin
(SB ST), como as tambin sus valores de pH en funcin de la temperatura (ver tabla a continuacin). Tambin es
posible adquirir comercialmente soluciones buffer para calibracin de pH-metros.
Temperatura
(C)
10
15
20
25
30
35
40
45
50
55
60
Tetraoxalato
de K+ 0,05 M
1,67
1,67
1,68
1,68
1,68
1,69
1,69
1,70
1,71
1,72
1,72
Biftalato de
K+ 0,05 M
4,00
4,00
4,00
4,01
4,02
4,02
4,04
4,05
4,06
4,08
4,09
Fosfato Equimolar
0,05 M
6,92
6,90
6,88
6,86
6,85
6,84
6,84
6,83
6,83
6,83
6,84
Tetraborato de
Na+ 0,01 M
9,33
9,28
9,23
9,18
9,14
9,10
9,07
9,04
9,01
8,99
8,96
Ca(OH)2 sat
a 25 C
13,00
12,81
12,63
12,45
12,29
12,13
11,98
11,84
11,71
11,57
11,45
En cuanto al procedimiento de calibracin del pH-metro, las farmacopeas establecen que se deben seguir las
indicaciones particulares de cada equipo y fabricante, a la vez que proporcionan los siguientes lineamientos generales
que deben realizarse cada vez que se vaya a utilizar el equipo (da de trabajo), e incluso puede hacerse varias veces
en un da:
Seleccionar dos soluciones buffer para estandarizacin (SB ST) cuya diferencia en pH no exceda las 4 unidades,
y tales que el pH esperado de la solucin que deseamos medir (solucin de trabajo) sea un valor intermedio entre
ellas.
Llenar la celda de medida con la primera de las SB ST y medir la temperatura.
Setear el control de temperatura del equipo a la temperatura recin medida.
Observar el valor de pH arrojado por el equipo para esta SB ST y luego ajustar el control de pH (o de calibracin)
para que el mismo coincida exactamente con el valor terico conocido de la SB ST.
Enjuagar el electrodo y la celda varias veces con agua primero y con porciones de la segunda SB ST luego.
Observar el valor de pH arrojado por el equipo para esta segunda SB ST: si el mismo se encuentra dentro de 0,07
unidades del valor tabulado, el equipo est listo para ser utilizado.
Si se observa una desviacin mayor, se debe examinar el equipo en busca de fallas y/o ajustar el control de
temperatura hasta que el valor observado coincida con el tabulado.
Repetir el procedimiento de estandarizacin con ambas SB ST hasta que los valores observados, y sin realizar
ajustes posteriores, no difieran ms de 0,02 unidades de pH de los tabulados.
60
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO I: CALIBRACIN Y VERIFICACIN DE EQUIPOS
Cuando el equipo est listo para ser utilizado, enjuagar el electrodo varias veces con la solucin a medir y luego
obtener la lectura de pH.
En todos los casos, se debe dejar al equipo el tiempo suficiente de estabilizacin antes de tomar la lectura.
Emplear agua libre de dixido de carbono para preparar o diluir la solucin cuyo valor de pH queremos
determinar (solucin de trabajo).
Por su parte, el Centro Espaol de Metrologa establece, en su procedimiento operativo QU-003 para la calibracin
de pH-metros digitales (disponible en http://www.cem.es/sites/default/files/qu-003_digital.pdf), lineamientos muy
similares a los recin mencionados, a los que se agregan: a) la evaluacin de la linealidad en la respuesta y; b) el clculo
de la incertidumbre en la medida. A diferencia de la calibracin de rutina descripta por la USP, estas dos evaluaciones
se realizan en forma peridica y programada, no en cada da de trabajo.
CALIBRACIN DEL ESPECTROFOTMETRO UV-VISIBLE
En el captulo <470> Espectrofotometra Ultravioleta y Visible, la FA 7 indica que los aparatos empleados para registrar
los espectros ultravioleta y visible deben cumplir con los ensayos que se describen a continuacin. En cuanto a la USP,
la misma cuenta con un captulo (<851> SPECTROPHOTOMETRY AND LIGHT-SCATTERING, Espectrofotometra y
Dispersin de Luz) dedicado a esta tcnica, donde tambin se indica que debe realizarse la calibracin del equipo.
A. Verificacin de la escala de longitudes de onda
Existen diversas formas de verificarla, entre ellas:
A. Midiendo los mximos de absorbancia de una solucin
estndar de perclorato de holmio 5% p/v a 241,15; 287,15;
361,50 y 536,30 nm,
B. Midiendo los mximos de absorbancia correspondientes a
las lneas de emisin de una lmpara de hidrgeno a 486,10
nm o deuterio a 486,00 nm,
C.
Midiendo las lneas de un arco de vapor de mercurio a
253,70; 302,25; 313,16; 334,15; 365,48; 404,66; 435,83; 546,07; 576,96 y 579,07 nm.
Espectro de una solucin de
Perclorato de Holmio
La tolerancia permitida es de 1 nm para el ultravioleta y 3 nm para el visible.
B. Control o comprobacin de absorbancias (exactitud fotomtrica)
Procedimiento:
1) Preparar una solucin de Dicromato de Potasio de la siguiente manera: secar el dicromato de potasio, calidad
estndar, a 130 C hasta peso constante. Pesar aproximadamente y exactamente 60 mg, disolver y enrasar hasta 1000
ml con cido Sulfrico 0,005 M.
61
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO I: CALIBRACIN Y VERIFICACIN DE EQUIPOS
2) Registrar el espectro de dicha solucin en cubeta de 1 cm de
paso ptico, utilizando cido Sulfrico 0,005 M como blanco, y
medir los valores de abs a 235; 257; 313 y 350 nm.
3) Calcular las absortividades para cada longitud de onda,
mediante la expresin:
1%
A 1cm
4) Los valores de
A( ) 10
C
1%
A 1cm deben estar dentro de las
tolerancias especificadas en la siguiente tabla:
Longitud de onda (, nm)
A 1cm
1%
Tolerancias
235
257
313
350
124,5
144,0
48,6
106,6
122,9- 126,2
142,4 145,7
47,0 50,3
104,9- 108,2
C.
Espectro de una solucin de
Dicromato de Potasio
Lmite de luz espuria
1) Preparar una solucin de cloruro de potasio al 1,2% p/v en agua
destilada.
2) Determinar su absorbancia en cubeta de 1 cm, a 200 nm 2,
utilizando agua destilada como blanco.
La absorbancia leda deber ser mayor a 2.
Espectro de una solucin de
Cloruro de Potasio
D. Celdas
Las absorbancias de las celdas de lectura, cuando se llenan con el mismo solvente, deben ser iguales. Si este no es el
caso, debe aplicarse una correccin apropiada.
La tolerancia en el paso ptico de las celdas empleadas es 0,005 cm. Las celdas deben limpiarse y manipularse con
cuidado.
E.
Resolucin (para anlisis cualitativo)
Se prepara una solucin al 0,02% p/v de tolueno en hexano. Se
registra su espectro: la relacin entre el mximo de absorbancia a
269 nm y el mnimo de absorbancia a 266 nm debe ser mayor a 1,5.
Espectro de una solucin de Tolueno 0,02%
en Hexano
62
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO I: CALIBRACIN Y VERIFICACIN DE EQUIPOS
F.
Solventes
Cuando se mide la Absorbancia del solvente de trabajo a una longitud de onda determinada, la absorbancia de la
celda de referencia y su contenido no debe ser mayor a 0,4 (incluso es conveniente que sea menor a 0,2) cuando se
mide con referencia al aire a la misma longitud de onda.
Abs solvente de trabajo () 0,4 (referencia aire)
G. Deriva
Medir la absorbancia sin celda a lo largo del tiempo, durante 30 minutos en el rango de 200 a 700 nm. Elegir 3
longitudes de onda y calcular la diferencia de absorbancia entre 0 y 30 minutos a cada una de ellas. Multiplicar por 2
para obtener la deriva.
Deriva (1) = (A(1)30 min- A(1)0 min) x 2
Especificacin = 0,0003 A/ hora
CALIBRACIN DE BALANZAS
Las siguientes indicaciones pueden encontrarse en la Disposicin ANMAT N 2819/2004 (con las modificaciones de la
Disp. ANMAT N 4844/2005) sobre Buenas Prcticas de Fabricacin para Elaboradores, Importadores/Exportadores
de Medicamentos:
Las balanzas analticas deben ser instaladas en un local adecuado, niveladas, libre de corriente de aire, en
mesadas exclusivas para las mismas y estables. Siempre que se pueda, deben estar dispuestas en ambientes con
temperatura controlada.
-
El lugar donde se emplaza la balanza solo debe tener un acceso para que no se utilice como habitacin de
paso. Los rincones son los lugares ms idneos pues dentro de un edificio son los lugares ms firmes y con
las menores vibraciones.
- No debe instalarse muy cerca de ventanas, ya que existe el peligro de que los rayos solares directos la
calienten irregularmente.
- No debe instalarse la prxima a los radiadores pues adems de la radiacin trmica directa, suelen producir
corrientes de aire relativamente fuertes.
- No debe instalarse cerca de acondicionadores de aire, ni de ventiladores, los cuales producen turbulencias
de aire fuertes.
Las balanzas deben ser acondicionadas despus de su uso. Debe haber un programa que incluya el
mantenimiento y la calibracin peridica (como mnimo, anualmente) con toda la informacin registrada y
archivada.
En el caso de balanzas electrnicas que no posean sistema de auto-calibracin, la verificacin debe ser hecha
diariamente, antes de su utilizacin, con pesas certificadas.
El registro de verificacin de las balanzas debe figurar como mnimo: fecha, datos de la verificacin diaria (en el
caso de que la balanza no cuente con auto-calibracin), nombre del operador y datos de la pesada.
Todos los registros deben ser archivados y las pesas utilizadas en las verificaciones deben ser re-certificadas
anualmente.
El centro debe contar con un procedimiento operativo con la informacin bsica sobre el uso y funcionamiento
de la balanza, limpieza, mantenimiento y calibracin de la misma
63
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO I: CALIBRACIN Y VERIFICACIN DE EQUIPOS
Por otro lado, el captulo <690> Pesas y Balanzas de la FA 7 indica que se deben realizar los siguientes ensayos durante
la calibracin de una balanza:
A. Ensayo de Excentricidad: El mismo se realiza desplazando sistemticamente una carga sobre el receptor (o
platillo) con el objetivo de determinar si la indicacin de la balanza es suficientemente insensible a cambios de
emplazamiento de la carga sobre el dispositivo receptor de carga.
B. Ensayo de Linealidad: El objetivo de este ensayo es comprobar la capacidad de la balanza de proporcionar
indicaciones concordantes con el valor de las masas patrn cargadas sobre el mismo, bajo condiciones normales
de utilizacin. Relacin lineal entre masa y valor indicado. Las cargas de masas patrn a emplear se escogern de
manera que se establezcan al menos diez divisiones a lo largo del rango de pesada, incluyendo cargas prximas
a la capacidad mnima y mxima de la balanza.
C.
Ensayo de Repetibilidad: La repetibilidad se define como el grado de aproximacin mutua de mediciones
consecutivas de la misma magnitud, efectuadas bajo las mismas condiciones de medida. Estas condiciones
reciben el nombre de condiciones de repetibilidad y comprenden:
El mismo procedimiento de medida.
El mismo observador.
La misma balanza, utilizada bajo las mismas condiciones.
El mismo lugar.
Repeticin dentro de un intervalo de tiempo breve.
En cuanto a la incertidumbre aceptada para las medidas de peso, tanto el captulo <690> de la FA 7 como el captulo
<41> de USP (WEIGHTS AND BALANCES) indican que, a menos que se especifique de otra manera, cuando las
sustancias deban ser exactamente pesadas debe emplearse un instrumento cuyo grado de incertidumbre (error
aleatorio ms error sistemtico) no sea mayor de 0,1 % de la lectura.
Es decir que la incertidumbre en la medida es aceptable si tres veces el valor de la desviacin estndar, de no menos
de diez pesadas, dividido por la cantidad pesada, no es mayor de 0,001.
64
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO I: CALIBRACIN Y VERIFICACIN DE EQUIPOS
PROBLEMAS DE APLICACIN
PROBLEMA 1
Los datos que se detallan a continuacin fueron obtenidos en una balanza con legibilidad al 0,01 mg:
Valor Pesa (mg)
Lectura (mg)
20,0
20,01
20,0
20,01
20,0
20,01
20,0
19,99
20,0
20,01
20,0
20,01
20,0
20,01
20,0
20,00
20,0
20,00
20,0
20,00
a. Indica si la incertidumbre de la medicin de la masa de 20 mg
cumple con lo establecido en por FA 7 <690> y USP <41>.
b. Podras pesar 25 mg de muestra en una balanza de este tipo?
Justifica tu respuesta.
PROBLEMA 2
Establece si crees correcto pesar 15 miligramos de muestra en una balanza analtica con las siguientes caractersticas:
Legibilidad: 0,0001 g = 0,1 mg
SD tpica: 0,1 mg (catlogo fabricante)
PROBLEMA 3
Un analista de Control de Calidad desea calibrar su balanza en trminos de excentricidad, linealidad y repetibilidad
de la medida. Las caractersticas de la balanza son las siguientes:
Marca: Mettler Toledo AG 20465
Capacidad Mxima: 200 g
Capacidad Mnima: 0,1 mg
Mnima Divisin: 0,0001
3
4
2
Posicin
Indicacin (g)
100,0000
100,0001
100,0002
99,9999
99,9999
Excentricidad: se registr el valor indicado para una carga
control de 100 g ubicada en las posiciones segn el esquema
superior. La tabla muestra los resultados.
Tolerancia para la mxima diferencia encontrada: 0,0004 g
65
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO I: CALIBRACIN Y VERIFICACIN DE EQUIPOS
Linealidad: trabajando con 10 cargas control, se registr el valor indicado por la balanza.
Carga Control
Indicacin Inicial (g)
0,0000
0,5
0,5000
1,0000
2,0000
5,0000
10
10,0000
20
20,0000
50
49,9998
100
99,9998
200
199,9998
Tolerancia para la mxima diferencia encontrada: 0,0002 g
Tolerancia para el Coeficiente de Correlacin (r) 0,999
Repetibilidad: se repiti 10 veces el procedimiento de medida de una carga control de 100 g
Pesada
Indicacin (g)
100,0000
100,0000
99,9999
99,9999
100,0000
99,9999
99,9999
100,0000
100,0000
10
100,0000
Tolerancia (FA 7 y USP): [3 x (SD) / Peso terico] 0,001
a.
En funcin de los resultados presentados, crees que el equipo es apto para su uso?
PROBLEMA 4
El mismo analista del problema anterior desea ahora evaluar la linealidad de la respuesta de su pH-metro en todo el
rango de lectura. Para ello recurre al procedimiento operativo QU-003 del Centro Espaol de Metrologa y encuentra
las siguientes indicaciones:
66
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO I: CALIBRACIN Y VERIFICACIN DE EQUIPOS
1) Proceso de ajuste: La lectura inicial debe realizarse con las SB ST de pH 4 y pH 7 procedindose al ajuste del pHmetro, si se dispone de la autorizacin del usuario, segn se indique en el Manual de Instrucciones del mismo. El
ajuste se realiza, normalmente, haciendo que la lectura del pH-metro coincida con el valor certificado de la SB ST
leda.
2) Se realiza la lectura de las siguientes SB ST de pH 2, pH 4; pH 7; pH 9 y pH 12. Todas las lecturas se realizan por
triplicado.
El analista procede de acuerdo a la secuencia anterior, trabajando siempre a 25 C por lo que no es necesario aplicar
correccin de temperatura, y obtiene los siguientes resultados:
Valor Nominal del SB ST a 25 C
Lectura 1
Lectura 2
Lectura 3
2,00
2,001
2,002
2,001
4,00
4,002
4,002
4,003
7,00
7,001
7,001
6,998
9,00
9,000
9,002
9,001
12,45
12,46
12,44
12,44
Tolerancia: el coeficiente de determinacin (r2) de la recta de regresin con las medias obtenidas debe estar comprendido
entre 0,995 y 1,005 (a menos que el manual de instrucciones del pH-metro indique otros lmites).
a.
Crees el pH-metro es apto para su uso en todo el rango de pH ensayado?
PROBLEMA 5
El mismo analista de Control de Calidad del problema 3, desea por ltimo evaluar la exactitud fotomtrica del
espectrofotmetro UV-Visible de su laboratorio. Para ello prepara una solucin de Dicromato de Potasio (peso: 60,4
mg) y procede segn lo indicado en la FA 7. Resultados:
a.
(nm)
Absorbancia
235
0,7522
257
0,8720
313
0,2935
350
0,6477
Qu opinas de estos resultados?
67
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO I: CALIBRACIN Y VERIFICACIN DE EQUIPOS
68
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO II: UNIFORMIDAD DE UNIDADES DE DOSIFICACIN
ANEXO II. ENSAYO DE UNIFORMIDAD DE UNIDADES DE DOSIFICACIN (UUD)
FARMACOPEA ARGENTINA VII ED.
El ensayo de uniformidad de unidades de dosificacin puede realizarse mediante dos mtodos: uniformidad de peso
(UP) y uniformidad de contenido (UC).
Puede realizarse por UP cuando el producto a ensayar contiene 50 mg o ms del principio activo, el cual adems
corresponda al 50% o ms del peso de la unidad de la forma farmacutica (se deben dar ambas condiciones juntas).
En el caso de unidades de dosificacin que contienen principio activo en una proporcin menor a la mencionada
anteriormente (o que representa un porcentaje del peso total menor al 50%) la UUD debe demostrarse mediante UC.
Por otro lado, este ltimo ensayo (UC) se exige en todos los casos para: comprimidos recubiertos (excepto los de
cubierta flmica), sistemas transdrmicos, suspensiones en envases unitarios o contenidas en cpsulas blandas,
aerosoles dosificadores y supositorios.
UNIFORMIDAD DE PESO (UP)
Para determinar la uniformidad de unidades de dosificacin mediante uniformidad de peso, se deben seleccionar no
menos de treinta unidades y proceder segn se indica:
Comprimidos y comprimidos con cubierta flmica: pesar exactamente y en forma individual diez comprimidos. A partir
del resultado de la Valoracin obtenido segn se indica en la monografa correspondiente, calcular el contenido de
principio activo en cada uno de los diez comprimidos, asumiendo que dicho principio activo est uniformemente
distribuido.
Cpsulas rgidas, cpsulas blandas, slidos, soluciones para inhalaciones, soluciones orales y jarabes: ver FA VII Ed.
<740> pg. 279.
UNIFORMIDAD DE CONTENIDO (UC)
Consiste en la determinacin de la UUD mediante la valoracin de unidades individuales. Para ello, se deben
seleccionar no menos de treinta unidades y proceder segn se indica:
Valorar diez unidades individualmente segn se indica en la Valoracin, a menos que se indique de otro modo en el
Procedimiento para uniformidad de contenido en la monografa correspondiente. Cuando la cantidad de principio
activo en una unidad de dosificacin es menor que la requerida en la Valoracin, ajustar el grado de dilucin de las
soluciones y/o el volumen de las alcuotas para que la concentracin de los principios activos en la solucin final sea
del mismo orden que la obtenida en la Valoracin; o para el caso de una titulacin, si fuera necesario, emplear un
titulante ms diluido, procurando emplear un volumen apropiado del mismo. Si se emplearan cualquiera de estas
modificaciones en la Valoracin que establece la monografa correspondiente, realizar los cambios apropiados en la
frmula y en el factor de titulacin.
CRITERIOS DE ACEPTACIN
A) Si el promedio de los lmites especificados en la definicin de concentracin o potencia del producto en la
monografa correspondiente es 100,0% o menos:
Comprimidos, comprimidos recubiertos, comprimidos con cubierta flmica, supositorios, suspensiones,
soluciones orales y jarabes, slidos y slidos estriles para uso parenteral: a menos que se especifique de otro
modo en la monografa correspondiente, los requisitos para la uniformidad se cumplen si la cantidad de
principio activo en cada una de las diez unidades de dosificacin determinada por UP o UC, segn
correspondiera, se encuentra dentro del intervalo de 85,0 - 115,0% del valor declarado y la desviacin estndar
relativa (CV) es menor o igual a 6,0%.
69
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO II: UNIFORMIDAD DE UNIDADES DE DOSIFICACIN
Si una unidad est fuera de dicho intervalo y ninguna unidad est fuera del 75,0 - 125,0% del valor declarado,
si el CV es mayor a 6,0% o si ambas condiciones prevalecen, ensayar veinte unidades adicionales. Los
requisitos se cumplen si no ms de una unidad de las treinta unidades de dosificacin est fuera del intervalo
de 85,0 - 115,0% del valor declarado, ninguna unidad est fuera del intervalo del 75,0 - 125,0% del valor
declarado y el CV no es mayor a 7,8%.
Cpsulas, sistemas transdrmicos y soluciones para inhalacin, aerosoles dosificadores: ver FA VII Ed.
B) Si el promedio de los lmites especificados en la definicin de concentracin o potencia del producto en la
monografa correspondiente es mayor de 100,0%, se pueden dar a su vez tres casos:
1)
Si el valor promedio de las unidades de dosificacin ensayadas es 100% o menos, los requisitos son como en
A).
2) Si el valor del promedio de las unidades de dosificacin ensayadas es mayor o igual al promedio de los lmites
especificados en la definicin de potencia en la monografa correspondiente, los requisitos son los descriptos
en A), excepto que las palabras valor declarado se reemplazan por las palabras valor declarado multiplicado
por el promedio de los lmites especificados en la definicin de potencia en la monografa correspondiente
dividido 100.
3) Si el valor promedio de las unidades de dosificacin ensayadas est entre 100% y el promedio de los lmites
especificados en la definicin de potencia en la monografa correspondiente, los requisitos son los descriptos
en A), excepto que las palabras valor declarado se reemplazan por las palabras valor declarado multiplicado
por el valor promedio de las unidades de dosificacin ensayadas (expresado como %SVD) dividido 100.
USP 38
Para asegurar la UUD, el contenido de principio activo (pa) de cada unidad en un lote debe estar dentro de un
estrecho rango alrededor del valor declarado. Las unidades de dosificacin son definidas como las formas de
dosificacin conteniendo una dosis nica, por ejemplo: comprimidos, cpsulas, etc. El trmino Uniformidad de
Unidades de Dosificacin es definido como el grado de uniformidad en la cantidad de pa entre las unidades de
dosificacin.
El ensayo de uniformidad de las unidades de dosificacin puede realizarse mediante dos mtodos: uniformidad de
peso (UP) y uniformidad de contenido (UC).
El mtodo por UC est basado en la valoracin del contenido individual del pa en un nmero determinado de unidades
de dosificacin individuales. Este mtodo puede ser utilizado en todos los casos, pero el mismo es exigido cuando el
producto a ensayar contiene menos de 25 mg del pa o cuando dicho pa corresponde a menos del 25% del peso de la
unidad de dosificacin (es decir, que para por realizar la UUD por UP, se debe cumplir, simultneamente, que el
contenido de pa sea mayor a 25 mg y que represente ms del 25% del peso total de la unidad).
Por otro lado, el ensayo de UC se exige en todos los casos para: comprimidos recubiertos (excepto los de cubierta
flmica), sistemas transdrmicos, suspensiones en envases unitarios o contenidas en cpsulas blandas, aerosoles
dosificadores, supositorios, slidos (incluidos los estriles), envasados en dosis unitarias.
UNIFORMIDAD DE CONTENIDO (UC)
Al igual que para FA, se trata de la determinacin de UUD mediante la valoracin de unidades individuales. Para ello,
seleccionar no menos de treinta unidades y proceder segn se indica:
Valorar diez unidades individualmente segn se indica en la Valoracin, a menos que se indique de otro modo en el
Procedimiento para uniformidad de contenido en la monografa correspondiente. Cuando la cantidad de principio
activo en una unidad de dosificacin es menor que la requerida en la Valoracin, ajustar el grado de dilucin de las
soluciones y/o el tamao de las alcuotas para que la concentracin de los principios activos en la solucin final sea
70
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO II: UNIFORMIDAD DE UNIDADES DE DOSIFICACIN
del mismo orden que la obtenida en la Valoracin; o para el caso de una titulacin, si fuera necesario, emplear un
titulante ms diluido, procurando emplear un volumen apropiado del mismo.
Cuando se especifique un procedimiento especial, diferente al indicado para la valoracin, para Uniformidad de
contenido en la monografa correspondiente, se deben hacer determinadas correcciones de los resultados obtenidos
(ver USP 34 <905>)
Finalizado este ensayo, se debe calcular un Valor de Aceptacin (VA).
Clculo del valor de aceptacin (VA). Se calcula mediante la siguiente frmula:
= | | +
= Media del contenido individual expresado como %SVD
M = Valor de referencia
K = Constante de Aceptabilidad (si n=10 K=2,4; si n=30 K=2)
n = nmero de unidades testeadas
s = Desviacin estndar
Por otro lado, se define el parmetro T como el %SVD de pa esperado tericamente al tiempo de elaboracin (T0). En
caso de no conocerse, T=100%.
Caso 1: Se aplica cuando T es 101,5%
(a) Si 98,5% 101,5%
(b) Si < 98,5%
(c) Si > 101,5%
entonces M = y VA = K.s
entonces M = 98,5% y VA = 98,5 - + K.s
entonces M = 101,5% y VA = 101,5 + K.s
Caso 2: Se aplica cuando T es > 101,5%
(a) Si 98,5% T
(b) Si < 98,5%
(c) Si > T
entonces M = y VA = K.s
entonces M = 98,5% y VA = 98,5 - + K.s
entonces M = T y VA = T + K.s
UNIFORMIDAD DE PESO (UP)
Para determinar la uniformidad de unidades de dosificacin mediante uniformidad de peso, seleccionar no menos de
treinta unidades y proceder segn se indica:
Comprimidos y comprimidos con cubierta flmica: pesar exactamente y en forma individual diez comprimidos. A partir
del resultado de la Valoracin obtenido segn se indica en la monografa correspondiente, calcular el contenido de
principio activo en cada uno de los diez comprimidos, asumiendo que dicho principio activo est uniformemente
distribuido
Cpsulas rgidas, cpsulas blandas, slidos, soluciones para inhalaciones, soluciones orales y jarabes: ver USP 34
<905>.
El resultado de la valoracin obtenida directamente como se indica en la monografa correspondiente se designa
como resultado A y el mismo es expresado como %SVD.
Clculo del valor de aceptacin (VA)
El VA se calcula conforme a lo indicado en UC excepto que el contenido individual de cada unidad es reemplazado
por el contenido individual estimado (xn), calculado segn:
71
CONTROL DE CALIDAD DE MEDICAMENTOS ANEXO II: UNIFORMIDAD DE UNIDADES DE DOSIFICACIN
Pn = Peso individual de cada unidad testeada
A = Contenido de pa expresado como %SVD
Pm = Peso medio
CRITERIOS DE ACEPTACIN
Aplicar el siguiente criterio (a menos que se especifique otra cosa en la monografa correspondiente):
Comprimidos con o sin cubierta, cpsulas, soluciones orales en envases unidosis, suspensiones, emulsiones o geles
orales en envases unidosis y slidos (incluyendo slidos estriles) en envases unidosis:
I.
Los requerimientos del ensayo de UUD son cumplidos si el VA de las primeras 10 unidades de dosificacin
ensayadas es L1% (VA L1%)
II.
Si VA > L1% testear las siguientes 20 unidades y calcular el nuevo VA.
III.
Los requerimientos son cumplidos si el VA final de las 30 unidades de dosificacin es L1% y el contenido
individual de cada una de las unidades de dosificacin testeadas est dentro del intervalo: (1 L2 *
0,01)*M
A menos que se especifique otra cosa en la monografa individual, L1 = 15,0 y L2 = 25,0
Donde L1 = mximo valor de aceptacin permitido y L2 = mximo rango permitido para la desviacin de cada
unidad de dosificacin testeada con respecto al valor calculado de M.
Para supositorios, sistemas transdrmicos y soluciones para inhalacin en envases unidosis: ver USP 34 <905>.
72
--------------------------------------------------------------------------------------------------------------------------------------------------------------------HOJAS PARA TRAER AL PARCIAL
yij yi 2
FRMULAS REGRESIN
s 2 ( y )
N ni
N 2
2
1
x
s ( a ) s ( y )
2
ni ni ( x i x )
i
i
2
i 1
s2( b )
s 2 ( y )
ni ( x i x )2
i
Descomposicin de la suma de cuadrados
ST = SR + SE
2
y ij y ni .( y i y ) 2 ( y ij y i ) 2
m ni
m ni
i 1 j 1
i 1
i 1 j 1
r2 = SR/ST
tcalc
T N 1 R E p 1 N p
N 2
1 r2
INTERVALOS DE CONFIANZA PARA UNA PREDICCIN DE Y
Para una sola respuesta futura
y 0 t / 2, N 2
Para la respuesta media
2
x0 x
1
s( y ) 1
ni ni ( xi x) 2
i
i
y 0 t / 2, N 2 s( y )
x i
INTERVALOS DE CONFIANZA PARA UNA PREDICCIN DE X
2
x0 x
1
n
ni ( xi x) 2
i
i
i
Replicando la incgnita r veces
x 0 t / 2, N 2 s( x ) , donde:
x 0 t / 2, N 2 s( x ) , donde:
s 2 ( y )
1 y0
s ( x )
1 N b
2
b
s 2 ( y )
2
s
(
x
)
b2
ni ( x i x ) 2
( yi a )
b
Sin replicar la incgnita
1 1 y 0
r N b
2
ni ( x i x )
OTRAS FRMULAS
As
W5%
2 f
Rs
2 t R 2 t R1
W1 W2
( ) ( )
1
1
+
2 =
t ob
100 % R
CV
n
2 + 2
+
73
--------------------------------------------------------------------------------------------------------------------------------------------------------------------HOJAS PARA TRAER AL PARCIAL
TABLA DE VALORES DE LA DISTRIBUCIN t DE STUDENT
74
--------------------------------------------------------------------------------------------------------------------------------------------------------------------HOJAS PARA TRAER AL PARCIAL
TABLA DE VALORES DE LA DISTRIBUCIN F (p=0,95)
75
--------------------------------------------------------------------------------------------------------------------------------------------------------------------HOJAS PARA TRAER AL PARCIAL
Ensayo de Disolucin Criterios de Aceptacin
1.
2.
3.
Criterios de Aceptacin para productos LI Muestreo Individual
Etapa
Unid.
E1
Ninguna unidad es menor de Q + 5%
E2
El promedio de 12 unid. (E1+E2) es igual o mayor que Q y ninguna unidad menor de Q
15%
E3
12
El promedio de 24 unid. (E1+E2+E3) es igual o mayor que Q, no ms de 2 unid. son
menores que Q - 15% y ninguna menor que Q - 25%
Criterios de Aceptacin para productos LI Muestreo Unificado
Etapa
Unid.
E1
La cantidad promedio no es menor de Q + 10%
E2
La cantidad promedio disuelta (E1+E2) es igual o mayor que Q + 5%
E3
12
La cantidad promedio disuelta (E1+E2+E3) es igual o mayor que Q
Criterio de Aceptacin
Criterios de Aceptacin para productos LP
Etapa
Unid.
E1
Ningn valor individual fuera de los rangos establecidos
E2
El promedio de 12 unid. dentro del rango establecido. Ningn valor individual
representa ms del 10% fuera del rango y ninguno est ms del 10% por debajo del lmite
del tiempo final
12
El promedio de 24 unid. dentro del rango establecido. No ms de 2 unid representan
ms del 10% fuera del rango y no ms de 2 estn ms del 10% por debajo del lmite del
tiempo final. Ninguna unidad representa ms del 20% fuera del rango y ninguna est
ms del 20% por debajo del lmite del tiempo final
E3
4.
Criterio de Aceptacin
Criterio de Aceptacin
Criterios de Aceptacin para productos LR Etapa cida*
Etapa
Unid.
Criterio de Aceptacin
E1
Ningn valor individual excede el 10% disuelto
E2
El promedio de 12 unid. (E1+E2) no es mayor del 10% disuelto y ninguna unidad individual
es mayor del 25%
E3
12
El promedio de 24 unid. (E1+E2+E3) no es mayor del 10% disuelto y ninguna unidad
individual es mayor de 25%
*NOTA: La Etapa de Solucin Reguladora sigue los criterios habituales para productos LI
76
--------------------------------------------------------------------------------------------------------------------------------------------------------------------HOJAS PARA TRAER AL PARCIAL
Ensayo de Uniformidad de Unidades de Dosificacin Criterios de Aceptacin
FA 7
A) Si el promedio de los lmites especificados en la definicin de concentracin o potencia del producto en la
monografa correspondiente es 100,0% o menos:
Comprimidos, comprimidos recubiertos, comprimidos con cubierta flmica, supositorios, suspensiones,
soluciones orales y jarabes, slidos y slidos estriles para uso parenteral: a menos que se especifique de
otro modo en la monografa correspondiente, los requisitos para la uniformidad se cumplen si la cantidad
de principio activo en cada una de las diez unidades de dosificacin determinada por UP o UC, segn
correspondiera, se encuentra dentro del intervalo de 85,0 - 115,0% del valor declarado y la desviacin
estndar relativa (CV) es menor o igual a 6,0%.
Si una unidad est fuera de dicho intervalo y ninguna unidad est fuera del 75,0 - 125,0% del valor
declarado, si el CV es mayor a 6,0% o si ambas condiciones prevalecen, ensayar veinte unidades
adicionales. Los requisitos se cumplen si no ms de una unidad de las treinta unidades de dosificacin
est fuera del intervalo de 85,0 - 115,0% del valor declarado, ninguna unidad est fuera del intervalo del
75,0 - 125,0% del valor declarado y el CV no es mayor a 7,8%.
Cpsulas, sistemas transdrmicos y soluciones para inhalacin, aerosoles dosificadores: ver FA VII Ed.
B) Si el promedio de los lmites especificados en la definicin de concentracin o potencia del producto en la
monografa correspondiente es mayor de 100,0%, se pueden dar a su vez tres casos:
4) Si el valor promedio de las unidades de dosificacin ensayadas es 100% o menos, los requisitos son como
en A).
5) Si el valor del promedio de las unidades de dosificacin ensayadas es mayor o igual al promedio de los
lmites especificados en la definicin de potencia en la monografa correspondiente, los requisitos son
los descriptos en A), excepto que las palabras valor declarado se reemplazan por las palabras valor
declarado multiplicado por el promedio de los lmites especificados en la definicin de potencia en la
monografa correspondiente dividido 100.
6) Si el valor promedio de las unidades de dosificacin ensayadas est entre 100% y el promedio de los
lmites especificados en la definicin de potencia en la monografa correspondiente, los requisitos son
los descriptos en A), excepto que las palabras valor declarado se reemplazan por las palabras valor
declarado multiplicado por el valor promedio de las unidades de dosificacin ensayadas (expresado
como %SVD) dividido 100.
USP 38
Clculo del valor de aceptacin (VA). Uniformidad de Contenido
= | | +
= Media del contenido individual expresado como %SVD
M = Valor de referencia
K = Constante de Aceptabilidad (si n=10 K=2,4; si n=30 K=2)
n = nmero de unidades testeadas
s = Desviacin estndar
77
--------------------------------------------------------------------------------------------------------------------------------------------------------------------HOJAS PARA TRAER AL PARCIAL
Por otro lado, se define el parmetro T como el %SVD de pa esperado tericamente al tiempo de elaboracin (T 0).
En caso de no conocerse, T=100%.
Caso 1: Se aplica cuando T es 101,5%
(a) Si 98,5% 101,5%
(b) Si < 98,5%
(c) Si > 101,5%
entonces M = y VA = K.s
entonces M = 98,5% y VA = 98,5 - + K.s
entonces M = 101,5% y VA = 101,5 + K.s
Caso 2: Se aplica cuando T es > 101,5%
(a) Si 98,5% T
(b) Si < 98,5%
(c) Si > T
entonces M = y VA = K.s
entonces M = 98,5% y VA = 98,5 - + K.s
entonces M = T y VA = T + K.s
Clculo del valor de aceptacin (VA) Uniformidad de Peso
El VA se calcula conforme a lo indicado en UC excepto que el contenido individual de cada unidad es reemplazado
por el contenido individual estimado (xn), calculado segn:
=
Pn = Peso individual de cada unidad testeada
A = Contenido de pa expresado como %SVD
Pm = Peso medio
CRITERIOS DE ACEPTACIN
Aplicar el siguiente criterio (a menos que se especifique otra cosa en la monografa correspondiente):
Comprimidos con o sin cubierta, cpsulas, soluciones orales en envases unidosis, suspensiones, emulsiones o
geles orales en envases unidosis y slidos (incluyendo slidos estriles) en envases unidosis:
IV.
Los requerimientos del ensayo de UUD son cumplidos si el VA de las primeras 10 unidades de
dosificacin ensayadas es L1% (VA L1%)
V.
Si VA > L1% testear las siguientes 20 unidades y calcular el nuevo VA.
VI.
Los requerimientos son cumplidos si el VA final de las 30 unidades de dosificacin es L1% y el
contenido individual de cada una de las unidades de dosificacin testeadas est dentro del intervalo:
(1 L2 * 0,01)*M
A menos que se especifique otra cosa en la monografa individual, L1 = 15,0 y L2 = 25,0
Donde L1 = mximo valor de aceptacin permitido y L2 = mximo rango permitido para la desviacin de cada
unidad de dosificacin testeada con respecto al valor calculado de M.
Para supositorios, sistemas transdrmicos y soluciones para inhalacin en envases unidosis: ver USP 38 <905>.
78
--------------------------------------------------------------------------------------------------------------------------------------------------------------------HOJAS PARA TRAER AL PARCIAL
Estabilidad
79
You might also like
- Serie de Ejercicios Desarrollo AnaliticoDocument9 pagesSerie de Ejercicios Desarrollo AnaliticoEspinosa Ortiz María FernandaNo ratings yet
- DUVIOLS - La CapacochaDocument4 pagesDUVIOLS - La CapacochaGaston GomezNo ratings yet
- Amoxicilin ADocument10 pagesAmoxicilin AAndresNavarreteMedinaNo ratings yet
- Cuantificación de Ácido Acetilsalicílico de Tabletas de Aspirina VA20Document2 pagesCuantificación de Ácido Acetilsalicílico de Tabletas de Aspirina VA20juniorNo ratings yet
- Validacion Del Metodo Analitico - ParacetamolDocument15 pagesValidacion Del Metodo Analitico - Paracetamolmario.enrique.molina.lNo ratings yet
- Ejercicios Unidad 5Document6 pagesEjercicios Unidad 5melissmeliss1No ratings yet
- Practica #2 Curva de ValoracionDocument20 pagesPractica #2 Curva de ValoracionNnaLupizNo ratings yet
- Informe 6 Experimental IIDocument12 pagesInforme 6 Experimental IISarahi HernandezNo ratings yet
- Cuantificacion de Glucosa en MermeladaDocument7 pagesCuantificacion de Glucosa en Mermeladajuansalvadorgarciahe100% (2)
- Practica 4 Aplicaciones de Neutralizacion Determinacion de AcidezpruebaDocument5 pagesPractica 4 Aplicaciones de Neutralizacion Determinacion de AcidezpruebaDiego OlivaresNo ratings yet
- TALLERTratamiento Estadistico de DatosDocument6 pagesTALLERTratamiento Estadistico de DatosSARA LISSETTE CUITIVA ARIASNo ratings yet
- Lab Quimica 6-UNMSMDocument13 pagesLab Quimica 6-UNMSMHaydee FigueroaNo ratings yet
- Análisis de acetaminofén en producto farmacéutico por HPLCDocument8 pagesAnálisis de acetaminofén en producto farmacéutico por HPLCGwynevere SOULNo ratings yet
- Informe 4 D Q.A. InstrumentalDocument16 pagesInforme 4 D Q.A. InstrumentalLidiaaurisNo ratings yet
- Informe de Lab Experiencia # 2Document11 pagesInforme de Lab Experiencia # 2Mateo Carcamo BarretoNo ratings yet
- Informe de Lab Experiencia # 2Document11 pagesInforme de Lab Experiencia # 2Mateo Carcamo BarretoNo ratings yet
- ALPRAZOLAM TABLETASDocument3 pagesALPRAZOLAM TABLETASErwin FernándezNo ratings yet
- Taller Clinico III (Diluciones y Tecnicas Inmunes)Document9 pagesTaller Clinico III (Diluciones y Tecnicas Inmunes)TRABAJOS ESCRITOS MEDELLINNo ratings yet
- Análisis de Comprimidos de AAS-CafeínaDocument4 pagesAnálisis de Comprimidos de AAS-CafeínaIssa VsqzNo ratings yet
- Análisis de almidón y azúcares en plátanoDocument5 pagesAnálisis de almidón y azúcares en plátanoAlee LaraNo ratings yet
- T.A. Enzimar Enzimático TabletasDocument10 pagesT.A. Enzimar Enzimático TabletasDesarrollo Química PatricNo ratings yet
- Anteproyecto Tabletas de ParacetamolDocument11 pagesAnteproyecto Tabletas de ParacetamolMitzi Vanessa Martínez CuevasNo ratings yet
- Informe DeparacetamolDocument4 pagesInforme DeparacetamolYasmin Atonal100% (1)
- Guía Control de CalidadDocument4 pagesGuía Control de CalidadwisievekNo ratings yet
- Informe Lab Estandarizacion TecnicasDocument5 pagesInforme Lab Estandarizacion TecnicashappychemestrianNo ratings yet
- Análisis de medicamentos: Ejercicios de cálculo de concentracionesDocument2 pagesAnálisis de medicamentos: Ejercicios de cálculo de concentracionesKarencita RodríguezNo ratings yet
- Informe 4 - Paracetamol en JarabeDocument8 pagesInforme 4 - Paracetamol en JarabeJoel SantosNo ratings yet
- Práctica RetrotitulaciónDocument16 pagesPráctica RetrotitulaciónLiss Muñoz PechNo ratings yet
- Prueba de disolución Ciprofloxacino tabletasDocument3 pagesPrueba de disolución Ciprofloxacino tabletaslunaivaNo ratings yet
- Análisis de ácido acetilsalicílico en tabletas por espectrofotometría UV-VISDocument11 pagesAnálisis de ácido acetilsalicílico en tabletas por espectrofotometría UV-VISStephanie Lizeth Torres MoralesNo ratings yet
- Azucares Reductores Por DNSDocument6 pagesAzucares Reductores Por DNSjerssonNo ratings yet
- Estandar InternoDocument6 pagesEstandar InternogcimarronNo ratings yet
- Protocolo (Marín - Ruiz)Document7 pagesProtocolo (Marín - Ruiz)JLGalarce BurboaNo ratings yet
- Tarea Uniformidad de DosisDocument4 pagesTarea Uniformidad de DosisJazive Esmeralda Alva MoralesNo ratings yet
- Cuestionario 2Document2 pagesCuestionario 2Arianna Mayté Lara PrimoNo ratings yet
- MTA826306 USUPEK 30 MG COMPRIMIDOS 14dic22Document8 pagesMTA826306 USUPEK 30 MG COMPRIMIDOS 14dic22Matias Perez AliagaNo ratings yet
- PROTOCOLO DE VALIDACION-Tabletas DivinaDocument22 pagesPROTOCOLO DE VALIDACION-Tabletas DivinaAaron SaavedraNo ratings yet
- Uniformidad de Unidades de Dosificación 2013Document7 pagesUniformidad de Unidades de Dosificación 2013dayanara886No ratings yet
- AnaliticaDocument34 pagesAnaliticamipeneNo ratings yet
- Practica 3 MedicamentosDocument5 pagesPractica 3 MedicamentosKaren PerezNo ratings yet
- Guia de Metodos de Analisis Por HPLCDocument17 pagesGuia de Metodos de Analisis Por HPLCFede SerrattiNo ratings yet
- Inf BioQ7Document13 pagesInf BioQ7Walter Salazar SandiNo ratings yet
- Inf BioQ6Document15 pagesInf BioQ6Walter Salazar SandiNo ratings yet
- Q. A. P.7A + DATOS SUGERIDOS - IAI - UNIA 2020 - II Determ. de Analitos en M.P.Document4 pagesQ. A. P.7A + DATOS SUGERIDOS - IAI - UNIA 2020 - II Determ. de Analitos en M.P.DENNIS RICOPA VASQUEZNo ratings yet
- Iniciación A La Bromatología (Prácticas) Protocolos de Análisis Ref: 15.4 Almidón (Espectrofotometría)Document3 pagesIniciación A La Bromatología (Prácticas) Protocolos de Análisis Ref: 15.4 Almidón (Espectrofotometría)fredy noyaNo ratings yet
- Ac - Bs Ejercicios Serie 2Document1 pageAc - Bs Ejercicios Serie 2kevinlarios290798No ratings yet
- Examen Parcial I CromatografiaDocument7 pagesExamen Parcial I CromatografiacynthiiaGaNo ratings yet
- COMPLEXOMETRIADocument6 pagesCOMPLEXOMETRIAIsabel CruzNo ratings yet
- PROMEFA - Guía de Procedimientos 2021 - v14 (2021 Feb 20)Document78 pagesPROMEFA - Guía de Procedimientos 2021 - v14 (2021 Feb 20)Martin BoninfanteNo ratings yet
- Tecnica Analitica de Moxiflow 400MG TabDocument4 pagesTecnica Analitica de Moxiflow 400MG TabEdwin MoralesNo ratings yet
- Determinación de Cafeína en Bebidas EnergizantesDocument4 pagesDeterminación de Cafeína en Bebidas EnergizantesCarlos Felipe Jaramillo LópezNo ratings yet
- Carbohidratos PracticaDocument2 pagesCarbohidratos Practicaerik712No ratings yet
- Fosfatasa Residual +Document3 pagesFosfatasa Residual +Luis Arturo Ruiz GalindoNo ratings yet
- Isotonía de preparados parenteralesDocument4 pagesIsotonía de preparados parenteralesJoice C FloresNo ratings yet
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadFrom EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadNo ratings yet
- Farmacometría:Curvas dosis-respuesta de tipo gradual. Volumen 1From EverandFarmacometría:Curvas dosis-respuesta de tipo gradual. Volumen 1No ratings yet
- Guiones experimentales para la enseñanza y aprendizaje del laboratorio de Toxicología (clave 1614)From EverandGuiones experimentales para la enseñanza y aprendizaje del laboratorio de Toxicología (clave 1614)No ratings yet
- QOS Limpiador AmoniacalDocument1 pageQOS Limpiador AmoniacalLili Vera RieraNo ratings yet
- Prepostseo 1702500943Document2 pagesPrepostseo 1702500943Lili Vera RieraNo ratings yet
- Escuela Superior Politécnica Del LitoralDocument108 pagesEscuela Superior Politécnica Del LitoralLili Vera RieraNo ratings yet
- Catalogo CosmeticosDocument122 pagesCatalogo CosmeticosLili Vera RieraNo ratings yet
- Incumbencias ProfesionalesDocument38 pagesIncumbencias ProfesionalesLili Vera RieraNo ratings yet
- Sieteleyesdela Conciencia MagicaDocument193 pagesSieteleyesdela Conciencia Magicajessicale82No ratings yet
- Joyce Meyer Cc3b3mo Oir A Dios PDFDocument139 pagesJoyce Meyer Cc3b3mo Oir A Dios PDFJoz Avalos H100% (2)
- Luis Alberto Montenegro Barrera: Universidad San Francisco de Quito UsfqDocument56 pagesLuis Alberto Montenegro Barrera: Universidad San Francisco de Quito UsfqAlexa PerezNo ratings yet
- Ud2 RESUMENDocument21 pagesUd2 RESUMENLili Vera RieraNo ratings yet
- ¿Qué Son Las Habilidades Socioemocionales (HSE)Document35 pages¿Qué Son Las Habilidades Socioemocionales (HSE)Lili Vera Riera100% (1)
- Arroz Exfoliante NaturalDocument3 pagesArroz Exfoliante NaturalJoel SolisNo ratings yet
- Gel AntiinflamatorioDocument13 pagesGel AntiinflamatorioLili Vera RieraNo ratings yet
- Ejercicio de ClaseDocument3 pagesEjercicio de ClaseLili Vera RieraNo ratings yet
- Poe P Acetamo2Document6 pagesPoe P Acetamo2Lili Vera RieraNo ratings yet
- Semana 1 Bebidas AlcoholicasDocument24 pagesSemana 1 Bebidas AlcoholicasLili Vera RieraNo ratings yet
- SupositoriosDocument5 pagesSupositoriosKaren Balam VazquezNo ratings yet
- Formula EditableDocument1 pageFormula EditableLili Vera RieraNo ratings yet
- Poe P Acetamo2Document6 pagesPoe P Acetamo2Lili Vera RieraNo ratings yet
- Buenas Practicas de ManufacturaDocument77 pagesBuenas Practicas de ManufacturaQF TeranNo ratings yet
- Poe P Acetamo2Document6 pagesPoe P Acetamo2Lili Vera RieraNo ratings yet
- Diagramas de ProcesosDocument5 pagesDiagramas de ProcesosLili Vera RieraNo ratings yet
- Poe P Acetamo2Document6 pagesPoe P Acetamo2Lili Vera RieraNo ratings yet
- Sistema Global Armonizado (Sga Onu 2011)Document607 pagesSistema Global Armonizado (Sga Onu 2011)Mario MontenegroNo ratings yet
- Protocolo SupositoriosDocument6 pagesProtocolo SupositoriosfakiplNo ratings yet
- Etiquetas Área SuciaDocument1 pageEtiquetas Área SuciaLili Vera RieraNo ratings yet
- MJJKLKLDocument32 pagesMJJKLKLnival24No ratings yet
- Carmita TF II SemisólidosDocument80 pagesCarmita TF II SemisólidosLili Vera RieraNo ratings yet
- F F Estriles 110412234218 Phpapp02Document37 pagesF F Estriles 110412234218 Phpapp02Lili Vera RieraNo ratings yet
- Elaboración de Pomadas: Farmacia PrácticaDocument3 pagesElaboración de Pomadas: Farmacia PrácticaLili Vera Riera100% (1)
- 08 Control de Calidad para Preparados EsterilesDocument51 pages08 Control de Calidad para Preparados EsterilesMilagros Santamaría Inoñan75% (4)
- Cloruro de PotasioDocument6 pagesCloruro de PotasioJuan Esteban Garcia FernandezNo ratings yet
- Plano Tablas VentiladoresDocument1 pagePlano Tablas VentiladoresFrank CabanillasNo ratings yet
- Sistemas de conservación de forrajeDocument6 pagesSistemas de conservación de forrajeFelipe FernándezNo ratings yet
- Zocalos y ContrazocalnestorDocument15 pagesZocalos y Contrazocalnestormario0% (1)
- Metodo Secuente de PicosDocument30 pagesMetodo Secuente de PicosRodriguez Veizaga Noelia100% (1)
- Resumen de Perfil PatujusalDocument6 pagesResumen de Perfil PatujusalJulio Ricardo Ruiz CardonaNo ratings yet
- PST para equipos de cocina y oficinaDocument82 pagesPST para equipos de cocina y oficinaMilena NavarreteNo ratings yet
- BioestadísticaDocument5 pagesBioestadísticaAlejandro NuñezNo ratings yet
- Práctica 1 Sockets en PythonDocument5 pagesPráctica 1 Sockets en Pythonhack hackNo ratings yet
- Arqueologia Actividad 6Document3 pagesArqueologia Actividad 6Maria Caicedo EnríquezNo ratings yet
- Griego 5Document76 pagesGriego 5Brian M Calixto-RamosNo ratings yet
- Leyenda BastianDocument3 pagesLeyenda BastianCristian CoronadoNo ratings yet
- Control N 6 Estrategía de Negociación IACCDocument5 pagesControl N 6 Estrategía de Negociación IACCao_kinghtonNo ratings yet
- Caso FinalDocument4 pagesCaso FinalKaren CastroNo ratings yet
- Proyecto de Aula ACA1 y ACA2Document8 pagesProyecto de Aula ACA1 y ACA2Daniel DiazNo ratings yet
- Responsabilidad Civil Del Fiduciario Ley 24441Document39 pagesResponsabilidad Civil Del Fiduciario Ley 24441Marcos SoriaNo ratings yet
- Guía de ejercicios de rapidez y velocidadDocument3 pagesGuía de ejercicios de rapidez y velocidadMoisés InostrozaNo ratings yet
- Determinaciones de fluoruro en aguaDocument4 pagesDeterminaciones de fluoruro en aguaSOFIA MELENDEZ RODRIGUEZNo ratings yet
- PISTASVEREDASTAMBILL0614Document35 pagesPISTASVEREDASTAMBILL0614Pablo Evaristo Vasquez VeraNo ratings yet
- Proyecto Final Metodos CuantitativosDocument19 pagesProyecto Final Metodos Cuantitativosnilvia ehernandezNo ratings yet
- Guias Pie DiabeticoDocument98 pagesGuias Pie Diabeticonashelly perezNo ratings yet
- Enfoques de Formulación para La Administración Oral de Medicamentos Orales - Beneficios y Limitaciones de Las Plataformas ActualesDocument24 pagesEnfoques de Formulación para La Administración Oral de Medicamentos Orales - Beneficios y Limitaciones de Las Plataformas ActualesLUIS MIGUEL CASTILLA MORANNo ratings yet
- 4F02 - Mcu Movimiento Circular UniformeDocument4 pages4F02 - Mcu Movimiento Circular UniformeTatiana RDNo ratings yet
- La Informacion Contable Contenida en Los Estados FinancierosDocument6 pagesLa Informacion Contable Contenida en Los Estados FinancierosElias ChakraNo ratings yet
- Eshú PDFDocument12 pagesEshú PDFEduardo MejiaNo ratings yet
- GUIA 2. Amplificador Inversor y No InversorDocument6 pagesGUIA 2. Amplificador Inversor y No InversorAyde Yadira Cuaran CuaranNo ratings yet
- T2 ErroresDocument2 pagesT2 ErroresJesus Resta NavarroNo ratings yet
- GI Fenómenos Químicos Etapa1Document21 pagesGI Fenómenos Químicos Etapa1Evelyn CarreraNo ratings yet
- Tarea 6 Calcular La Media Aritmetica y La MedianaDocument18 pagesTarea 6 Calcular La Media Aritmetica y La MedianaMichelle GonzalezNo ratings yet
- 1er Parcial - MacroDocument6 pages1er Parcial - MacroSabri CastagnettoNo ratings yet