Professional Documents
Culture Documents
05 Spectroscopie Dans Ultraviolet
Uploaded by
Bibi BibaCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
05 Spectroscopie Dans Ultraviolet
Uploaded by
Bibi BibaCopyright:
Available Formats
Complément - Chapitre 5
Spectroscopie
Spectroscopie dans l’ultraviolet et le visible
La région du visible du spectre électromagnétique correspond à la lumière dont les
longueurs d’onde varient environ de 400 à 700 nanomètres (1 nm = 10-9 mètre). Les
longueurs d'onde de la lumière ultraviolette sont plus courtes, soit environ de 10 nm à
400 nm, alors que la lumière infrarouge possède des longueurs d'onde plus grandes, aux
alentours de 2,5 μm à 25 μm (1 μm = 10-6 mètre) dans le cas de l’IR moyen, région
utilisée pour les spectres IR. Les anciennes unités utilisées pour ce type de spectroscopie
étaient les millimicrons (1 mμ = 1 nm) ou angström (10 Å = 1 nm). Le tableau 5.a
dresse une liste des longueurs d’onde correspondant aux régions du visible et de
l’ultraviolet exprimées avec les différentes unités.
La quantité d’énergie associée à la lumière visible varie de 155 kJ/mol à 314 kJ/mol et
celle de la lumière ultraviolette, de 314 kJ/mol à 628 kJ/mol (voir le tableau 5.a). Cette
énergie est beaucoup plus élevée que celle employée en spectroscopie infrarouge
(8 kJ/mol à 50 kJ/mol). Elle correspond à la quantité d’énergie requise (qui doit être
absorbée) pour provoquer le saut d’un électron d’une orbitale moléculaire occupée à une
orbitale moléculaire d’énergie supérieure vacante. Les spectres UV-visibles sont donc des
spectres d’absorption. De tels sauts d’électrons sont appelés transitions électroniques.
Un spectre ultraviolet-visible démontre les transitions électroniques, soit le dépla-
cement des électrons d’une orbitale moléculaire occupée vers une autre orbitale d’énergie
supérieure et vacante.
1 nanomètre (nm) = 10–9 mètres
1 millimicron (mµ) = 1 nm
10 angströms (Å) = 1 nm
Remarque : La molécule excitée pourra dissiper son énergie absorbée en émettant de la chaleur
ou de la lumière (par exemple, dans les phénomènes de fluorescence et de phosphorescence).
Tableau 5.a Unités des spectres dans l’ultraviolet et le visible
Région du spectre Unités actuelles Anciennes unités
Visible (vis) 400–800 nm 4 000–8 000 Å
Ultraviolet (UV) 200–400 nm 2 000–4 000 Å
Chimie organique 1 – Chapitre 5 – Complément © 2008 Les Éditions de la Chenelière inc. 1
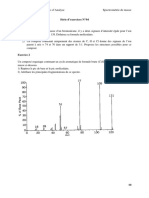
Figure 5.a Spectre d’absorption du 4-méthylpent-3-én-2-one
La figure 5.a montre un spectre d’absorption ultraviolet typique. Contrairement aux
spectres infrarouges, les spectres ultraviolets-visibles sont assez étendus et ne
comportent généralement qu’un petit nombre de bandes d’absorption. Chaque bande
d’absorption est enregistrée à la longueur d'onde à laquelle l’absorbance maximale
survient (λmax). La cétone conjuguée et insaturée dont le spectre est montré à la figure 5.a
présente une absorption intense à λmax = 232 nm et une absorption notablement plus faible
à λmax = 330 nm.
L’intensité d’une bande d’absorption peut être exprimée quantitativement. Cette intensité
est fonction de la structure de la molécule, mais aussi du nombre de molécules qui
absorbent les radiations dans le trajet du faisceau. Si l’on suppose qu’un faisceau de
lumière à une longueur d’onde donnée traverse un échantillon absorbant situé dans une
cuvette d’épaisseur A (voir la figure 5.b), l’absorbance correspond au logarithme du
rapport de l’intensité du faisceau incident (I0) sur celle du faisceau sortant (I) de
l’échantillon, tel que montré par l’équation 5.a. Cette équation est en fait la loi de Beer-
Lambert 1 .
L’absorbance d’un échantillon dépend de la structure moléculaire et du nombre de
molécules (concentration), à une longueur d’onde déterminée.
1
En l’honneur du mathématicien, physicien et astronome français Johann Heinrich Lambert (1728-1777) et
du mathématicien, chimiste et physicien allemand August Beer (1825-1863) qui découvrirent cette loi à des
moments distincts, respectivement en 1760 et en 1852.
Dans certains pays, notamment en Russie, cette loi porte le nom du mathématicien, physicien et
hydrographe français Pierre Bouguer (1698-1758) qui élabora cette loi en 1729 (on parle de la loi de
Bouguer ou de la loi de Beer-Lambert-Bouguer).
Chimie organique 1 – Chapitre 5 – Complément © 2008 Les Éditions de la Chenelière inc. 2
Figure 5.b Illustration du faisceau de lumière incident I0 traversant une cuvette
contenant l’échantillon étudié. Le faisceau sortant est désigné par I.
Io I
I0
A = log = - log T = ε A c (équation 5.a)
I
où A (qui n’a pas d’unité) est l’absorbance de l’échantillon à la longueur d’onde (λ)
sélectionnée (qui correspond généralement à la longueur d’onde où l’absorbance est
maximale); ε (la lettre grecque epsilon) représente l’absorptivité molaire, aussi parfois
appelé cœfficient d’extinction molaire, (mol-1 ⋅L ⋅cm-1), c est la concentration de la
solution (mol/L) et A, la distance parcourue par le faisceau dans l’échantillon, soit la
largeur de la cuvette (cm).
Remarque : Dans un graphique de l’absorbance en fonction de la concentration (A = y et c = x),
la pente de la droite obtenue correspond au produit du coefficient d’extinction molaire avec la
largeur de la cellule (m = ε ⋅ A).
A=εlc
y = mx
Chimie organique 1 – Chapitre 5 – Complément © 2008 Les Éditions de la Chenelière inc. 3
La valeur de ε pour toutes les bandes d’absorption du spectre d’un composé est une
constante caractéristique d’une structure moléculaire donnée à une longueur d’onde
donnée. Les valeurs de ε sont donc différentes d’une bande à l’autre dans un spectre
d’absorption. Par exemple, les valeurs de ε pour les bandes du spectre de la cétone
insaturée montrées à la figure 5.a sont λmax = 232 nm (ε = 12 600 mol-1 ⋅L ⋅cm-1) et
λmax = 330 nm (ε = 78 mol-1 ⋅L ⋅cm-1).
Exemple 5.a
Si on doublait la concentration d’un échantillon donné, quel en serait l’effet sur
l’absorbance A ? Quel en serait l’effet sur le coefficient d’extinction molaire ε ?
Solution
L’absorbance observée A doublerait puisque l’absorbance est directement proportionnelle
à la concentration selon la loi de Beer-Lambert. Toutefois, la valeur de ε dépend de la
nature de la substance absorbante (et de la longueur d’onde) et demeure donc constante,
c’est-à-dire qu’elle est indépendante de la concentration.
Exercice 5.a
Une solution de (CH3)2C=CHCOCH3, la cétone dont le spectre est illustré à la figure 5.a,
est placée dans une cellule dont la largeur est de 1 cm et donne un pic à λmax = 232 nm
avec une absorbance observée de A = 2,2. Calculez la concentration de la solution.
Utilisez la valeur de ε mentionnée dans le texte ci-dessus.
Les spectres ultraviolets-visibles servent surtout à déceler la présence de
conjugaison. En général, les molécules sans liaisons doubles ou avec uniquement une
liaison double n’absorbent pas dans la région de l’ultraviolet-visible (de 200 nm à
800 nm), contrairement aux systèmes conjugués. Cela est dû au fait que la liaison σ
possède une trop grande différence d’énergie entre son orbitale moléculaire de plus haut
niveau d’énergie occupée (orbitale liante) et celle inoccupée de plus bas niveau d’énergie
(orbitale anti-liante). Il faudrait donc fournir une énergie nettement supérieure à celle
observée dans le domaine de l’UV-visible pour pouvoir réaliser cette transition
électronique. Or, dans le cas de liaisons doubles conjuguées, les transitions électroniques
entre les orbitales moléculaires liante et anti-liante des liaisons π sont plus faibles en
énergie.
Plus la conjugaison est importante, plus la longueur d'onde de l’absorption maximale est
grande (et donc l’énergie est minimale), comme il est démontré dans les exemples
suivants, à la figure 5.c.
Chimie organique 1 – Chapitre 5 – Complément © 2008 Les Éditions de la Chenelière inc. 4
Figure 5.c Divers systèmes conjugués avec les longueurs d’onde d’absorption
maximale et les coefficients d’extinction molaire ε correspondants
CH2 CH CH CH2 CH2 CH CH CH CH CH2
λmax = 220 nm λmax = 257 nm
(ε = 21 mol-1 L cm-1) (ε = 35 mol-1 L cm-1)
CH2 CH CH CH CH CH CH CH2
λmax = 287 nm
(ε = 52 mol-1 L cm-1)
λmax = 255 nm λmax = 314 nm λmax = 380 nm
(ε = 215 mol-1 L cm-1) -1
(ε = 289 mol L cm ) -1
(ε = 9000 mol-1 L cm-1)
λmax = 480 nm
(ε = 13 mol-1 L cm-1)
Exercice 5.b
Selon vous, lequel des composés aromatiques suivants absorbera à la plus grande
longueur d'onde ?
ou CH2
Chimie organique 1 – Chapitre 5 – Complément © 2008 Les Éditions de la Chenelière inc. 5
Solutionnaire des exercices du complément
5.a La loi de Beer-Lambert est : A = ε A c
En isolant c, on obtient :
c = A / ε A = 2,2 / (12 600 mol-1 L cm-1 x 1 cm) = 1,7 x 10-4 mol/L
5.b Dans le biphényle (structure de gauche), toutes les liaisons doubles sont conjuguées
les unes avec les autres. Par contre, le diphénylméthane (structure de droite) ne
possède pas une conjugaison dans toute sa structure, car le groupement -CH2-
interrompt cette conjugaison. Puisque la longueur d’onde est directement
proportionnelle à l’ampleur du système conjugué au sein d’une structure, c’est le
biphényle qui aura la plus grande longueur d’onde d’absorption.
Chimie organique 1 – Chapitre 5 – Complément © 2008 Les Éditions de la Chenelière inc. 6
You might also like
- Contrat de Travail Duree Indeterminee PDFDocument3 pagesContrat de Travail Duree Indeterminee PDFMoussa Tamba100% (1)
- Exercice 1Document1 pageExercice 1Redha Alouaoui100% (1)
- Fluorimetrie PDFDocument12 pagesFluorimetrie PDFЮляВиталикNo ratings yet
- Les Conditions de La PolygamieDocument5 pagesLes Conditions de La Polygamiewakilazer100% (1)
- Fiche Droit Penal SpecialDocument38 pagesFiche Droit Penal Specialfafinette75% (4)
- Série 1 UVDocument3 pagesSérie 1 UVam.ayouazNo ratings yet
- LPVPT - TD N°1 - TD N°2Document30 pagesLPVPT - TD N°1 - TD N°2Mimi BCGNo ratings yet
- 2008 IR RMN CorrectionDocument17 pages2008 IR RMN CorrectionKadaNo ratings yet
- Série de TD #01 Corrigé - TextMarkDocument6 pagesSérie de TD #01 Corrigé - TextMarknadjet polyNo ratings yet
- TD 1 Techniques D'analysesDocument4 pagesTD 1 Techniques D'analysesGalounou IssaNo ratings yet
- Serie 2Document1 pageSerie 2mirouNo ratings yet
- Fiche TD 2 IR PDFDocument2 pagesFiche TD 2 IR PDFIk RamNo ratings yet
- Expose de ChromatographieDocument19 pagesExpose de ChromatographieJunior MbatepNo ratings yet
- Tables IRDocument6 pagesTables IRbouchane mariaNo ratings yet
- TD° 5 C433 - CopieDocument3 pagesTD° 5 C433 - CopieRayene BARNo ratings yet
- Ill-Procédure de Collecte Et D'envoi Des Souches BactériennesDocument4 pagesIll-Procédure de Collecte Et D'envoi Des Souches BactériennesBAURICE COMPUTER BAURICE COMPUTERNo ratings yet
- RMN 2DDocument14 pagesRMN 2Dezo ezoNo ratings yet
- Cours N 02Document6 pagesCours N 02rou röuNo ratings yet
- Série TD 1Document3 pagesSérie TD 1Čœür Dê MįēlNo ratings yet
- Fiche TD 2 MPCA 2023 2024Document4 pagesFiche TD 2 MPCA 2023 2024Clash of Clans Bilal DzNo ratings yet
- 2 Pol RefractoDocument4 pages2 Pol RefractoEssassi AmmarNo ratings yet
- Série de TD 1Document2 pagesSérie de TD 1Muhammed AddalaNo ratings yet
- Spectro IRDocument9 pagesSpectro IRfatima azalmad100% (1)
- Mecanismes Reactionnels Cours LeconteDocument16 pagesMecanismes Reactionnels Cours LeconteNajimou Alade Tidjani100% (1)
- Belhammou SeifeddineDocument35 pagesBelhammou SeifeddineAnissa Villa100% (3)
- Série Dexercices 4 - Spectrométrie de MasseDocument4 pagesSérie Dexercices 4 - Spectrométrie de MasseMarius MissiNo ratings yet
- Chapitre C3 ConductimetrieDocument5 pagesChapitre C3 ConductimetrieMANSOURINo ratings yet
- S6 Chapitre 6 Cinetique Chimique PDFDocument12 pagesS6 Chapitre 6 Cinetique Chimique PDFAzizElheni100% (1)
- Polycopié Exercices PDFDocument6 pagesPolycopié Exercices PDFTaouil MohamedNo ratings yet
- Série Dexercices 2 - Spectrométrie Infra RougeDocument3 pagesSérie Dexercices 2 - Spectrométrie Infra RougeSamar ZedamNo ratings yet
- L3 TAA Toutes Les Series TD TABCorrigésDocument27 pagesL3 TAA Toutes Les Series TD TABCorrigésIbtissam HmNo ratings yet
- Chapitre II - Application de La Spectroscopie UV-VisibleDocument18 pagesChapitre II - Application de La Spectroscopie UV-VisibleBrahim El Makhate100% (1)
- Comment Rédiger Un Rapport ScientifiqueDocument15 pagesComment Rédiger Un Rapport ScientifiqueKhaoula SettaraNo ratings yet
- Polycopié de Biophysique-28!03!2020Document77 pagesPolycopié de Biophysique-28!03!2020Oumia HarbitNo ratings yet
- TD Chromatographie en Phase Gazeuse de L3Document6 pagesTD Chromatographie en Phase Gazeuse de L3Kharoubi NassimaNo ratings yet
- Tables IrDocument5 pagesTables IrMahmoud AyadNo ratings yet
- Loi de Beer LambertDocument2 pagesLoi de Beer Lambertamine100% (1)
- Corrige Session 2 2015Document4 pagesCorrige Session 2 2015Moha MohaNo ratings yet
- Serie3 Corrections PDFDocument4 pagesSerie3 Corrections PDFmirouNo ratings yet
- Ds 2 CorrigéDocument22 pagesDs 2 CorrigéSouad BouafiaNo ratings yet
- IntroductionDocument29 pagesIntroductionchaou chaimaNo ratings yet
- Série n6 SPECTRO DE MASSE PDFDocument3 pagesSérie n6 SPECTRO DE MASSE PDFMahdi Jmai100% (1)
- TP C1. Bleu de Méthylène Dans Un Collyre: ObjectifDocument3 pagesTP C1. Bleu de Méthylène Dans Un Collyre: ObjectifRyan BoucettaNo ratings yet
- RMN (2017-2018)Document58 pagesRMN (2017-2018)Walid AbouloifaNo ratings yet
- Corrigé-Type TD 3Document18 pagesCorrigé-Type TD 3biochimie L30% (1)
- Chapitre IV 1Document37 pagesChapitre IV 1sidiNo ratings yet
- TP - Spectroscopie IR - CorrectionDocument2 pagesTP - Spectroscopie IR - CorrectionJojo BoubNo ratings yet
- Cours Mec FluorescenceDocument54 pagesCours Mec FluorescenceAlain BeauNo ratings yet
- Cours de CCMDocument15 pagesCours de CCMHouria NacerNo ratings yet
- Exercices de TD de ChromatographieDocument3 pagesExercices de TD de ChromatographieDjibrine Habib Hissein100% (1)
- ChromatographieDocument10 pagesChromatographieAbdelhakim BailalNo ratings yet
- Correction Serie3Document2 pagesCorrection Serie3mirouNo ratings yet
- Spectrometrie de Masse LPVPT 2022 - 2023Document81 pagesSpectrometrie de Masse LPVPT 2022 - 2023Mimi BCG100% (1)
- Cours - HADDADI GUEMGHAR Hayate - Méthodes SéparativesDocument78 pagesCours - HADDADI GUEMGHAR Hayate - Méthodes SéparativesAl moukhtar BaNo ratings yet
- Cours - Exercices de Chromatographie Ex1Document2 pagesCours - Exercices de Chromatographie Ex1Farid HammouNo ratings yet
- TP Biochimie Analytique 2017-2018Document19 pagesTP Biochimie Analytique 2017-2018Frédéric KTchinfanbéNo ratings yet
- Corrigé-Type TD 3 - SuiteDocument14 pagesCorrigé-Type TD 3 - Suitebiochimie L3No ratings yet
- Atomic Spectrometrie Rev2Document15 pagesAtomic Spectrometrie Rev2Merouane TouatiNo ratings yet
- Cours 11 Méthodes Spectrophotometrique PDFDocument6 pagesCours 11 Méthodes Spectrophotometrique PDFJilani BejaouiNo ratings yet
- Exo SpecstroscopieDocument17 pagesExo SpecstroscopieMelainine Tounsy100% (1)
- C04 RMN Diapo - PpsDocument16 pagesC04 RMN Diapo - PpsccstchmiNo ratings yet
- Applications de la spectrophotomérie en phytochimie: sciencesFrom EverandApplications de la spectrophotomérie en phytochimie: sciencesNo ratings yet
- Oxydation Des Colorants Par Les Procedes Doxydation Avancee Sur Des Catalyseurs A Base de La Montmorillonite Modifiee PDFDocument48 pagesOxydation Des Colorants Par Les Procedes Doxydation Avancee Sur Des Catalyseurs A Base de La Montmorillonite Modifiee PDFBibi BibaNo ratings yet
- Ben Guell A 2009Document10 pagesBen Guell A 2009Bibi BibaNo ratings yet
- Intro Coll o Que 130110Document9 pagesIntro Coll o Que 130110Saloum ThioubNo ratings yet
- Serie1 Org2-1Document2 pagesSerie1 Org2-1Bibi Biba100% (1)
- 3 Les Liaisons Chimiques - Theorie - 2013Document24 pages3 Les Liaisons Chimiques - Theorie - 2013Bibi BibaNo ratings yet
- Plan de CoursDocument4 pagesPlan de CoursBibi BibaNo ratings yet
- Les Modeles D Analyse StrategiqueDocument9 pagesLes Modeles D Analyse StrategiqueBibi BibaNo ratings yet
- Exer Spectro Suppl Et CorrigeDocument50 pagesExer Spectro Suppl Et CorrigeBibi BibaNo ratings yet
- 5 Substitution Electrophile 2Document11 pages5 Substitution Electrophile 2Bibi BibaNo ratings yet
- AD ChimiosélectivitéDocument4 pagesAD ChimiosélectivitéBibi BibaNo ratings yet
- Objectif BAC 3Document2 pagesObjectif BAC 3Bibi BibaNo ratings yet
- 3méthodologie D - Analyse Urbaine DDocument4 pages3méthodologie D - Analyse Urbaine DBibi Biba100% (1)
- Exer Spectro Suppl Et Corrige PDFDocument34 pagesExer Spectro Suppl Et Corrige PDFBibi Biba0% (1)
- 2 Addition Electrophile 2Document10 pages2 Addition Electrophile 2Bibi BibaNo ratings yet
- The Holy Quran (Full) القران الكريم - نسخة كاملة من المصحف الكريمDocument569 pagesThe Holy Quran (Full) القران الكريم - نسخة كاملة من المصحف الكريمikarus kuwait100% (15)
- LANGAGES 23 - 01 - Discours Politique (GUESPIN, Problématiques Des Travaux Sur Le Discours Politique) (1971)Document23 pagesLANGAGES 23 - 01 - Discours Politique (GUESPIN, Problématiques Des Travaux Sur Le Discours Politique) (1971)EDisPALNo ratings yet
- TabelaDocument17 pagesTabelaNelson LoboNo ratings yet
- Bon Sortie MaterielDocument48 pagesBon Sortie Materielhachani ibrahimNo ratings yet
- La Lucha TshisekediDocument10 pagesLa Lucha Tshisekedi8rvz5qg7rmNo ratings yet
- GF Examen 2017 (Enoncé + Corrigé)Document7 pagesGF Examen 2017 (Enoncé + Corrigé)Jghider JuniorNo ratings yet
- Lexique ManagementDocument7 pagesLexique ManagementDeeneesh moturNo ratings yet
- Conditions Geěneěrales D'utilisation - Bank To WalletDocument3 pagesConditions Geěneěrales D'utilisation - Bank To WalletPapa sissao DiedhiouNo ratings yet
- Rapport de Synthèse Sur L - Audit Fiscal Au MarocDocument19 pagesRapport de Synthèse Sur L - Audit Fiscal Au MarocKarim BenjebbourNo ratings yet
- 021 - Politique Salariale (Classes 1 À 6) - QC - F.1.0Document2 pages021 - Politique Salariale (Classes 1 À 6) - QC - F.1.0Ellie ChrétienNo ratings yet
- Chap 2 Le Bilan Enregistrement Des Écritures ProfDocument8 pagesChap 2 Le Bilan Enregistrement Des Écritures ProfNico. BenoitNo ratings yet
- 30 Informatique Teleinformatique Definitifs 2023Document3 pages30 Informatique Teleinformatique Definitifs 2023AmstrongNo ratings yet
- Analyste Risques de Crédit PDFDocument3 pagesAnalyste Risques de Crédit PDFnacima201206No ratings yet
- Demande VirementDocument3 pagesDemande VirementQrlNo ratings yet
- 1000 Fevrier 2018 Special 1000eDocument72 pages1000 Fevrier 2018 Special 1000eSamîh KouddârNo ratings yet
- EWS - ForensicDocument48 pagesEWS - ForensicrmigrecNo ratings yet
- Droit Des Transports CompletDocument27 pagesDroit Des Transports CompletKaris Shine SpArowzzNo ratings yet
- Kbis - 32739 - 11 30 2021 12 37 41Document2 pagesKbis - 32739 - 11 30 2021 12 37 41emokasahanNo ratings yet
- Martisnisme - Annales Martinistes Des Origines À Nos JoursDocument19 pagesMartisnisme - Annales Martinistes Des Origines À Nos JoursodecracNo ratings yet
- Conditions de BanqueDocument10 pagesConditions de BanqueMoh AmedNo ratings yet
- Cours 21 - Exprimer Son Accord Et Son DésaccordDocument2 pagesCours 21 - Exprimer Son Accord Et Son DésaccordGabriela da Costa GonçalvesNo ratings yet
- Impôt Sur La Société ExercicesDocument5 pagesImpôt Sur La Société ExercicesomarNo ratings yet
- Jonh Locke - Traité Sur La Tolérance - 40-49Document4 pagesJonh Locke - Traité Sur La Tolérance - 40-49lapointe gabrielNo ratings yet
- CasnosDocument5 pagesCasnosMOKRANI50% (2)
- Décl Revenu GlobalDocument5 pagesDécl Revenu GlobalredalouziriNo ratings yet
- CivilisationDocument3 pagesCivilisationlady anasthasyaNo ratings yet
- 7-Configuration de Accés DistantDocument50 pages7-Configuration de Accés DistantMoustapha SanoussiNo ratings yet