Professional Documents
Culture Documents
P8
Uploaded by
Ernesto Muñoz PalmaCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
P8
Uploaded by
Ernesto Muñoz PalmaCopyright:
Available Formats
PRCTICA 8
CLCULO DEL CALOR DE DISOLUCIN POR MEDIDAS DE SOLUBILIDAD
1.- FUNDAMENTO TERICO Conceptos generales Cuando vertemos azcar en el caf y agitamos el lquido, estamos preparando una disolucin, una mezcla homognea de varias sustancias. Si en lugar de leche y azcar usamos agua y sal, tambin nos referimos a una disolucin. Imaginemos que en medio vaso de agua, aadimos media cucharada de sal y agitamos. El resultado es que la sal se disuelve y desaparece. Parece como si slo hubiese agua en el vaso, sin embargo su sabor salado nos indica que contiene sal. La sal, que es la sustancia que se disuelve se denomina soluto, mientras que el agua, que es la sustancia en la que se dispersa se llama disolvente. El conjunto de agua y sal recibe el nombre de disolucin o solucin. En general, es fcil distinguir entre soluto y disolvente ya que el primero est en menor proporcin. A la cantidad de soluto disuelto en una determinada cantidad de disolvente se le denomina concentracin. Puesto que la cantidad de sal (soluto) en el agua (disolvente) es poca, decimos que la disolucin es diluida. Si echamos una cucharada ms de sal y volvemos a agitar, la disolucin se dice que est concentrada, porque hay mucha cantidad de soluto. Si volvemos a echar otras dos cucharadas de sal, por ms que agitemos queda un resto en el fondo del vaso sin disolverse. La disolucin est ahora saturada. La concentracin de esa disolucin saturada es la solubilidad de la sal. Al calentar el agua, veremos que se disuelve ms cantidad, lo que quiere decir que la solubilidad vara con la temperatura. Normalmente los slidos, como la sal, el azcar o el bicarbonato aumentan su solubilidad con la temperatura, mientras que los gases, como el dixido de carbono o el oxgeno, la disminuyen. Por ello, cuando en el laboratorio encontramos dificultades para disolver un slido en un disolvente lquido, a veces se recurre a calentar ligeramente la disolucin. Al hacerlo, incrementamos la energa cintica de las molculas de soluto y disolvente, favoreciendo as la aparicin de un sistema homogneo. Por ejemplo, el biftalato potsico ( ftalato cido de potasio) es una sustancia patrn que se emplea para valorar bases. A veces se requiere emplear disoluciones relativamente concentradas de esta sal, encontrando serios problemas para solubilizarla. En este caso, el problema se resuelve calentando un poco y agitando.
8-1
De todo ello se deduce que existe una dependencia entre la solubilidad y la temperatura, que puede describirse matemticamente como: Solubilidad = f (Temperatura); Solubilidad y Calor Cuando se disuelve NaOH en agua, se desprende energa en forma de calor1 . Este hecho experimental lo hemos podido constatar en el laboratorio (si no lo ha constatado an, lo har en breve). En general, todo proceso de disolucin lleva asociado un valor de energa (calor) que puede liberarse en el proceso, ocasionando un aumento de la temperatura. Tambin podra absorberse; en este caso provocara una disminucin. Cuando la disolucin tiene lugar en condiciones de presin constante, a esa energa absorbida o liberada, se la denomina calor de disolucin o entalpa de disolucin, Hdisolucin. Cuando durante el proceso, el sistema absorbe energa (calor) se dice que es endotrmico y viene caracterizado por un valor de Hdisolucin positivo. Cuando la energa se libera, el proceso es exotrmico y el signo de Hdisolucin es negativo. Solubilidad, temperatura y Hdisolucin La relacin matemtica que existe entre la solubilidad y la temperatura, queda reflejada en una funcin que engloba a la entalpa de disolucin: d ln s H Disolucin = ; dT RT 2 donde, s = solubilidad T = temperatura R = constante de los gases ideales Integrando y suponiendo que Hdisolucin es un valor constante que no depende de la temperatura, se llega a:
dln s =
H Disolucin dT; RT 2
ln s =
H Disolucin 1 + C; R T
Mtodo de ajuste por mnimos cuadrados. Regresin lineal La chicharra es un insecto hemptero del suborden de los hompteros que tiene un abdomen cnico en cuya base disponen los machos de un sistema con el cual producen un ruido estridente y montono. Recientemente, cientficos espaoles han descubierto que la frecuencia de su canto establece una relacin lineal con la temperatura. Es decir, cuanto mayor es la temperatura, tanto mayor es la frecuencia de su canto. Por el contrario, cuando la temperatura disminuye
1
Para conocer ms detalles sobre esta magnitud consulte en prctica 7: Calor de Neutralizacin.
8-2
tambin lo hace el nmero de chirridos. Lo interesante de esta conclusin es que si contamos el nmero de chirridos por unidad de tiempo podremos conocer, con un nivel de precisin aceptable, la temperatura ambiente.
Frecuencia de Chirridos
Temperatura
Figura 1
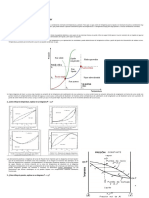
La grfica que se muestra en la figura 1 expresa, a grosso modo, esta relacin lineal. Como se ve, la funcin matemtica corresponde con una lnea recta. Es por eso que se le denomina relacin lineal. Matemticamente una lnea recta queda definida por la expresin, Y = A + BX Donde Y representa los valores mostrados en el eje vertical (ordenada). En el ejemplo anterior la variable Y representa la frecuencia de chirridos. La variable X corresponde con el eje horizontal ( abcisa) y en el ejemplo sera la temperatura. Los parmetros A y B (distngase parmetro de variable), son los que definen inequvocamente a la recta, es decir, dos rectas son diferentes o dicho de otro modo, dos relaciones lineales son distintas, si difieren en el valor de alguno de estos dos parmetros. A es el trmino independiente, denominado ordenada en el origen y corresponde con el valor de Y cuando X vale cero. B es la pendiente. Informa sobre la inclinacin de la recta y corresponde con la tangente del ngulo que forma con la horizontal. Cuando se trata de una recta horizontal B vale cero y cuando es vertical, no est definido. Existen infinidad de funciones matemticas aparte de sta, sin embargo, todas las dems son incapaces de reproducir con exactitud el trazado de una recta. Por esto y porque la relacin lineal queda totalmente definida con slo dos parmetros, en el mundo de la investigacin se busca con cierta ansiedad relacionar las variables estudiadas con una funcin lineal. De alguna manera constituye la mejor forma de simplificar el comportamiento de la naturaleza. Pero, en la investigacin sobre el canto de la chicharra, cmo se encontr la relacin lineal?. La metodologa es sencilla. Un seor se dedica a someter a la chicharra a ambientes a distinta temperatura controlada y a contar el nmero de chirridos por unidad de tiempo. La representacin grfica de los datos recopilados podra ser parecida a la que aparece en la figura 2. A simple vista se observa que los puntos se distribuyen ms o menos alrededor de una recta imaginaria y es aqu donde debemos aplicar un mtodo para encontrar los 8-3
parmetros A y B de esta recta: el mtodo de ajuste por mnimos cuadrados mtodo de regresin lineal .
Frecuencia de Chirridos
Temperatura
Figura 2
El mtodo consiste en calcular la distancia ms corta entre cada punto y la recta hipottica que se busca. La recta ms representativa es la que hace mnima estas distancias elevadas al cuadrado. El desarrollo del mtodo da como resultado las siguientes expresiones para A y B:
Y = A + BX ;
B=
( x x )( y y ) = n xy x y ; n x ( x) (x x )
2 2 2
A = y Bx =
y B x ;
n n
r=
xy x y ; {n x ( x) }{n y ( y) }
2 2 2 2
donde n es el nmero de pares de datos disponible y r es el coeficiente de regresin; un valor que nos indica si los datos se ajustan bien o no a una recta. Es importante entender esto ltimo. La aplicacin del mtodo de mnimos cuadrados SIEMPRE da como resultado una recta, sin embargo eso no quiere decir que los datos se ajusten bien a una relacin lineal. El valor de r est comprendido entre 1 y +1. Cuanto ms prximo sea a cualquiera de estos valores, ms ajustada es la distribucin de los datos a una relacin lineal. Pero si r vale cero o un valor prximo, entonces debemos descartar la existencia de una relacin lineal.
8-4
Frecuencia de Chirridos
II I
r = 0.9988236742
r = 0.0212637739 Y
Temperatura
Figura 3
La grfica I de la figura 3 muestra los datos y la recta obtenida por el ajuste de regresin lineal en el ejemplo de la chicharra. En este caso el valor r = 0.9988 indica que la distribucin es lineal. La grfica II corresponde a la obtenida por aplicacin del mismo ajuste sobre otros datos muy diferentes. Se observa que aunque el mtodo proporciona una recta, los datos no se ajustan linealmente. En este caso la recta debe rechazarse porque r es un valor muy cercano a cero. Aplicacin del mtodo de ajuste por mnimos cuadrados al clculo del calor de disolucin HDisolucin La expresin que relaciona la solubilidad con la temperatura es
ln s = HDisolucin 1 +C; R T
Obsrvese que las variables que ah aparecen se pueden asociar con los parmetros caractersticos de una distribucin lineal.
HDisolucion 1 +C R T
ln s =
Y = A + BX
Si representamos en el eje horizontal la variable recta ser
HDisolucin . R
1 y en el eje vertical la variable dada T
por ln s, si el coeficiente de regresin r, es cercano a 1 a 1, entonces la pendiente de esa
En definitiva, calculando la pendiente de la recta de ajuste a los datos experimentales que se obtendrn en esta prctica, podremos calcular el valor de HDisolucin. 2.- OBJETIVO DE LA PRCTICA Se pretende obtener experimentalmente el calor de disolucin del cido benzoico en agua por medidas de solubilidad y anlisis de regresin lineal (mtodo de ajuste por mnimos cuadrado). 8-5
3.- MATERIAL Y REACTIVOS MATERIAL 2 Matraces erlenmeyers de 250 ml con tapn. 2 Erlenmeyers de 100 ml. 1 Matraz Kitasato. 1 Matraz aforado de 250 ml. 1 Varilla de vidrio. 1 Embudo Buchner. 1 Bureta. 1 Bao termosttico. 1 Probeta de 250 ml. 1 Probeta de 25 ml. 1 Vaso de precipitados de 100 ml. 1 Vaso de precipitados de 500 ml. 1 Bomba de vaco. 1 Termmetro. Junta de goma para embudo Buchner. Papel de filtro. REACTIVOS cido benzoico. NaOH. Ftalato cido de potasio. Fenolftalena. 4.- PROCEDIMIENTO EXPERIMENTAL Disuelva en un erlenmeyer de 250 ml, 1 gramo de cido benzoico en 200 ml de agua (medidos en una probeta). Caliente en una placa calefactora y agite de vez en cuando hasta que se disuelva el contenido. Mientras tanto recorte cinco crculos en papel de filtro con las dimensiones del dimetro del embudo Buchner. Servirn para filtrar en ocasiones posteriores. Una vez disuelto el cido benzoico, tape el matraz y mrquelo como MUESTRA 1. Deje enfriar por contacto con el ambiente hasta 30C. Despus prepare otra disolucin como la anterior pero que contenga en este caso 3 g de cido benzoico. Caliente en una placa calefactora y agite de vez en cuando hasta que se disuelva el contenido. Una vez disuelto, marque el matraz como M UESTRA 2. Tpelo y djelo enfriar por contacto con el ambiente hasta 40 C.
En el transcurso de la espera se proceder a la preparacin de la disolucin de hidrxido sdico que se emplear posteriormente en la valoracin :
8-6
Preparacin de una disolucin de 250 ml NaOH 0.1 M Disuelva 1 g de NaOH en aproximadamente 100 ml de agua destilada. Adicinelo a un matraz aforado de 250 ml y enrase con agua destilada. Luego agite la disolucin. Factorizacin de la disolucin de NaOH 0.1 M Pese exactamente 0.2 gramos de ftalato cido de potasio y disulvalos en aproximadamente 50 ml de agua. Aada 2 gotas de fenolftalena y valore con la disolucin de NaOH que se aadir desde una bureta. Anote el volumen consumido en la tabla 5.1. y calcule la molaridad exacta de la disolucin de NaOH.
Una vez que la M UESTRA 1 ha alcanzado los 30C introdzcala en el bao termosttico a 25 C. All debe permanecer hasta alcanzar el equilibrio trmico. Agite de vez en cuando. Introduzca tambin la probeta de 25 ml, el kitasatos y un erlenmeyer de 100 ml, con la cantidad de agua purificada suficiente para vencer el empuje (principio de Arqumedes) y no vuelquen en el bao. (Se pretende que el instrumental tome la temperatura de trabajo). Las siguientes operaciones se realizarn en el seno del bao termosttico:
P ROCEDIMIENTO* :
Pase agua del erlenmeyer de 100 ml a travs del papel de filtro colocado previamente sobre el embudo Buchner, a fin de que las paredes vayan tomando la temperatura del bao. Filtre la muestra utilizando la bomba de vaco y el matraz kitasatos. Mida en la probeta exactamente, un volumen aproximado de 25 ml de disolucin filtrada. Vacese en el bao el resto de agua que contena el erlenmeyer de 100 ml y virtase en este mismo matraz el contenido de la probeta. Llene el vaso de 500 ml con agua del bao termostatizado e introdzcase en l, al bao Mara, el matraz erlenmeyer al que aadir 2 gotas de fenolftalena. Lleve el conjunto (vaso de 500 ml + erlenmeyer al bao Mara) hasta la bureta previamente enrasada con disolucin de NaOH y valore la muestra. Finalizada la valoracin devuelva el agua del bao Mara al bao termostatizado.
Anote el volumen consumido en la valoracin en el cuadro 5.2. Eleve la temperatura del termostato hasta 35C. 8-7
Lave el erlenmeyer de 250 ml utilizado como MUESTRA 1 y prepare en l una tercera disolucin con 3 g de cido benzoico en 200 ml de agua purificada. Calintela en la placa calefactora, agitando de vez en cuando. Cuando se haya disuelto todo el cido benzoico, tape el matraz, mrquelo como M UESTRA 3 y djelo enfriar por contacto con el ambiente hasta 45C. Vuelva a la M UESTRA 2. Cuando la disolucin alcance 40 C, introduzca el matraz en el bao termosttico hasta equilibrio trmico y opere como se indic en el apartado P ROCEDIMIENTO* . Valore aproximadamente 25 ml de la muestra, exactamente medidos, con NaOH 0.1 N y anote el volumen consumido en el cuadro 5.2. Eleve la temperatura del bao hasta 40C. Lave el erlenmeyer de 250 ml que emple en la M UESTRA 2 y prepare en l una cuarta disolucin con 3 g de cido benzoico en 200 de agua purificada. Caliente en la placa calefactora, agitando de vez en cuando. Cuando se haya disuelto todo el cido benzoico, tape el matraz, mrquelo como M UESTRA 4 y djelo enfriar por contacto con el ambiente hasta 55C. Vuelva a la M UESTRA 3. Cuando la disolucin alcance 45C, introduzca el matraz en el bao termosttico hasta equilibrio trmico y opere como se indic en el apartado P ROCEDIMIENTO* . Valore aproximadamente 25 ml de la muestra, exactamente medidos, con la disolucin de NaOH y anote el volumen consumido en la tabla 5.2. Eleve la temperatura del bao hasta 50C. Vuelva a la M UESTRA 4. Cuando la disolucin alcance 55 C, introduzca el matraz en el bao termosttico hasta equilibrio trmico y opere como se indic en el apartado P ROCEDIMIENTO* . Valore aproximadamente 25 ml de la muestra exactamente medidos con NaOH 0.1 N y anote el volumen consumido en el cuadro 5.2.
CLCULOS:
Realice los clculos pertinentes para rellenar las tablas 5.2 y 5.3. Represente los datos de la tabla 5.3 en la grfica que se adjunta (figura 4) y aplique el mtodo de regresin lineal para encontrar la recta que mejor se adapta a los resultados experimentales. (Se aconseja el empleo de calculadora) Calcule los siguientes datos y antelos en la tabla 5.4. 1. Ordenada en el origen 2. Pendiente 3. Coeficiente de regresin A partir de los datos obtenidos deduzca el valor de HDisolucin y antelo en la tabla 5.4.
8-8
5.- RESULTADOS EXPERIMENTALES
5.1.- Datos referidos a la factorizacin de la disolucin de NaOH 0.1 M Masa pesada de biftalato (gr) VNaOH (ml)
MNaOH
5.2.- Tabla de resultados Volumen valorado (/ml) Muestra Muestra Muestra Muestra 1 2 3 4 (25C) (35C) (40C) (50C) Moles de cido benzoico Masa de cido benzoico (/gr) Solubilidad (g/l)
5.3.- Tabla de datos para la representacin grfica. T (/C) T (/K) Solubilidad (g/l) 25 35 40 50 5.4.- Datos derivados del anlisis de regresin lineal Ordenada en el origen: Pendiente:
ln s
1 / T (/K )
-1
Coeficiente de regresin:
HDisolucin :
2.5 2.4 2.3 2.2 2.1 2.0 1.9
ln s
1.8 1.7 1.6 1.5 1.4 1.3 1.2 1.1 1.0
3.0x10 -3 3.1x10-3 3.1x10 -3 3.2x10-3 3.2x10 -3 3.3x10-3 3.3x10 -3 3.4x10 -3 3.4x10-3
1 / T (K-1)
Figura 4
8-9
You might also like
- Calor de disolución del ácido benzoicoDocument4 pagesCalor de disolución del ácido benzoicoGICELANo ratings yet
- Día 3 Curso de Termodinámica (Resoluciones)Document7 pagesDía 3 Curso de Termodinámica (Resoluciones)Serena Libros MendezNo ratings yet
- Informe Liquidos No MisciblesDocument18 pagesInforme Liquidos No Misciblesyasminkjl21No ratings yet
- UntitledDocument7 pagesUntitledAndrés Méndez EscurraNo ratings yet
- Dia. Fase - Balance 1 comp-GRUPO N°4Document13 pagesDia. Fase - Balance 1 comp-GRUPO N°4Marcelo TorresNo ratings yet
- Regresion LinealDocument6 pagesRegresion LinealAntonio Carvajal0% (1)
- Práctica 4 - Gases IdealesDocument6 pagesPráctica 4 - Gases IdealesCinthia Tamara100% (1)
- Constante de Equilibrio: Disolución de KNO3Document8 pagesConstante de Equilibrio: Disolución de KNO3Julio MuñozNo ratings yet
- Convección de MasaDocument5 pagesConvección de MasaELIZABETH RAQUEL MENA DIONICIONo ratings yet
- Informe Práctica #3 Punto de BurbujaDocument5 pagesInforme Práctica #3 Punto de BurbujaDiego Nicolas ManceraNo ratings yet
- 2 - Unidad II - Equilibrio de FasesDocument71 pages2 - Unidad II - Equilibrio de Faseseldoradode666No ratings yet
- HumidificaciónDocument12 pagesHumidificaciónSol RodríguezNo ratings yet
- Laboratorio Entalpia de VaporizacionDocument11 pagesLaboratorio Entalpia de VaporizacionIz RemyNo ratings yet
- PR - CTICA No 1Document5 pagesPR - CTICA No 1Elmas AleatorioNo ratings yet
- Resumen Capitulo 15 CastellanDocument30 pagesResumen Capitulo 15 CastellanAlejandro Garcia GarciaNo ratings yet
- Unidad I Fisicoquimica II 2020Document14 pagesUnidad I Fisicoquimica II 2020Antonela YanethNo ratings yet
- 02-Propiedades ColigativasDocument16 pages02-Propiedades ColigativasMaría Constanza BritoNo ratings yet
- Resumen FisicoquimicaDocument24 pagesResumen FisicoquimicaXiime WalburgNo ratings yet
- AsdasDocument13 pagesAsdasCristhyan Willy Raa TorresNo ratings yet
- FQ Clase 12 2022-2Document7 pagesFQ Clase 12 2022-2MIRANDA ALEXANDRA ESPINOZA URBINANo ratings yet
- Laboratorio N4Document6 pagesLaboratorio N4KAREN JULISSA Villa EspinosaNo ratings yet
- Diagrama de Fases para Mezclas de Liquidos Parciales MisciblesDocument4 pagesDiagrama de Fases para Mezclas de Liquidos Parciales MisciblesSantiago Castro RengifoNo ratings yet
- Variacion de La Solubilidad 1Document25 pagesVariacion de La Solubilidad 1ivan gallegos huamanNo ratings yet
- Proyecto Final FQ.Document29 pagesProyecto Final FQ.MariaNo ratings yet
- Diagrama de Fases para Mezclas de Liquidos Parciales MisciblesDocument4 pagesDiagrama de Fases para Mezclas de Liquidos Parciales MisciblesSantiago CastroNo ratings yet
- Wuolah-Capítulo 6Document5 pagesWuolah-Capítulo 6ksaweryjpcNo ratings yet
- Entalpía de Vaporización de Un Líquido PuroDocument4 pagesEntalpía de Vaporización de Un Líquido PuromagicianchemistNo ratings yet
- Equilibrio QuimicoDocument15 pagesEquilibrio QuimicoAlexander Yauri GomezNo ratings yet
- Practica 1 de Termodinamica de FasesDocument18 pagesPractica 1 de Termodinamica de FasesAlberto Arteaga100% (1)
- TERMOQUÍMICADocument16 pagesTERMOQUÍMICANaty ZothyNo ratings yet
- Investigar Sobre Concentración de SolucionesDocument11 pagesInvestigar Sobre Concentración de SolucionesJulio Enrique Mendoza MosqueraNo ratings yet
- Informe de Laboratorio N°7 TermodinámicaDocument7 pagesInforme de Laboratorio N°7 TermodinámicaRoger LopezNo ratings yet
- Lab 5 - Presin Vs TemperaturaDocument4 pagesLab 5 - Presin Vs TemperaturaD Carolina Meneses100% (1)
- Propiedades ColigativasDocument14 pagesPropiedades ColigativasLUAR PADRONNo ratings yet
- Cuestionario Previo 8 (Ley de Charles) - 1 - 278Document9 pagesCuestionario Previo 8 (Ley de Charles) - 1 - 278Alan Alberth OHNo ratings yet
- Diferencia Entre Gas y VaporDocument8 pagesDiferencia Entre Gas y VaporJosé TorrezNo ratings yet
- Equilibrio HeterogeneoDocument50 pagesEquilibrio HeterogeneoEliana picoNo ratings yet
- Condiciones de equilibrio y espontaneidad en sistemas termodinámicosDocument3 pagesCondiciones de equilibrio y espontaneidad en sistemas termodinámicosPatricia LeónNo ratings yet
- Determinación de La Constante de Henry de CO2 en AguaDocument5 pagesDeterminación de La Constante de Henry de CO2 en AguaLaura Rodríguez100% (2)
- Ley de HenryDocument7 pagesLey de HenryJuan Luis Ramírez AgudeloNo ratings yet
- TP 3 Volumetría de PrecipitaciónDocument4 pagesTP 3 Volumetría de PrecipitaciónSerena Méndez LLanquetruNo ratings yet
- BenzoicoDocument5 pagesBenzoicoErick LópezNo ratings yet
- Clase Fisico PDFDocument62 pagesClase Fisico PDFKaren Estefany Pulamarin DíazNo ratings yet
- 01-Gas Ideal PDFDocument8 pages01-Gas Ideal PDFKathyPazmiñoViteriNo ratings yet
- Propiedades ColigativasDocument10 pagesPropiedades ColigativasElectromotrizTorres TorresNo ratings yet
- Lección 31 El LaplacianoDocument9 pagesLección 31 El LaplacianovidriosNo ratings yet
- Determinacion de Calor LatenteDocument9 pagesDeterminacion de Calor LatenteEstuardo Javier Gan Rodríguez100% (1)
- LabFIQUI-I-"PRESIÓN DE VAPOR DE LÍQUIDOS PUROS"BDocument9 pagesLabFIQUI-I-"PRESIÓN DE VAPOR DE LÍQUIDOS PUROS"Bcefiqt100% (2)
- Gases ideales y ecuaciones de estadoDocument12 pagesGases ideales y ecuaciones de estadoAnahis CalderonNo ratings yet
- Determinación de Entalpías de RXN y de FormaciónDocument6 pagesDeterminación de Entalpías de RXN y de FormaciónMary GuerraNo ratings yet
- Resolución Ejercicios - Serie 3 PDFDocument29 pagesResolución Ejercicios - Serie 3 PDFmatias100% (1)
- 01-Gas IdealDocument11 pages01-Gas IdealEduardo AlemánNo ratings yet
- Presión de Vapor y Ecuaciones de EstadoDocument8 pagesPresión de Vapor y Ecuaciones de EstadoVALENTINA RUIZ GARCIANo ratings yet
- EdpDocument34 pagesEdpSantiago LampreaNo ratings yet
- Laboratorio de Fisica 2: Leyde PascalDocument7 pagesLaboratorio de Fisica 2: Leyde Pascalesteban19913No ratings yet
- Tema 3-Propiedades de Las Sutancias Puras y Mezclas-19-3Document46 pagesTema 3-Propiedades de Las Sutancias Puras y Mezclas-19-3Armando CastroNo ratings yet
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSFrom EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSRating: 4.5 out of 5 stars4.5/5 (7)
- Calor de disolución del ácido benzoicoDocument9 pagesCalor de disolución del ácido benzoicoErnesto Muñoz PalmaNo ratings yet
- P12Document5 pagesP12d.rios.a7585No ratings yet
- BenzoicoDocument5 pagesBenzoicoErick LópezNo ratings yet
- Calor de disolución del ácido benzoicoDocument9 pagesCalor de disolución del ácido benzoicoErnesto Muñoz PalmaNo ratings yet