Professional Documents
Culture Documents
Termoquc 3 Admica
Uploaded by
Percy R. Samaniego ValdezOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Termoquc 3 Admica
Uploaded by
Percy R. Samaniego ValdezCopyright:
Available Formats
Colegio Andrs Bello
Chiguayante
Jorge Pacheco R.
Profesor de Biologa y Qumica
UNIDAD I: TERMOQUMICA
Captulo 1: FUNDAMENTOS
DE LA TERMOQUMICA
TERMOQUMICA
APRENDIZAJES ESPERADOS:
Relacionan reacciones qumicas con
intercambios de energa.
Reconocen el primer principio de la
termodinmica como un caso
particular del principio de la
conservacin de la energa.
Aplican el concepto de la entalpa a
situaciones de la vida cotidiana.
PREGUNTAS PREVIAS
Qu es la Energa?
Del griego energeia: actividad,
operacin; energos: fuerza de accin o
fuerza trabajando.
La energa es una magnitud fsica que
asociamos con la capacidad que tienen
los cuerpos para producir trabajo
mecnico, emitir luz, generar calor, etc.
PREGUNTAS PREVIAS
Qu tipos de energa conoces?
Energa Potencial.
Energa Cintica.
Energa Qumica.
Energa Elctrica.
Energa Trmica.
Energa Magntica.
Energa Nuclear
Energa Radiante.
PREGUNTAS PREVIAS
Calor y Temperatura, son lo mismo?
Calor corresponde a la transferencia
de energa entre cuerpos o diferentes
zonas de un mismo cuerpo que se
encuentran a distintas temperaturas.
Temperatura es una medida de la
energa cintica de las molculas de
un sistema.
FUNDAMENTOS DE LA
TERMODINMICA
TERMOQUMICA
Corresponde al rea de la
qumica que estudia las
transferencias de calor
asociadas a las reacciones
qumicas.
TERMOQUMICA
SISTEMA
El sistema es lo que se desea estudiar, mientras que el
entorno es la zona en la que se produce algn intercambio
con el sistema.
Aquella separacin real entre el sistema y el entorno se
denominan lmites o paredes del sistema, mientras que el
conjunto de sistema y entorno se denomina universo.
UNIVERSO
SISTEMA + AMBIENTE = UNIVERSO
SISTEMA ABIERTO
Sistema que intercambian materia y energa con el
entorno.
SISTEMA CERRADO
Sistema que intercambian energa pero no materia
con el entorno.
SISTEMA AISLADO
Sistema en donde no existe intercambio de energa y
materia con el entorno.
CLASIFICACIN
Qu tipo de sistema es lo que representa la siguiente
imagen?
SISTEMA
CERRADO
CLASIFICACIN
Qu tipo de sistema es lo que representa la siguiente
imagen?
SISTEMA
ABIERTO
CLASIFICACIN
Qu tipo de sistema es lo que representa la siguiente
imagen?
SISTEMA
ABIERTO
CLASIFICACIN
Qu tipo de sistema es lo que representa la siguiente
imagen?
SISTEMA AISLADO
UNIVERSO
CLASIFICACIN
Qu tipo de sistema es lo que representa la siguiente
imagen?
SISTEMA
ABIERTO
Las variables termodinmicas se clasifican en dos
grandes grupos:
A) Variable Extensiva: Son aquellas variables que
dependen de la cantidad de materia, y su valor no
se puede definir en cualquier punto del sistema.
B) Variable Intensiva: Son aquellas variables que no
dependen de la cantidad de materia y su valor se
puede determinar en cualquier punto del sistema.
Ejemplo: Masa y Volumen.
Ejemplo: Densidad y Temperatura.
VARIABLES TERMODINMICAS
VARIABLES TERMODINMICAS
Para describir el estado de un
sistema termodinmico se emplea
una serie de magnitudes
macroscpicas observables y
medibles llamada variables de
estado, como: presin, volumen,
temperatura, masa o nmero de
mol.
Categora Variables Smbolo
Mecnica Presin y
Volumen
P y V
Trmica Temperatura
T
Material Composicin
qumica
Xn (Fraccin
Molar)
VARIABLES TERMODINMICAS
VARIABLES TERMODINMICAS
FUNCIONES DE ESTADO
Entre las variables termodinmicas
existen magnitudes llamadas funciones de
estado. Estas tienen un valor definido y
nico que depende solo del estado inicial
y final del sistema.
X = X final X inicial
A) Isotrmico: Proceso que se lleva a
cabo a temperatura constante.
B) Isobrico: Proceso que se lleva a
cabo a presin constante.
TIPOS DE PROCESOS
C) Adiabtico: Proceso en el cual no hay
transferencia de calor pero s
intercambio de trabajo entre el sistema
y el entorno.
PRIMER PRINCIPIO DE LA
TERMODINMICA
ENERGA INTERNA (U)
Corresponde a la totalidad
de la energa cintica y
potencial de las partculas
de un sistema.
Es una funcin de estado.
Es una variable extensiva.
CALOR (Q)
Se denomina calor (Q) a la
transferencia de energa que se
produce de un sistema a otro como
consecuencia de una diferencia de
temperatura.
El calor fluye desde el cuerpo de
mayor temperatura al de menor
temperatura hasta que ambos se
igualan (equilibrio trmico).
No es funcin de estado.
CALOR (Q)
CALOR (Q)
0 Q
0 Q
El sistema recibe calor
El sistema pierde calor
TRABAJO (W)
Se define como le energa que se
transfiere entre un sistema y su
entorno cuando entre ambos se ejerce
una fuerza.
Matemticamente se define como el
producto de la fuerza (F) aplicada
sobre un cuerpo y la distancia (d) que
este recorre.
W = F x d
No es funcin de estado.
TRABAJO (W)
El sistema realiza trabajo sobre el entorno
El entorno realiza trabajo sobre el sistema
W <0
W >0
SISTEMA
Q > 0
W > 0
W < 0
Q < 0
ENERGA INTERNA
El trabajo se
realiza contra
el ambiente
El trabajo se
realiza sobre
el sistema
El sistema
libera calor
El sistema
abosrbe calor
PRIMER PRINCIPIO DE LA TERMODINAMICA
Principio de la conservacin de la
energa, el cual establece que: la
energa en el universo permanece
constante. Esto quiere decir que la
energa solo se transfiere entre el
sistema y su entorno.
U = U
sistema
+ U
ambiente
PRIMER PRINCIPIO DE LA TERMODINAMICA
El primer principio de la
termodinmica se puede enunciar
como: la variacin de la energa
interna de un sistema es igual al
calor absorbido ms el trabajo
externo realizado por el sistema.
U = Q + W
EJEMPLO
Determina la variacin de energa interna para
un sistema que ha absorbido 2990 joule y
realiza un trabajo de 4000 joule sobre su
entorno.
Segn convenio de signos:
Q= 2990 J y W= - 4000 J
U = Q + W
U = 2990 J + (- 4000 J)
U = - 1010 J
Respuesta = El sistema ha disminuido su
energa interna en 1010 J.
EJERCICIO
El trabajo realizado cuando se comprime un gas
en un cilindro, es de 462 J. durante este
proceso hay una transferencia de calor de 128 J
del gas hacia los alrededores. Determina el
cambio de energa para el proceso
Segn convenio de signos:
Q= - 128 J y W= 462 J
U = Q + W
U = - 128 J + 462 J
U = 334 J
Respuesta = Como resultado de la compresin y
transferencia de calor, la energa interna del gas aumenta
ACTIVIDAD: RESPONDE
1. Qu es un sistema termodinmico? Menciona dos
ejemplos para cada tipo de sistemas, es decir, abierto,
cerrado y aislado.
2. Cules son las principales caractersticas de los sistemas
abierto, cerrado y aislado?
3. Qu diferencia existen entre las variables intensivas y
extensivas?
4. Cules de los siguientes conceptos: presin,
temperatura, volumen, trabajo, energa y calor, son
funciones de estado? justifica tu respuesta.
5. Qu es la energa? Menciona dos ejemplos de aplicacin
cotidiana, es decir, ejemplos de uso de energa.
6. Qu es una funcin de estado?
EJERCICIOS
1. Un gas se expande y realiza un trabajo
sobre los alrededores igual a 325 J. Al
mismo tiempo, absorbe 127 J de calor de su
alrededor. Determina el cambio de energa
del gas.
2. El trabajo realizado para comprimir un gas
es de 74J. Como resultado, libera 26 J de
calor hacia los alrededores. Determina el
cambio de energa del gas.
Muchas Gracias
Colegio Andrs Bello
Chiguayante
You might also like
- Plan de Trabajo Seguro - Proyecto Noviembre 2021Document22 pagesPlan de Trabajo Seguro - Proyecto Noviembre 2021Percy R. Samaniego ValdezNo ratings yet
- Plan de Trabajo Proyectos 2021 Proyecto Alimentacion de MolinosDocument9 pagesPlan de Trabajo Proyectos 2021 Proyecto Alimentacion de MolinosPercy R. Samaniego ValdezNo ratings yet
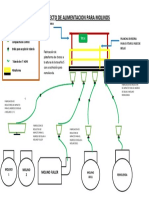
- Proyecto de alimentación para molinosDocument1 pageProyecto de alimentación para molinosPercy R. Samaniego ValdezNo ratings yet
- 000 PROPUESTA SICAYA - 4 PISOS-Model 01Document1 page000 PROPUESTA SICAYA - 4 PISOS-Model 01Percy R. Samaniego ValdezNo ratings yet
- Proyección de vigas y planos de puente grúaDocument2 pagesProyección de vigas y planos de puente grúaPercy R. Samaniego ValdezNo ratings yet
- Planos PlataformaDocument2 pagesPlanos PlataformaPercy R. Samaniego ValdezNo ratings yet
- Plano Cajon 2Document1 pagePlano Cajon 2Percy R. Samaniego ValdezNo ratings yet
- Reductor y DuctoDocument2 pagesReductor y DuctoPercy R. Samaniego ValdezNo ratings yet
- Plano CajonDocument1 pagePlano CajonPercy R. Samaniego ValdezNo ratings yet
- Hzssosepre17-B PlantaDocument1 pageHzssosepre17-B PlantaPercy R. Samaniego ValdezNo ratings yet
- EjemploDocument1 pageEjemploPercy R. Samaniego ValdezNo ratings yet
- 000 PROPUESTA SICAYA - 4 PISOS-Model 02Document1 page000 PROPUESTA SICAYA - 4 PISOS-Model 02Percy R. Samaniego ValdezNo ratings yet
- 1 ProyecccionDocument9 pages1 ProyecccionPercy R. Samaniego ValdezNo ratings yet
- EjemploDocument1 pageEjemploPercy R. Samaniego ValdezNo ratings yet
- 000 PROPUESTA SICAYA - 4 PISOS-ModelDocument1 page000 PROPUESTA SICAYA - 4 PISOS-ModelPercy R. Samaniego ValdezNo ratings yet
- Diseño de Maquinas N°1Document7 pagesDiseño de Maquinas N°1Percy R. Samaniego ValdezNo ratings yet
- Plano CajonDocument1 pagePlano CajonPercy R. Samaniego ValdezNo ratings yet
- Reductor y DuctoDocument2 pagesReductor y DuctoPercy R. Samaniego ValdezNo ratings yet
- Samaniego Inves. 1Document7 pagesSamaniego Inves. 1Percy R. Samaniego ValdezNo ratings yet
- Plano Cajon 2Document1 pagePlano Cajon 2Percy R. Samaniego ValdezNo ratings yet
- Marco Teorico Cap 2Document2 pagesMarco Teorico Cap 2Percy R. Samaniego ValdezNo ratings yet
- PLANOS PLATAFORMA EspecificadoDocument2 pagesPLANOS PLATAFORMA EspecificadoPercy R. Samaniego ValdezNo ratings yet
- INTRODUCCIÓNDocument7 pagesINTRODUCCIÓNPercy R. Samaniego ValdezNo ratings yet
- Ficha de Obtención de PatentesDocument2 pagesFicha de Obtención de PatentesPercy R. Samaniego ValdezNo ratings yet
- INTRODUCCIÓNDocument7 pagesINTRODUCCIÓNPercy R. Samaniego ValdezNo ratings yet
- Aministracion de SueldoDocument6 pagesAministracion de SueldoPercy R. Samaniego ValdezNo ratings yet
- Samaniego Ryac N°1Document10 pagesSamaniego Ryac N°1Percy R. Samaniego ValdezNo ratings yet
- Manual del operador de la perforadora Quasar NVDocument72 pagesManual del operador de la perforadora Quasar NVkelvisba0% (1)
- Programa CunetasDocument8 pagesPrograma CunetasPercy R. Samaniego ValdezNo ratings yet
- Ficha de Obtención de PatentesDocument2 pagesFicha de Obtención de PatentesPercy R. Samaniego ValdezNo ratings yet
- Informe Academico CompetenciaDocument17 pagesInforme Academico CompetenciaHyoudou Issei100% (1)
- Ley Del Mínimo y de La ToleranciaDocument9 pagesLey Del Mínimo y de La ToleranciaAlejandraNo ratings yet
- Lab 01 Conc. MineralesDocument15 pagesLab 01 Conc. MineralesDanthe VergaraNo ratings yet
- Placas Tectonicas y SismologiaDocument13 pagesPlacas Tectonicas y SismologiaErikita MoratóNo ratings yet
- LEY de COULOMB Informe de Fisica IIIDocument14 pagesLEY de COULOMB Informe de Fisica IIIHarold Paredes Mardini29% (7)
- Tipos de AguaDocument5 pagesTipos de AguaedisonNo ratings yet
- Grupo 5 Montajes de LaboratorioDocument4 pagesGrupo 5 Montajes de Laboratoriotoga-sanNo ratings yet
- Marcos PortafolioDocument5 pagesMarcos PortafolioDavid ZamoraNo ratings yet
- Esp TecDocument135 pagesEsp TecdanielNo ratings yet
- Trabajo ComunitariaDocument13 pagesTrabajo ComunitariaLaleska perdomoNo ratings yet
- Fuentes de Eenergia - GeologiaDocument5 pagesFuentes de Eenergia - GeologiaNelly Hermitaño AlcantaraNo ratings yet
- Trabajo CristalografiaDocument14 pagesTrabajo CristalografiaHarold Junior Seminario NavarroNo ratings yet
- Pictogramas de Identificacion de Peligros Sistema de ClasificacionDocument42 pagesPictogramas de Identificacion de Peligros Sistema de ClasificacionEduardo Camarena SullcaNo ratings yet
- García Frank S7P4 Tarea7Document6 pagesGarcía Frank S7P4 Tarea7alain garciaNo ratings yet
- Expediente Tecnico - Remodelacion Baños TerpelDocument73 pagesExpediente Tecnico - Remodelacion Baños Terpelrobinson matta ramirezNo ratings yet
- Diapositivas de MaderasDocument10 pagesDiapositivas de MaderasdanmetotorquiNo ratings yet
- J9 La Palma Valle Del Lunarejo Laureles Las CanasDocument25 pagesJ9 La Palma Valle Del Lunarejo Laureles Las CanasMateus AlvezNo ratings yet
- Proyecto Piedra LargaDocument232 pagesProyecto Piedra LargaLuis Alberto Otero HerreraNo ratings yet
- Informe - Smart MiningDocument13 pagesInforme - Smart Miningerick tacillaNo ratings yet
- Guía de Factores de La Producción VegetalDocument7 pagesGuía de Factores de La Producción VegetalAndres Manuel Villalobos CastroNo ratings yet
- 2 - Gabriel HernanDocument28 pages2 - Gabriel HernanJaviercito VelascoNo ratings yet
- FÍSICA GENERAL. Dr. Roberto Pedro Duarte Zamorano 2010 Departamento de Física Universidad de SonoraDocument26 pagesFÍSICA GENERAL. Dr. Roberto Pedro Duarte Zamorano 2010 Departamento de Física Universidad de SonoraKoraima Sofía Pino PanihuaraNo ratings yet
- Mantenimientos en Lineas de TransmisiónDocument5 pagesMantenimientos en Lineas de TransmisiónBenny JoseNo ratings yet
- Amaudruz. Nosotros Los RacistasDocument83 pagesAmaudruz. Nosotros Los RacistasIvan GrassNo ratings yet
- Estudio HidrologicoDocument15 pagesEstudio HidrologicoEdi R SáezNo ratings yet
- Trabajo de TermodinamicaDocument6 pagesTrabajo de TermodinamicaBryan Milla TrejoNo ratings yet
- Eva Nat 7b b4 l10 Tablet MediaDocument13 pagesEva Nat 7b b4 l10 Tablet Mediajose marioNo ratings yet
- Planilla - Gravedad Específica y Peso UnitarioDocument1 pagePlanilla - Gravedad Específica y Peso UnitarioJuniior PkNo ratings yet
- Trabajo de Ciencias - OdtDocument19 pagesTrabajo de Ciencias - OdtMartín MoralesNo ratings yet
- PTAP: Procesos de tratamiento de agua potableDocument31 pagesPTAP: Procesos de tratamiento de agua potablegsr600ibagueNo ratings yet